
���}Ŀ�����I(y��)ȼ��ú��ʯ�͵Ȼ�ʯȼ��ጷų�������������(NOx)��CO2��SO2�Ț��w��������Ⱦ�՚⡣���U���M��Ó����Ó̼��Ó��̎���Ɍ��F(xi��n)�Gɫ�h(hu��n)�����U�����á�
��.����
��֪H2��ȼ�����285.8kJ��mol��1
N2(g)��2O2(g)=2NO2(g) ��H����133kJ��mol��1
H2O(g)=H2O(l) ��H����44kJ��mol��1
���������£�H2߀ԭNO2����ˮ����������o�����|(zh��)�ğữ�W(xu��)����ʽ��___��
��.Ó̼����1����2L���]�����м���2molCO2��6molH2�����m��(d��ng)?sh��)Ĵ��������£��l(f��)������(y��ng)��CO2(g)��3H2(g)![]() CH3OH(l)��H2O(l) ��H<0
CH3OH(l)��H2O(l) ��H<0
��ԓ����(y��ng)�l(f��)�M�еėl����___(��͜ء����ߜء�������ضȡ�)
�����Д������f���˷���(y��ng)�_��ƽ���B(t��i)����___(����ĸ)��
a����Ϛ��w��ƽ�����������|(zh��)�����ֲ�׃ b��CO2��H2���w�e�֔�(sh��)���ֲ�׃
c��CO2��H2���D(zhu��n)������� d����Ϛ��w���ܶȱ��ֲ�׃
e��1molCO2���ɵ�ͬ�r��3 molH��H�I����
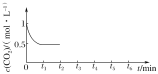
��CO2�ĝ���S�r�g(0��t2)׃����D��ʾ����t2�r�������ݷe�sСһ����t3�r�_��ƽ�⣬
t4�r���͜ضȣ�t5�r�_��ƽ�⣬Ո����t2��t6�r�g��CO2����S�r�g��׃��___��
��2����׃�ضȣ�ʹ����(y��ng)CO2(g)��3H2(g)![]() CH3OH(g)��H2O(g) ��H<0�е��������|(zh��)�����B(t��i)����ʼ�ضȡ��w�e��ͬ(T1�桢2L���]����)������(y��ng)�^���в��֔�(sh��)��(j��)Ҋ�±���
CH3OH(g)��H2O(g) ��H<0�е��������|(zh��)�����B(t��i)����ʼ�ضȡ��w�e��ͬ(T1�桢2L���]����)������(y��ng)�^���в��֔�(sh��)��(j��)Ҋ�±���
����(y��ng)�r�g | CO2(mol) | H2(mol) | CH3OH(mol) | H2O(mol) | |
����(y��ng)�� ��غ��� | 0min | 2 | 6 | 0 | 0 |
10min | 4.5 | ||||
20min | 1 | ||||
30min | 1 | ||||
����(y��ng)�� �^����� | 0min | 0 | 0 | 2 | 2 |
���_��ƽ��r������(y��ng)��?q��)��ȣ�ƽ��rCH3OH�ĝ��c(��)___c(��)(����>����<����������)��
�ڌ�����(y��ng)��ǰ10min��(n��i)��ƽ������(y��ng)����v(CH3OH)��___���������l����׃����r�£���30 min�rֻ��׃�ض���T2�棬�˕rH2�����|(zh��)������3.2mol���tT1___(����>����<����������)T2����30min�rֻ���������ٳ���1 molCO2(g)��1molH2O(g)���tƽ��___(��������������������������)�Ƅӡ�
��3�������˹�������ÿɌ�CO2�D(zhu��n)������ᣬ����(y��ng)ԭ���2CO2��2H2O=2HCOOH��O2���b����D��ʾ��
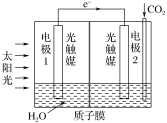
��늘O2��늘O����(y��ng)ʽ��____��
���ژ˜ʠ�r�£���(d��ng)늘O2����11.2LCO2����(y��ng)����Փ��늘O1��Һ�w�|(zh��)��___(���������������p����)___g��
���𰸡�4H2(g)��2NO2(g)=N2(g)��4H2O(g) ��H����1100.2kJ��mol��1 �͜� de 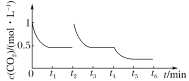 < 0.025mol��L��1��min��1 < �� CO2��2H����2e��=HCOOH �p�� 9
< 0.025mol��L��1��min��1 < �� CO2��2H����2e��=HCOOH �p�� 9
��������
����(j��)�}���֪�����}����ữ�W(xu��)����ʽ�ĕ��������W(xu��)ƽ���Ƅӡ����W(xu��)����(y��ng)���ʡ�늻��W(xu��)֪�R���\���w˹���ɡ���������ԭ����![]() ��늻��W(xu��)ԭ��������
��늻��W(xu��)ԭ��������
��.H2��ȼ�����285.8kJmol1���t��.2H2(g)+O2(g)=2H2O(l) ��H=571.6kJmol1����.N2(g)+2O2(g)=2NO2(g) ��H=+133kJmol1��.H2O(g)=H2O(l) ��H=44kJmol1����(j��)�w˹���ɢ���2���ۡ�4�ɵã�4H2(g)+2NO2(g)=N2(g)+4H2O(g)���t����H=2��(571.6kJmol1)133kJmol14��(44kJmol1) = 1100.2kJmol1���ʷ���(y��ng)�ữ�W(xu��)����ʽ�飺4H2(g)+2NO2(g)=N2(g)+4H2O(g) ��H=1100.2kJmol1��
�ʴ𰸞飺4H2(g)+2NO2(g)=N2(g)+4H2O(g) ��H=1100.2kJmol1��
��. (1)��CO2(g)+3H2(g)�TCH3OH(l)+H2O(l)����׃��S<0���t����(y��ng)��׃��H<0���͜��M���HT��S<0
�ʴ𰸞飺�͜أ�
��a.�״���ˮ��Һ�w��CO2��H2����ʼ���|(zh��)����֮�Ȟ�1:3������(y��ng)�����|(zh��)����1:3����(y��ng)���ʻ�Ϛ��w��CO2��H2����ʼ���|(zh��)����֮�Ȟ�1:3��ƽ��Ħ���|(zh��)����(sh��)ֵ��ƽ�����������|(zh��)��ʼ�K���ֲ�׃���o���Д���ƽ���B(t��i)����a�e�`��
b.��a�з�������֪CO2��H2���w�e�֔�(sh��)��(sh��)ֵʼ�K���ֲ�׃���o���Д���ƽ���B(t��i)����b�e�`��
c.��a�з�������֪CO2��H2���D(zhu��n)����ʼ�K��ȣ��o���Д���ƽ���B(t��i)����c�e�`��
d.�����ݷe��׃����Ϛ��w�|(zh��)���pС���S����(y��ng)�M�л�Ϛ��w�ܶȜpС����(d��ng)��Ϛ��w���ܶȲ�׃������(y��ng)���_ƽ�⣬��d���_��
e.1molCO2���ɵ�ͬ�r��3molHH�I���ѣ���1molCO2���ɵ�ͬ�r����3molHH�I���������������c����������ȣ�����(y��ng)���_ƽ�⣬��e���_��
�ʴ𰸞飺de��
��t2�rCO2��Ȟ�0.5mol/L���t�����׃������(1mol/L0.5mol/L)��3=1.5mol/L�����ƽ���Ȟ�![]() 1.5mol/L=1.5mol/L���tԓ�ض���ƽ�ⳣ��(sh��)
1.5mol/L=1.5mol/L���tԓ�ض���ƽ�ⳣ��(sh��)![]() ����t2�r�������ݷe�sСһ����˲�gCO2���׃?y��u)?/span>1mol/L����������ƽ����������(y��ng)�����Ƅӣ�t3�r�_��ƽ��r����Ч���_ʼ�w�e�sСһ�����_��ƽ�⣬�O(sh��)�˕rCO2��Ȟ�xmol/L���t��
����t2�r�������ݷe�sСһ����˲�gCO2���׃?y��u)?/span>1mol/L����������ƽ����������(y��ng)�����Ƅӣ�t3�r�_��ƽ��r����Ч���_ʼ�w�e�sСһ�����_��ƽ�⣬�O(sh��)�˕rCO2��Ȟ�xmol/L���t��
CO2(g)+3H2(g)CH3OH(l)+H2O(l)
�_ʼ(mol/L): 2 6
�D(zhu��n)��(mol/L): 2x 63x
ƽ��(mol/L) :x 3x
�t![]() �����x=0.5��
�����x=0.5��
t3�r�_��ƽ��rCO2��Ȟ�0.5mol/L��t4�r���͜ضȣ�˲�gCO2��Ȳ�׃��������(y��ng)��şᷴ��(y��ng)������ƽ����������(y��ng)�Ƅӣ�CO2��ȜpС������t2t6CO2�ĝ���S�r�g��׃����D��
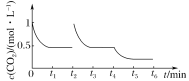 ��
��
�ʴ𰸞飺  ��
��
�ʴ𰸞飺<��
��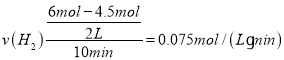 ������֮�ȵ��ڻ��W(xu��)Ӌ����(sh��)֮�ȣ�v(CH3OH)=
������֮�ȵ��ڻ��W(xu��)Ӌ����(sh��)֮�ȣ�v(CH3OH)=![]() v(H2)=0.025mol/(Lmin)��20min�r���D(zhu��n)����CO2��2mol1mol=1mol���t���ɵ�CH3OH��1mol����30min�rCH3OH��1mol����20min�r���_ƽ�⣬
v(H2)=0.025mol/(Lmin)��20min�r���D(zhu��n)����CO2��2mol1mol=1mol���t���ɵ�CH3OH��1mol����30min�rCH3OH��1mol����20min�r���_ƽ�⣬
CO2(g)+3H2(g)CH3OH(g)+H2O(g)
�_ʼ(mol/L): 2 6 0 0
�D(zhu��n)��(mol/L): 1 3 1 1
ƽ��(mol/L): 1 3 1 1
��ƽ�ⳣ��(sh��) ��
��
ƽ��r����6mol1mol��3=3mol�����ƽ���Ȟ�![]() ���������l����׃����r�£���30min�rֻ��׃�ض�T2�棬�˕rH2�����|(zh��)������3.2mol��ƽ�������Ƅӣ��������������������(y��ng)��şᷴ��(y��ng)���������ߜضȣ���T1<T2��������(y��ng)����30min�rֻ���������ٳ���1molCO2(g)��1molH2O(g)���˕r�����
���������l����׃����r�£���30min�rֻ��׃�ض�T2�棬�˕rH2�����|(zh��)������3.2mol��ƽ�������Ƅӣ��������������������(y��ng)��şᷴ��(y��ng)���������ߜضȣ���T1<T2��������(y��ng)����30min�rֻ���������ٳ���1molCO2(g)��1molH2O(g)���˕r�����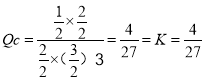 ���tƽ�ⲻ�Ƅӣ�
���tƽ�ⲻ�Ƅӣ�
�ʴ𰸞飺0.025mol/(Lmin)��<������
(3)��늘O2�����O�����O�϶�����̼����Ӻ͚��x�ӷ���(y��ng)����HCOOH��늘O����(y��ng)ʽ��CO2+2H++2e=HCOOH��
�ʴ𰸞飺CO2+2H++2e=HCOOH��
��늘O1ʽ��ؓ�O���l(f��)����늘O����(y��ng)ʽ��2H2O4e=4H++O2������Փ���S����(d��ng)늘O2����11.2L CO2����(y��ng)��������̼�����|(zh��)������![]() ���D(zhu��n)����Ӟ�0.5mol��2=1mol��늘O1�҅��ӷ���(y��ng)��ˮ���|(zh��)����18g/mol��
���D(zhu��n)����Ӟ�0.5mol��2=1mol��늘O1�҅��ӷ���(y��ng)��ˮ���|(zh��)����18g/mol��![]() =9g����늘O1����Փ�pСҺ�w�|(zh��)����9g��
=9g����늘O1����Փ�pСҺ�w�|(zh��)����9g��
�ʴ𰸞飺�pС��9��



| �꼉 | �����n�� | �꼉 | �����n�� |
| ��һ | ��һ���M�n�����]�� | ��һ | ��һ���M�n�����]�� |
| �߶� | �߶����M�n�����]�� | ���� | �������M�n�����]�� |
| ���� | �������M�n�����]�� | ���� | �������M�n�����]�� |
��Ŀ�����л��W(xu��) ��Դ�� �}�ͣ�
���}Ŀ�����Ќ��ڷ���(y��ng)��![]() ���f�����_����( )
���f�����_����( )
A.�������c߀ԭ�����|(zh��)���Ȟ�1:2
B.![]() ����������ˮ��߀ԭ��
����������ˮ��߀ԭ��
C.����![]() �t��
�t��![]() ��Ӱl(f��)���D(zhu��n)��
��Ӱl(f��)���D(zhu��n)��
D.�����a(ch��n)���c߀ԭ�a(ch��n)������|(zh��)�����Ȟ�1:2
�鿴�𰸺ͽ���>>
��Ŀ�����л��W(xu��) ��Դ�� �}�ͣ�
���}Ŀ����֪X��һ�N��Ҋ��ĝ���Һ����ʹ����׃�ڡ�A�cX����(y��ng)���D(zhu��n)���P(gu��n)ϵ��D��ʾ�����з���(y��ng)�l�������֮a(ch��n)�������ȥ���t�������P(gu��n)�f�����_���ǣ� ��
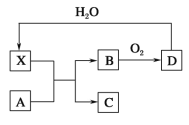
A.Xʹ����׃����Ҫ�w�F(xi��n)��X����ˮ��
B.��A���F���t����A�cX���Ҝ��¼�����ȫ����(y��ng)
C.��A��̼���|(zh��)���t��Cͨ�������ij���ʯ��ˮ�У�һ�����^�쵽�а�ɫ�����a(ch��n)��
D.��B�D(zhu��n)����D�ķ���(y��ng)�ǹ��I(y��)�Ƃ�X�^���е���Ҫ����(y��ng)
�鿴�𰸺ͽ���>>
��Ŀ�����л��W(xu��) ��Դ�� �}�ͣ�
���}Ŀ������ҳ����ü�ȩ���y��(NH4)2SO4��Ʒ�е����|(zh��)���֔�(sh��)���䷴��(y��ng)ԭ��飺4NH4+��6HCHO=3H����6H2O��(CH2)6N4H��[�ζ��r��1mol(CH2)6N4H���c1molH���ஔ(d��ng)]��Ȼ����NaOH�˜���Һ�ζ�����(y��ng)���ɵ��ᡣij�dȤС�M�ü�ȩ���M��������
���E�� �Qȡ��Ʒ1.500g��
���E�� ����Ʒ�ܽ����ȫ�D(zhu��n)�Ƶ�250mL����ƿ�У����ݣ���֓u��
���E�� ��ȡ25.00mL��Ʒ��Һ��250mL�F��ƿ�У�����10mL20%�����Լ�ȩ��Һ���u���o��5min����1��2�η�̪ԇҺ����NaOH�˜���Һ�ζ����K�c�������������������؏�(f��)2�Ρ�
��1������(j��)���E����գ�
�ىAʽ�ζ��������sˮϴ���ֱ�Ӽ���NaOH�˜���Һ�M�еζ����t�y�Ø�Ʒ�е����|(zh��)���֔�(sh��)___(����ƫ��������ƫ���������oӰ���)��
���F��ƿ�����sˮϴ���ˮδ���M���t�ζ��r��ȥNaOH�˜���Һ���w�e___(����ƫ��������ƫС�������oӰ���)��
���ζ��Y(ji��)���ķ�����K������___��׃��������C�y׃����
�۵ζ��r߅��߅�u���F��ƿ���۾���(y��ng)�^��___��
�ܵζ��_���K�c�F(xi��n)��__ ��
��2���ζ��Y(ji��)�����±���ʾ��
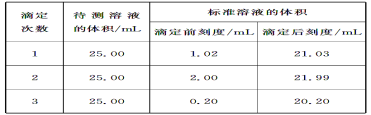
��NaOH�˜���Һ�ĝ�Ȟ�0.1010mol/L���tԓ��Ʒ�е����|(zh��)���֔�(sh��)��___��(����4λ��Ч��(sh��)��)
�鿴�𰸺ͽ���>>
��Ŀ�����л��W(xu��) ��Դ�� �}�ͣ�
���}Ŀ���r(n��ng)ˎ������Һ����Ҫ�ɷ���CuSO4�����Ѓɂ�����(y��ng)����CuSO4���ɡ�
��Cu��2H2SO4(��)![]() CuSO4��SO2����2H2O
CuSO4��SO2����2H2O
��CuO��H2SO4��CuSO4��H2O
����(y��ng)�ٵĸ��a(ch��n)��SO2�Ǵ����Ⱦ�����NaOH��Һ���գ��l(f��)������(y��ng)�Ļ��W(xu��)����ʽ��(����)
A.NaOH��SO2��Na2SO3
B.NaOH��SO2��Na2SO3��H2O
C.2NaOH��SO2��Na2SO3��H2O
D.2NaOH��SO2��2NaHSO3��H2O
�鿴�𰸺ͽ���>>
��Ŀ�����л��W(xu��) ��Դ�� �}�ͣ�
���}Ŀ����0.2molij�ЙC���0.5mol������һ���]������ȼ���îa(ch��n)���CO2��CO��H2O(��)���a(ch��n)��ͨ�^������r,��������|(zh��)��������7.2g;��ͨ�^�Ɵ�������~�r,�����~���|(zh��)���p����3.2g;��ͨ�^�Aʯ�ҕr,�Aʯ�ҵ��|(zh��)��������17.6g��ԓ�ЙC��Ļ��W(xu��)ʽ��( )
A.C2H4B.C2H6OC.C2H6O2D.C3H6O3
�鿴�𰸺ͽ���>>
��Ŀ�����л��W(xu��) ��Դ�� �}�ͣ�
���}Ŀ����D��ʾ���׳صĿ�����(y��ng)ʽ�飺N2H4+O2 =N2+H2O�������P(gu��n)��ԓ늳ع����r���f�����_���ǣ� ��
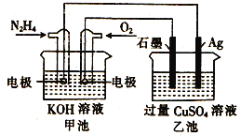
A.ԓ�b�ù����r���׳�����Һ��pH����
B.�ҳ���ؓ�O����(y��ng)��2Ag-2e-+SO42-=Ag2SO4
C.�׳����O����(y��ng)O2+4e-+4H+=2H2O
D.��(d��ng)�׳�������0.05molN2H4�r���ҳ�����Փ�����a(ch��n)��6.4g���w
�鿴�𰸺ͽ���>>
��Ŀ�����л��W(xu��) ��Դ�� �}�ͣ�
���}Ŀ���ἤ��늳ؿ������������(d��o)���Ĺ����Դ��һ�N�ἤ��늳صĻ����Y(ji��)��(g��u)��D��ʾ����������늽��|(zh��)�ğoˮLiCl-KCl������ܟ����ں�늳ؼ���˲�gݔ����ܡ�ԓ늳ؿ�����(y��ng)�飺PbSO4+2LiCl+Ca = CaCl2+Li2SO4+Pb���������P(gu��n)�f�����_����

A. ���O����(y��ng)ʽ��Ca + 2Cl����2e�� = CaCl2
B. ����^���У�Li+��ؓ�O�Ƅ�
C. �]�D(zhu��n)��0.1mol��ӣ���Փ������20.7 g Pb
D. ���ؕr������ؓ�O�g�����������z��Ӌ��ָᘲ�ƫ�D(zhu��n)
�鿴�𰸺ͽ���>>
��Ŀ�����л��W(xu��) ��Դ�� �}�ͣ�
���}Ŀ��������ij�dȤС�M��������ɳ�Ĵ��}�M���ἃ�������̈D��Ո�ش����І��}��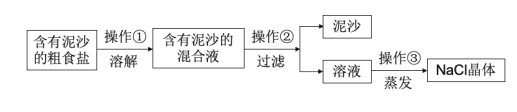
��1�����������õ��IJ����x����__��
��2�����������������������__��
��3���������NaCl�Įa(ch��n)��ƫ�ͣ��t���ܵ�ԭ��__�����x헣���
A���^�V�r�V�����Ɠp
B�����l(f��)�r�]����������
C���ܽ⺬��ɳ�Ĵ��}�r������ˮ������
D�������Ȼ��c���w�]�к�ɣ�����ˮ��
E���^�V��ĞV���ǝ�ģ����ϵ�ˮ�ܽ���һЩ�Ȼ��c
�鿴�𰸺ͽ���>>
���H�W(xu��)У��(y��u)�x - ����(x��)���б� - ԇ�}�б�
����ʡ��(li��n)�W(w��ng)�`���Ͳ�����Ϣ�e��ƽ�_ | �W(w��ng)���к���Ϣ�e�^(q��) | ����p�_�e�^(q��) | ��vʷ̓�o���x�к���Ϣ�e�^(q��) | �����֙�(qu��n)�e�^(q��)
�`���Ͳ�����Ϣ�e���Ԓ��027-86699610 �e���]�䣺58377363@163.com