
科目: 來源: 題型:
【題目】我國秦俑彩繪和漢代器物上用的顏料被稱為“中國藍”、“中國紫”,直到近年來人們才研究出來其成分為BaCuSi4O10,BaCuSi2O6。
(1)“中國藍”、“中國紫”中均具有Cun+離子,n=___,基態時該陽離子的價電子排布式為______。
(2)在5500年前,古代埃及人就己經知道如何合成藍色顏料—“埃及藍”CaCuSi4O10,其合成原料中用CaCO3代替了BaCO3,其它和“中國藍”一致。CO32一中鍵角∠OCO為___。根據所學,從原料分解的角度判斷“埃及藍”的合成溫度比“中國藍”更___(填“高”或“低”)。
(3)配離子Cu(CN)32-中,中心離子的雜化類型是___________,該配離子的空間構型為___________;CN-中配位原子是___________ (填名稱)。
(4)CaCux合金可看作由如圖所示的(a)、(b)兩種原子層交替堆積排列而成。(a)是由Cu和Ca共同組成的層,層中Cu—Cu之間由實線相連;(b)是完全由Cu原子組成的層,Cu—Cu之間也由實線相連。圖中虛線構建的六邊形,表示由這兩種層平行堆積時垂直于層的相對位置;(c)是由(a)和(b)兩種原子層交替堆積成CaCux合金的晶體結構圖。在這種結構中,同一層的Ca—Cu距離為294pm,相鄰兩層的Ca—Cu距離為327pm。
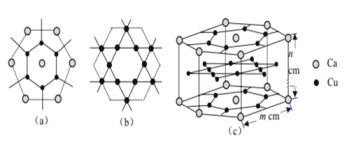
①該晶胞中Ca有___________個Cu原子配位(不一定要等距最近)。
②同一層中,Ca原子之間的最短距離是___________pm,設NA為阿伏加德羅常數的值,CaCu晶體的密度是___________g/cm3(用含m、n的式子表示)。
查看答案和解析>>
科目: 來源: 題型:
【題目】鈷、鐵、鎵、砷的單質及其化合物在生產生活中有重要的應用。回答下列問題:
(1)寫出 As 的基態原子的電子排布式_____。
(2)將 NaNO3 和 Na2O 在一定條件下反應得到一種白色晶體,已知其中陰離子與 SO42-互為等 電子體,則該陰離子的化學式是_____。
(3)Fe3+、Co3+與 N3-、CN-等可形成絡合離子。
①K3[Fe(CN)6]可用于檢驗 Fe2+,配體 CN-中碳原子雜化軌道類型為_____。
②[Co(N3)(NH3)5]SO4 中 Co 的配位數為_____,其配離子中含有的化學鍵類型為___(填離子鍵、共價鍵、配位鍵)。
查看答案和解析>>
科目: 來源: 題型:
【題目】完成下列填空。
(1)在 25℃、101kPa 時,C(s)、H2(g)、CH3COOH(l)的燃燒熱分別為 393.5kJ/mol、285.8kJ/mol、870.3kJ/mol,則 2C(s)+2H2(g)+O2(g)= CH3COOH(l)的△H=___________。
(2)溫度為 T 時,在 2 L 的密閉容器中加入 2.0 mol SO2 和 1.0 mol O2 發生反應,達到平衡時容器內氣體壓強變為起始時的 0.7 倍。該反應的平衡常數為_____。
(3)在一定體積 pH=12 的 Ba(OH)2 溶液中,逐滴加入一定物質的量濃度的 NaHSO4 溶液, 當溶液中的 Ba2+恰好完全沉淀時,溶液 pH=11。若反應后溶液的體積等于 Ba(OH)2 溶液與 NaHSO4 溶液的體積之和,則 Ba(OH)2 溶液與 NaHSO4 溶液____
(4)利用如圖所示的電解裝置,可將霧霾中的 NO、SO2 轉化為硫酸銨,從而實現廢氣的回 收再利用。通入 NO 的電極反應式為_____;若通入的 NO 體積為 4.48 L(標況下),則理論上另一電極通入 SO2 的物質的量應為_________。

查看答案和解析>>
科目: 來源: 題型:
【題目】(1)下列幾種烴類物質:

①正四面體烷的二氯取代產物有_____種;立方烷的二氯取代產物有_____種。
② 關于苯和環辛四烯的說法正確的是_____(填字母符號)。
A 都能使酸性 KMnO4 溶液褪色
B 都能與 H2 發生加成反應,等質量的苯和環辛四烯消耗 H2 的物質的量之比為 3:4
C 都是碳碳單鍵和碳碳雙鍵交替結構
D 都能發生氧化反應
(2)已知:
①R—NO2 ![]() R—NH2;
R—NH2;
②![]() +HO-SO3H
+HO-SO3H +H2O
+H2O
③苯環上原有的取代基對新導入的取代基進入苯環的位置有顯著影響。以下是用苯為原料制備某些化合物的轉化關系圖:

④A 轉化為 B 的化學方程式是_____。
⑤在“ ”的所有反應中屬于取代反應的是________(填字母),屬于加成反應的是_____(填字母)。
”的所有反應中屬于取代反應的是________(填字母),屬于加成反應的是_____(填字母)。
查看答案和解析>>
科目: 來源: 題型:
【題目】(1)分子式為 C2H6O 的有機物,有兩種同分異構體,乙醇(CH3CH2OH)、甲醚(CH3OCH3),則通過下列方法,不可能將二者區別開來的是 (_________)
A.紅外光譜 B. 1H 核磁共振譜 C.質譜法 D.與鈉反應
(2)有機物 A 只含有 C、H、O 三種元素,常用作有機合成的中間體。16.8g 該有機物在足 量 O2中充分燃燒生成 44.0gCO2 和 14.4gH2O,質譜圖表明其相對分子質量為 84,分析其紅 外光譜圖可知 A 分子中含有 O-H 鍵和位于端點處的 C C 鍵,核磁共振氫譜上有三組峰, 峰面積之比為6:1:1。A的結構簡式是______________________。
(3)已知乙烯分子是平面結構, 1,2-二氯乙烯可形成![]() 和
和![]() 兩種不 同的空間異構體,稱為順反異構。下列能形成類似上述空間異構體的是(_________)
兩種不 同的空間異構體,稱為順反異構。下列能形成類似上述空間異構體的是(_________)
A.1-丙烯 B.4-辛烯 C.1-丁烯 D.2-甲基-1-丙烯
(4)請寫出 C(CH3)3Br與NaOH溶液、乙醇混合加熱的反應方程式__________________
查看答案和解析>>
科目: 來源: 題型:
【題目】(1)已知反應2HI(g)=H2(g) + I2(g)的△H=+11kJ·mol-1,1molH2(g)、1molI2(g)分子中化學鍵斷裂時分別需要吸收436KJ、151KJ的能量,則1molHI(g)分子中化學鍵斷裂時需吸收的能量為___kJ。
(2)已知某密閉容器中存在下列平衡:CO(g)+H2O(g) ![]() CO2(g)+H2(g),CO的平衡物質的量濃度c(CO)與溫度T的關系如圖所示。
CO2(g)+H2(g),CO的平衡物質的量濃度c(CO)與溫度T的關系如圖所示。

①該反應△H__________ 0(填“>”或“<”)
②若T1、T2時的平衡常數分別為K1、K2,則K1_______K2(填“>”、“<”或“=”)。
③T3時在某剛性容器中按1:2投入CO(g)和H2O(g),達到平衡后測得CO的轉化率為75%,則T3時平衡常數K3=____________。
(3)在恒容密閉容器中,加入足量的MoS2和O2,僅發生反應: 2MoS2(s)+7O2(g) ![]() 2MoO3(s)+4SO2(g) ΔH。
2MoO3(s)+4SO2(g) ΔH。
測得氧氣的平衡轉化率與起始壓強、溫度的關系如圖所示:

①p1、p2、p3的大小:_________。
②若初始時通入7.0 mol O2,p2為7.0 kPa,則A點平衡常數Kp=________(用氣體平衡分壓代替氣體平衡濃度計算,分壓=總壓×氣體的物質的量分數,寫出計算式即可)。
(4)中科院蘭州化學物理研究所用Fe3(CO)12/ZSM-5催化CO2加氫合成低碳烯烴反應,所得產物含CH4、C3H6、C4H8等副產物,反應過程如圖。

催化劑中添加Na、K、Cu助劑后(助劑也起催化作用)可改變反應的選擇性,在其他條件相同時,添加不同助劑,經過相同時間后測得CO2轉化率和各產物的物質的量分數如下表。
助劑 | CO2轉化率(%) | 各產物在所有產物中的占比(%) | ||
C2H4 | C3H6 | 其他 | ||
Na | 42.5 | 35.9 | 39.6 | 24.5 |
K | 27.2 | 75.6 | 22.8 | 1.6 |
Cu | 9.8 | 80.7 | 12.5 | 6.8 |
①欲提高單位時間內乙烯的產量,在Fe3(CO)12/ZSM-5中添加_______助劑效果最好;加入助劑能提高單位時間內乙烯產量的根本原因是_____;
②下列說法正確的是______;
a 第ⅰ步所反應為:CO2+H2![]() CO+H2O
CO+H2O
b 第ⅰ步反應的活化能低于第ⅱ步
c 催化劑助劑主要在低聚反應、異構化反應環節起作用
d Fe3(CO)12/ZSM-5使CO2加氫合成低碳烯烴的ΔH減小
e 添加不同助劑后,反應的平衡常數各不相同
查看答案和解析>>
科目: 來源: 題型:
【題目】有關晶體的結構如圖所示,下列說法中不正確的是( )

A. 在NaCl晶體中,距Na+最近的Cl-有6個
B. 在CaF2晶體中,每個晶胞平均占有4個Ca2+
C. 在金剛石晶體中,碳原子與碳碳鍵個數的比為1∶2
D. 該氣態團簇分子的分子式為EF或FE
查看答案和解析>>
科目: 來源: 題型:
【題目】高錳酸鉀是常用的氧化劑。工業上以軟錳礦(主要成分是MnO2)為原料制備高錳酸鉀晶體。中間產物為錳酸鉀。下圖是實驗室模擬制備KMnO4晶體的操作流程:

已知:錳酸鉀(K2MnO4)是墨綠色晶體,其水溶液呈深綠色,這是錳酸根離子(MnO42-)在水溶液中的特征顏色,在強堿性溶液中能穩定存在;在酸性、中性和弱堿性環境下,MnO42-會發生自身氧化還原反應,生成MnO4-和MnO2。
回答下列問題:
(1)KOH的電子式為______,煅燒KOH和軟錳礦的混合物應放在_______中加熱(填標號)。
a.燒杯 b.瓷坩堝 c.蒸發皿 d.鐵坩堝
(2)調節溶液pH過程中,所得氧化產物與還原產物的物質的量之比為______。
(3)趁熱過濾的目的是_______________________________。
(4)已知20℃時K2SO4、KCl、CH3COOK的溶解度分別為11.1g、34g、217g,則從理論上分析,選用下列酸中__________(填標號),得到的高錳酸鉀晶體純度更高。
a.稀硫酸 b.濃鹽酸 c.醋酸 d.稀鹽酸
(5)產品中KMnO4的定量分析:
①配制濃度為0.1250mg·mL-1的KMnO4標準溶液100mL。
②將上述溶液稀釋為濃度分別為2.5、5.0、7.5、10.0、12.5、15.0(單位:mg·L-1)的溶液,分別測定不同濃度溶液對光的吸收程度,并將測定結果繪制成曲線如下。

③稱取KMnO4樣品(不含K2MnO4)0.1250g按步驟①配得產品溶液1000mL,取10mL稀釋至100mL,然后按步驟②的方法進行測定,兩次測定所得的吸光度分別為0.149、0.151,則樣品中KMnO4的質量分數為____。
(6)酸性KMnO4溶液與FeSO4溶液反應的離子方程式為_______________________。
查看答案和解析>>
科目: 來源: 題型:
【題目】下列描述中正確的是
A. CS2為V形的極性分子
B. ClO3—的空間構型為平面三角形
C. SF6中有6對相同的成鍵電子對
D. SiF4和SO32—的中心原子均為sp2雜化
查看答案和解析>>
科目: 來源: 題型:
【題目】一種熔融碳酸鹽燃料電池原理示意如圖。有關該電池的說法正確的是( )

A. 反應CH4+H2O![]() 3H2+CO,每消耗1 molCH4轉移12 mol電子
3H2+CO,每消耗1 molCH4轉移12 mol電子
B. 電極B上發生的電極反應:O2+2CO2+4e-=2CO32-
C. 電池工作時,CO32-向電極B移動
D. 電極A上H2參與的電極反應:H2+2OH--2e-=2H2O
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com