
科目: 來源: 題型:
【題目】有機物Y(乙酰氧基胡椒酚乙酸酯)具有抗氧化、抗腫瘤作用,可由化合物X在一定條件下合成,下列說法錯誤的是
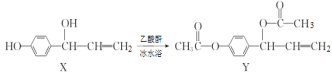
A.X轉化成Y為取代反應
B.X、Y分子中含有的手性碳原子數不相同
C.1molX與溴水充分反應,最多消耗Br2的物質的量為3mol
D.1molY與NaOH溶液充分反應,最多消耗NaOH的物質的量為3mol
查看答案和解析>>
科目: 來源: 題型:
【題目】不能用勒夏特列原理解釋的是( )
A.H2、I2(g)混合氣體加壓后顏色變深B.過量空氣有利于SO2轉化為SO3
C.向氯水中加石灰石可提高次氯酸的濃度D.光照新制氯水,氯水顏色變淺
查看答案和解析>>
科目: 來源: 題型:
【題目】鉬(Mo)是一種重要的過渡金屬元素,在電子行業有可能取代石墨烯,其化合物鉬酸鈉晶體(Na2MoO42H2O)可制造阻燃劑和無公害型冷水系統的金屬抑制劑。由鉬精礦(主要成分MoS2,含有少量不反應雜質)制備鉬及鉬酸鈉晶體的工藝流程如下:

(1)焙燒時,下列措施有利于使鉬精礦充分反應的是________(填序號)。
a 增大鉬精礦的量 b 將礦石粉碎 c 采用逆流原理混合
(2)操作1的名稱是______,“堿浸”過程中反應的離子方程式為________。
(3)經“蒸發結晶”過程可得到鉬酸鈉晶體的粗品,要得到純凈的鉬酸鈉晶體,需要進行的操作2名稱是_________。
(4)Mo元素有+4、+6兩種價態,鉬精礦中存在非整比晶體MoS2.7,則MoS2.7中Mo4+所占Mo元素的物質的量分數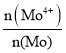 為__________。
為__________。
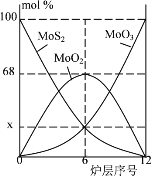
(5)焙燒鉬精礦所用的裝置是多層焙燒爐,如圖為各爐層固體物料的物質的量的百分組成。圖像中縱坐標x =_____。
(6)在實際生產中會有少量SO42-生成,用固體Ba(OH)2除去。在除SO42-前測定堿浸液中c(MoO42-)=0.80mol·L-1, c(SO42-)=0.04mol·L-1,當BaMoO4開始沉淀時,SO42-的去除率為94.5%,則Ksp(BaMoO4)=_________。[ Ksp(BaSO4)= 1.1×10-10,溶液體積變化、溫度變化可忽略。]
查看答案和解析>>
科目: 來源: 題型:
【題目】一定條件下,對于可逆反應N2(g)+3H2(g)![]() 2NH3(g),若N2、H2、NH3起始濃度分別為c1、c2、c3(均不為零),到達平衡時,N2、H2、NH3的濃度分別為0.1mol·L-1、0.3 mol·L-1、0.08mol·L-1,則下列判斷正確的是( )
2NH3(g),若N2、H2、NH3起始濃度分別為c1、c2、c3(均不為零),到達平衡時,N2、H2、NH3的濃度分別為0.1mol·L-1、0.3 mol·L-1、0.08mol·L-1,則下列判斷正確的是( )
A.c1:c2=3:1
B.平衡時,H2和NH3的生成速率之比為2:3
C.N2和H2的轉化率不相等
D.c1的取值范圍為0mol·L-1<c1<0.14mol·L-1
查看答案和解析>>
科目: 來源: 題型:
【題目】下列有關敘述正確的是( )

A. 如上圖所示是測定中和熱的簡易裝置,大小兩燒杯間填滿碎泡沫塑料的作用是固定小燒杯
B. 若用50 mL 0.55 mol·L-1的氫氧化鈉溶液,分別與50 mL 0.50 mol·L-1的鹽酸和50 mL0.50 mol·L-1的硫酸充分反應,兩反應測定的中和熱不相等
C. 實驗時需要記錄初始溫度T1和最高溫度T2
D. 做一次實驗根據公式即可得出中和反應的反應熱
查看答案和解析>>
科目: 來源: 題型:
【題目】藥物他莫肯芬(Tamoxifen)的一種合成路線如圖所示:

已知:![]() +HBr
+HBr![]() +RBr
+RBr

回答下列問題。
(1)A+B→C的反應類型為__;C中官能團有醚鍵、__(填名稱)。
(2)CH3CH2I的名稱為__。
(3)反應D→E的化學方程式為__。
(4)Tamoxifen的結構簡式為__。
(5)X是C的同分異構體。X在酸性條件下水解,生成2種核磁共振氫譜都顯示4組峰的芳香族化合物,其中一種遇FeCl3溶液顯紫色。X的結構簡式為__、__(寫2種)。
(6)設計用 和CH3I為原料(無機試劑任選)制備
和CH3I為原料(無機試劑任選)制備 的合成路線:__。
的合成路線:__。
查看答案和解析>>
科目: 來源: 題型:
【題目】苯胺![]() 是重要的化工原料。某興趣小組在實驗室里進行苯胺的相關實驗。
是重要的化工原料。某興趣小組在實驗室里進行苯胺的相關實驗。
已知:①![]() 和NH3相似,與鹽酸反應生成易溶于水的鹽
和NH3相似,與鹽酸反應生成易溶于水的鹽![]()
②用硝基苯制取苯胺的反應原理: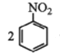 +3Sn+12HCl
+3Sn+12HCl![]()
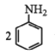 +3SnCl4+4H2O
+3SnCl4+4H2O
③有關物質的部分物理性質見下表:
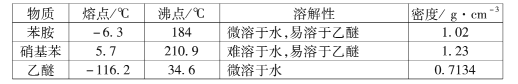
I.比較苯胺與氨氣的性質
(1)將分別蘸有濃氨水和濃鹽酸的玻璃棒靠近,產生白煙,反應的化學方程式為____;用苯胺代替濃氨水重復上述實驗,卻觀察不到白煙,原因是____。
Ⅱ.制備苯胺
往圖1所示裝置(夾持裝置略,下同)的冷凝管口分批加入20mL濃鹽酸(過量),置于熱水浴中回流20min,使硝基苯充分還原;冷卻后,往三頸燒瓶中滴入一定量50% NaOH溶液,至溶液呈堿性。

(2)冷凝管的進水口是____(填“a”或“b”);
(3)滴加NaOH溶液的主要目的是析出苯胺,反應的離子方程式為____。
Ⅲ.提取苯胺
i.取出圖1所示裝置中的三頸燒瓶,改裝為圖2所示裝置。加熱裝置A產生水蒸氣,燒瓶C中收集到苯胺與水的混合物;分離混合物得到粗苯胺和水溶液。

ii.往所得水溶液中加入氯化鈉固體,使溶液達到飽和狀態,再用乙醚萃取,得到乙醚萃取液。
iii.合并粗苯胺和乙醚萃取液,用NaOH固體干燥,蒸餾后得到苯胺2.79g。
(4)裝置B無需用到溫度計,理由是____。
(5)操作i中,為了分離混合物,取出燒瓶C前,應先打開止水夾d,再停止加熱,理由是____。
(6)該實驗中苯胺的產率為____。
(7)欲在不加熱條件下除去苯胺中的少量硝基苯雜質,簡述實驗方案:____。
查看答案和解析>>
科目: 來源: 題型:
【題目】硫氰酸鹽在化學工業中應用廣泛。
(1)組成硫氰酸根(SCN -)的三種元素的部分性質見下表:
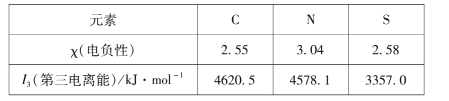
①硫氰酸根中碳元素的化合價為____。
②碳元素的I1、I2均比氮小。但I3卻比氮高,其原因是____。
(2)晶體場理論認為,基態離子的d軌道存在未成對電子時,d電子發生d-d躍遷是金屬陽離子在水溶液中顯色的主要原因。下列硫氰酸鹽的水溶液有顏色的是____(填標號)。
A KSCN B Fe(SCN)3 C Ni(SCN)2 D Zn(SCN)2
(3)NH4SCN廣泛應用于醫藥、印染等行業,隔絕空氣加熱后可分解生成NH3、CS2、H2S、(CN)2及N2。
①SCN-可能具有[S-C≡N]-和____(填結構式)兩種結構,中心原子碳的軌道雜化方式均為____。
②(CN)2熔沸點高于N2的原因是____。
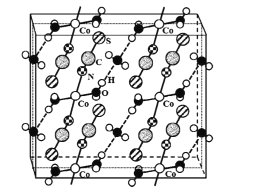
(4)硫氰酸鈷可用于毒品檢驗。其水合物晶體的晶胞結構如下圖所示(所有原子都不在晶胞的頂點或棱上)。
①晶體中微粒間作用力有____(填標號)。
A 金屬鍵 B 氫鍵 C 非極性鍵 D 極性鍵 E 配位鍵
②晶體的化學式為____。
③硫氰酸鈷晶體屬于正交晶系,晶胞參數分別為a nm、b nm.c nm,α=β=γ=90°。晶體的摩爾質量為M g·mol-1。則晶體密度=____g·cm-3(列計算式)。
查看答案和解析>>
科目: 來源: 題型:
【題目】CO2催化加氫制甲醇,是極具前景的溫室氣體資源化研究領域。在某CO催化加氫制甲醇的反應體系中,發生的主要反應有:
i.CO2(g)+3H2(g) ![]() CH3OH(g)+H2O(g) △H1=-49.4kJ·mol-1
CH3OH(g)+H2O(g) △H1=-49.4kJ·mol-1
ⅱ.CO2(g)+H2(g) ![]() CO(g)+H2O(g) △H2=+41.2kJ·mol-1
CO(g)+H2O(g) △H2=+41.2kJ·mol-1
ⅲ.CO(g)+2H2(g) ![]() CH3OH(g) △H3
CH3OH(g) △H3
(1)△H3________ kJ·mol-1
(2)5MPa時,往某密閉容器中按投料比n(H2):n(CO2)=3:1充入H2和CO2。反應達到平衡時,測得各組分的物質的量分數隨溫度變化的曲線如圖所示。
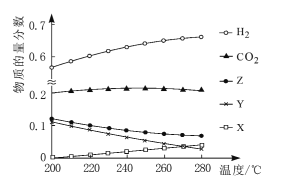
①體系中CO2的物質的量分數受溫度的影響不大,原因是____。
②250℃時,反應ii的平衡常數____1(填“>”“<”或“=”)。
③下列措施中,無法提高甲醇產率的是____(填標號)。
A 加入適量CO B 增大壓強 C 循環利用原料氣 D 升高溫度
④如圖中X、Y分別代表____(填化學式)。
(3)反應i可能的反應歷程如下圖所示。
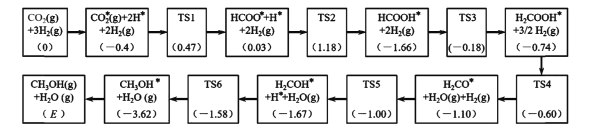
注:方框內包含微粒種類及數目、微粒的相對總能量(括號里的數字或字母,單位:eV)。其中,TS表示過渡態、*表示吸附在催化劑上的微粒。
①反應歷程中,生成甲醇的決速步驟的反應方程式為____。
②相對總能量E=____(計算結果保留2位小數)。(已知:leV=1.6×10-22kJ)
(4)用電解法也可實現CO2加氫制甲醇(稀硫酸作電解質溶液)。電解時,往電解池的____極通入氫氣,陰極上的電極反應為____。
查看答案和解析>>
科目: 來源: 題型:
【題目】有反應4HCl(g)+O2(g)═2Cl2(g)+2H2O(g),已知2 mol O2被還原時,放出a kJ的熱量,且知斷開1 mol O=O鍵需要吸收b kJ的熱量,斷開1 mol Cl—Cl鍵需要吸收c kJ的熱量。則斷開1 mol H—O鍵比斷開1 mol H—Cl鍵所需能量高
A. (b-a-2c)/4kJB. (a+2b-4c)/8kJC. (a+b-2c)/4kJD. (2b-a-4c)/8kJ
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com