
【題目】實驗室里需要純凈的氯化鈉晶體,但現在只有混有硫酸鈉、碳酸氫銨的氯化鈉。某學生設計了如下方案:

![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
請回答下列問題:
(1)操作①加熱的目的是________________,
(2)操作②除用BaCl2溶液外,還可用____________替代。
(3)操作②,判斷SO42-已除盡的方法是________________________。
(4)操作③的目的是____________,不先過濾后再加Na2CO3溶液的理由是____________。
(5)操作④的名稱是______________,應在________(填儀器名稱)中進行。
【答案】加熱分解除去NH4HCO3 Ba(OH)2溶液 取上層清液加入BaCl2溶液,若無沉淀說明SO42-已除盡 除去過量的Ba2+ 減少一次過濾操作 蒸發結晶 蒸發皿
【解析】
(1)化合物中碳酸氫銨受熱分解分析;
(2)操作②是沉淀硫酸根離子的作用,也可以加入氫氧化鋇溶液,注意不能引入新的雜質;
(3)判斷SO42-已除盡選擇的試劑是BaCl2溶液;
(4)操作③是除去過量的鋇離子;
(5)操作④是蒸發氯化鈉溶液得到氯化鈉晶體,溶液蒸發在蒸發皿中加熱進行。
(1)操作①加熱的目的是利用碳酸氫銨受熱分解生成氨氣、二氧化碳、水蒸氣除去碳酸氫銨固體;故答案為:加熱分解除去NH4HCO3;
(2)操作②是完全沉淀硫酸根離子,原則是加入的試劑不能引入新的雜質,或最后易于除去,除了用BaCl2溶液外,也可以用Ba(OH)2溶液;
(3)操作②,判斷SO42-已除盡的方法是取上層清液加入BaCl2溶液,若無沉淀說明SO42-已除盡;
(4)操作③是加入碳酸鈉溶液,目的是除去過量的鋇離子,避免引入鋇離子雜質;所以加入碳酸鈉的目的是除去過量的Ba2+;不先過濾后再加Na2CO3溶液的理由是減少一次過濾操作;
(5)操作④將溶液蒸發結晶得到溶質晶體;操作④是將氯化鈉溶液蒸發結晶得到氯化鈉晶體,溶液蒸發應在蒸發皿中加熱進行。


科目:高中化學 來源: 題型:
【題目】1體積pH=2.5的鹽酸與10體積某一元強堿溶液恰好完全反應,則該堿溶液的pH等于( )
A. 9.0 B. 9.5 C. 10.5 D. 11.0
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】元素X 位于第四周期,其基態原子的內層軌道全部排滿電子,且最外層電子數為2。元素Y基態原子的3p 軌道上有4個電子。元素Z 的原子最外層電子數是其內層的3倍。

(1)X與Y所形成化合物晶體的晶胞如右圖所示。
①在1個晶胞中,X離子的數目為 。
②該化合物的化學式為 。
(2)在Y的氫化物(H2Y)分子中,Y原子軌道的雜化類型是 。
(3)Z的氫化物(H2Z)在乙醇中的溶解度大于H2Y,其原因是 。
(4)Y 與Z 可形成YZ42-
①YZ42-的空間構型為 。
②寫出一種與YZ42-互為等電子體的分子的化學式: 。
(5)X的氯化物與氨水反應可形成配合物[X(NH3)4]Cl2,1mol該配合物中含有σ鍵的數目為 。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】硫酸四氨合銅(Ⅱ)是一種重要的染料及農藥中間體。a、b、c、d、e是硫酸四氨合銅(Ⅱ)中原子序數依次增大的五種元素。
(1)該配合物中,配體的電子式為________;五種元素中電負性最大的是________ (填元素名稱),基態b原子的價層電子排布圖為______________________。
(2)a和其它4種元素形成的二元共價化合物中,分子中既含有極性共價鍵、又含有非極性共價鍵的化合物是_______________、______________(填化學式,寫出兩種)。
(3)基態e原子中,核外占據最高能層的電子的電子云輪廓圖形狀為________形;c、d元素形成的分子dc3中心原子雜化軌道類型為________。
(4)元素d可以形成兩種常見含氧酸,其通式為(HO)mdOn,請根據結構與性質的關系解釋該兩種含氧酸酸性強弱的原因是_____________________________。
(5)與銅同周期的鋅為六方最密堆積晶體,晶胞如圖。鋅的原子半徑為r,在正四面體A1A2A4B中,點A1到A2A4B平面的距離為h,NA是阿伏加德羅常數的值。鋅原子的配位數為________,晶胞參數(長、寬、高)依次為________,晶體密度的計算式為__________。

查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】已知:乙二酸晶體熔點101.5℃;乙二酸晶體加熱分解的方程式為:H2C2O42H2O![]() 3H2O + CO2↑+ CO↑。現利用下列裝置驗證反應產物中含有CO2和CO(裝置不能重復使用)。請回答下列問題:
3H2O + CO2↑+ CO↑。現利用下列裝置驗證反應產物中含有CO2和CO(裝置不能重復使用)。請回答下列問題:

(1)檢驗裝置A氣密性的方法是________________________________________________
(2)A裝置是否有誤_____________(填“是”或“否”),原因為_______________________
(3)按氣流方向連接各儀器,用數字表示接口的連接順序:①→_________________________;
(4)該套裝置有明顯缺陷,請予以更正________________________________________________
(5)證明CO存在的實驗現象是_________________________________________________;
(6)根據題給的數據,假設反應產生的氣體全部排出,并與吸收液充分反應(提示:B、C中澄清石灰水均先變渾濁,后又變澄清),最終D中生成了兩種物質,則這兩種生成物的化學式及對應的物質的量分別是①_______________,②_______________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列圖示與對應的敘述相符的是
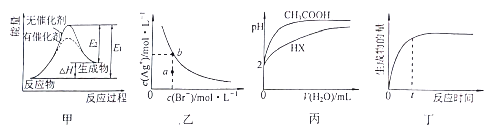
A. 圖甲表示放熱反應在有無催化劑的情況下反應過程中的能量變化
B. 圖乙表示一定溫度下,溴化銀在水中的沉淀溶解平衡曲線,其中a點代表的是不飽和溶液,b點代表的是飽和溶液
C. 圖丙表示25℃時,分別加水稀釋體積均為100mL、pH=2的一元酸CH3COOH溶液和HX溶液,則25℃時HX的電離平衡常數大于CH3COOH
D. 圖丁表示某可逆反應生成物的量隨反應時間變化的曲線,由圖知t時反應物轉化率最大
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列實驗操作能達到目的是
A. 用PH試紙測定次氯酸溶液的pH
B. 將FeCl3溶液加熱蒸干并灼燒獲得Fe2O3固體
C. 向明礬溶液中加入一定量NaOH,制備Al(OH)3膠體
D. 室溫下,測得pH=5的NaHSO4溶液與pH=9的NaHCO3溶液中水的電離程度相等
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】氨基羧酸鹽在工業、農業、生活中都有著十分廣泛的應用。氨基甲酸銨(NH2COONH4)可用做肥料、滅火劑、洗滌劑等,甘氨酸亞鐵[(NH2CH2COO)2Fe]可用作補鐵劑等。
已知:i. 氨基甲酸銨:白色固體,易分解,易水解;甘氨酸亞鐵:易溶于水,難溶于乙醇。
ii. 甘氨酸:易溶于水,微溶于乙醇,兩性化合物。
iii. 檸檬酸:易溶于水和乙醇,有較強酸性和還原性。
實驗室制備方法如下:
I.制備氨基甲酸銨:反應的化學方程式為:2NH3(g)+CO2(g) ![]() NH2COONH4(g) △H<0
NH2COONH4(g) △H<0
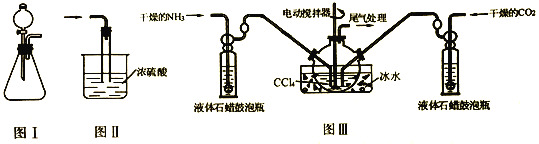
(1)圖Ⅰ裝置制備NH3,則所選試劑為_________________
(2)圖Ⅲ裝置制備氨基甲酸銨,把氨氣和二氧化碳通入四氯化碳中,不斷攪拌混合,生成的氨基甲酸銨小晶體懸浮在四氯化碳中。(注:四氯化碳與液體石蠟均為惰性介質。)
①從反應后的混合物中分離出產品的實驗操作是_______________(填操作名稱)
②圖Ⅱ裝置進行尾氣處理,則雙通玻璃管的作用________________
③液體石蠟鼓泡瓶的作用是________________
④發生器用冰水冷卻的原因是________________
II.制備(NH2CH2COO)2Fe:裝置如圖(夾持和加熱儀器已省略), 用CO2氣體將裝置中空氣排凈,加入藥品后,滴入檸檬酸并加熱。反應結束后過濾,將濾液蒸發濃縮,加入乙醇,過濾、干燥得到產品。
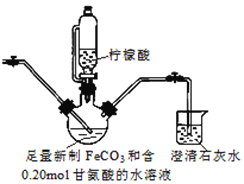
(3)燒杯中澄清石灰水的作用是_______________。
(4)檸檬酸可調節pH,體系pH與產率的關系如下表:
實驗 | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 |
體系pH | 4.0 | 4.5 | 5.0 | 5.5 | 6.0 | 6.5 | 7.0 | 7.5 |
產率/% | 65.74 | 74.96 | 78.78 | 83.13 | 85.57 | 72.98 | 62.31 | 56.68 |
分析pH過低使產率下降的原因是___________;檸檬酸的作用還有_____(填序號)。
a.作反應終點指示劑 b.防止二價鐵被氧化 c. 作催化劑 d. 促進FeCO3溶解
(5)乙醇的作用是________________。
(6)若產品的質量為m g,則產率為________________。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com