
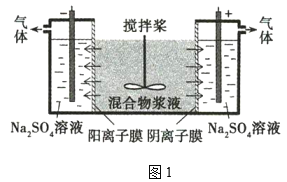
【題目】某混合物漿液含Al(OH)3、MnO2和少量Na2Cr2O4。考慮到膠體的吸附作用使Na2Cr2O4不易完全被水浸出,某研究小組利用設計的電解分離裝置(如圖1),使漿液分離成固體混合物和含鉻元素溶液,并回收利用。
固體混合物的分離和利用的流程圖如圖2所示(流程圖中的部分分離操作和反應條件未標明):
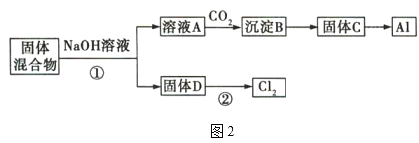
(1)反應①所加試劑NaOH的電子式為___,B→C的反應條件為___,C→Al的制備方法稱為___。
(2)該小組探究反應②發生的條件。D與濃鹽酸混合,不加熱,無變化;加熱有Cl2生成,當反應停止后,固體有剩余,此時滴加硫酸,又產生Cl2。由此判斷影響該反應有效進行的因素有___(填序號)。
a.溫度 b.Cl-的濃度 c.溶液的酸度
【答案】![]() 加熱(或煅燒) 電解法 ac
加熱(或煅燒) 電解法 ac
【解析】
在圖1中,與電源負極相連的是電解池的陰極,發生反應為2H2O+2e-=2OH-+H2↑,混合物漿液中Na+向陰極移動;與電源正極相連的是電解池的陽極,發生反應為2H2O-4e-=O2↑+4H+,混合物漿液中的Cr2O42-向陽極移動。此時混合物漿液中的物質為Al(OH)3、MnO2。在圖2中,固體混合物中加入NaOH溶液,Al(OH)3溶解生成NaAlO2溶液,此為溶液A的主要成分,MnO2為固體D的主要成分。溶液A中通入CO2,與NaAlO2發生反應:NaAlO2+CO2+2H2O=Al(OH)3↓+NaHCO3,沉淀B的主要成分為Al(OH)3,受熱分解生成Al2O3,成為固體C的主要成分,熔融電解可獲得Al。固體D中的MnO2與濃鹽酸在加熱條件下反應,可制得Cl2。
(1)NaOH為離子化合物,由Na+和OH-構成,電子式為![]() 。根據圖2中的轉化關系,向溶液A中通入CO2,發生反應:NaAlO2+CO2+2H2O=Al(OH)3↓+NaHCO3,沉淀B為Al(OH)3,固體C為Al2O3,B→C的反應條件為加熱或煅燒,Al2O3→Al的制備方法為氧化鋁的熔融電解法。答案為:
。根據圖2中的轉化關系,向溶液A中通入CO2,發生反應:NaAlO2+CO2+2H2O=Al(OH)3↓+NaHCO3,沉淀B為Al(OH)3,固體C為Al2O3,B→C的反應條件為加熱或煅燒,Al2O3→Al的制備方法為氧化鋁的熔融電解法。答案為:![]() ;加熱或煅燒;電解法;
;加熱或煅燒;電解法;
(2)根據“D與濃鹽酸混合,不加熱,無變化;加熱有Cl2生成”知,溫度對反應有影響;滴加硫酸,引入H+,又產生Cl2,說明溶液的酸度對反應有影響。答案為:ac。


 閱讀快車系列答案
閱讀快車系列答案科目:高中化學 來源: 題型:
【題目】(1)下列物質中,既含離子鍵又含共價鍵的化合物是_________;同時存在σ鍵和π鍵的分子是_________,含有極性鍵的非極性分子是_________。
A.N2 B.C2H6 C.CaCl2 D.NH4Cl
(2)用“>”或“<”填空:
晶格能:Na2O_______KCl 酸性:H2SO4_______HClO4 離子半徑:Al3+_______F-
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】實驗室里從海藻中提取碘的流程如下圖:
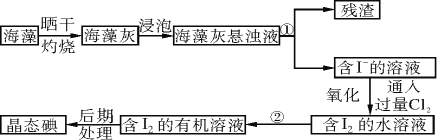
(1)指出制取碘的過程中有關的實驗操作名稱(或儀器):
①操作名稱________________,②儀器________________。
(2)提取碘的過程中,可供選擇的有機溶劑是________(填字母序號)。
a.甲苯、酒精 b.四氯化碳、苯
c.汽油、乙酸 d.汽油、甘油
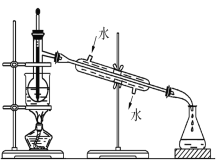
(3)含碘的有機物溶液中提取碘和回收有機溶劑,還需要經過蒸餾,觀察下列實驗裝置指出其錯誤之處,并指出正確操作。____________________________________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】圖1是銅鋅原電池示意圖。圖2中,x軸表示實驗時流入正極的電子的物質的量,y軸表示( )
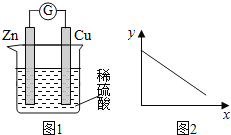
A. 銅棒的質量 B. c(Zn2+) C. c(H+) D. c(SO42-) -
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】常溫下,向1L pH=10的NaOH溶液中持續通入CO2。通入的CO2的體積(V)與溶液中水電離出的OH-離子濃度(![]() )的關系如圖所示。下列敘述正確的是
)的關系如圖所示。下列敘述正確的是
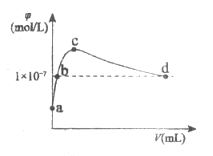
A.a點溶液:水電離的c(OH-)=1×10-4mol/L
B.b點溶液:c(OH-)=c(H+)
C.c點溶液:c(Na+)=2c(CO32-)+2c(HCO3-)+2c(H2CO3)
D.d點溶液:c(Na+)>2c(CO32-)+c(HCO3-)
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】已知在 1標準大氣壓、25℃ 下,1mol 氣態 AB 分子生成氣態 A 原子和 B 原子的過程中所吸收的能量稱為AB間共價鍵的鍵能,已知水分子的能量變化關系圖如下:

下列說法正確的是
A.△H1<0,且△H3 <△H4
B.△H4 是 O2的鍵能
C.△H5 =△H1+△H2+△H3+△H4
D.△H3+△H4 >△H5
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】設NA表示阿伏加德羅常數的值。下列說法正確的是( )
A.14g聚丙烯中含C-H鍵總數目為2NA
B.常溫下,pH=13的NaOH溶液中含有的OH-數目為0.1NA
C.100mL12mol·L-1濃硝酸與過量Cu反應轉移電子的數目為0.6NA
D.電解精煉銅時,若陽極質量減少64g,則陰極得到電子的數目為2NA
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】反應N2O4(g) ![]() 2NO2(g) ΔH=+57kJ·mol-1,在溫度為T1、T2時,平衡體系中NO2的體積分數隨壓強變化曲線如圖所示。下列說法不正確的是
2NO2(g) ΔH=+57kJ·mol-1,在溫度為T1、T2時,平衡體系中NO2的體積分數隨壓強變化曲線如圖所示。下列說法不正確的是
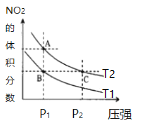
A.A點的反應速率小于C點的反應速率
B.A、C兩點氣體的顏色:A淺,C深
C.由狀態B到狀態A,可以用降溫的方法
D.A、C兩點氣體的平均相對分子質量:A<C
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列中心原子的雜化軌道類型和分子幾何構型不正確的是
A. CCl4中C原子sp3雜化,為正四面體形
B. H2S分子中,S為sp2雜化,為直線形
C. CS2中C原子sp雜化,為直線形
D. BF3中B原子sp2雜化,為平面三角形
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com