
【題目】X和Y是原子序數大于4的短周期元素, ![]() 、
、![]() 兩種離子的核外電子排布相同。下列說法中正確的是 ( )
兩種離子的核外電子排布相同。下列說法中正確的是 ( )
A. X的原子半徑比Y的原子半徑小 B. X和Y的核電荷數之差為m -- n
C. Y原子核內所含質子數比X多 D. ![]() 半徑比
半徑比![]() 小
小
【答案】D
【解析】X、Y是原子序數大于4的兩種主族元素,Xm+和Yn-兩種離子的核外電子排布相同,則二者核外電子數相等,X處于Y的下一周期,且X為金屬元素,Y為非金屬元素,則A.X處于Y的下一周期,且X為金屬元素,Y為非金屬元素,X的原子半徑比Y的原子半徑大,A錯誤;B.令X、Y的原子序數分別為a、b,離子核外電子排布相同,則a-m=b+n,故a-b=m+n,即X和Y的核電荷數之差為m+n,B錯誤;C.Xm+和Yn-兩種離子的核外電子排布相同,X處于Y的下一周期,原子序數大小為:X>Y,所以Y原子核內所含質子數比X少,C錯誤;D.核外電子排布相同時離子半徑隨原子序數的增大而減小,則Xm+半徑比Yn-小,D正確,答案選D。


 互動課堂系列答案
互動課堂系列答案 激活思維智能訓練課時導學練系列答案
激活思維智能訓練課時導學練系列答案科目:高中化學 來源: 題型:
【題目】用足量的一氧化碳還原4.64 g某金屬氧化物,把生成的二氧化碳全部通入到過量的澄清石灰水中,得到的沉淀干燥后質量為8.0 g,則此金屬氧化物是下列中的( )
A. 氧化銅 B. 氧化鐵 C. 四氧化三鐵 D. 二氧化錳
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】已知元素周期表中共有18縱行,下圖中實線表示元素周期表的邊界。按電子排布,可把周期表里的元素劃分為下列幾個區:s區、p區、d區、ds區等。除ds區外,其他區的名稱來自構造原理最后填入的電子的能級符號。
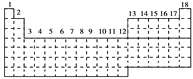
(1)請在圖中用實線畫出s區、p區、d區、ds區的邊界線,并分別用陰影![]() 和
和![]() 表示d區和ds區____。
表示d區和ds區____。
(2)有的同學受這種劃分的啟發,認為d區內6、7縱行的部分元素可以排在另一區,你認為應排在__________區。
(3)在元素周期表中4s軌道半充滿的元素為__________(填元素符號)
(4)請利用電子排布的相關知識解釋Fe3+比Fe2+穩定的原因______________________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】A~H等8種物質存在如下轉化關系(反應條件,部分產物未標出)。已知:A是正鹽,B是能使品紅溶液退色的氣體,G是紅棕色氣體。按要求回答問題:
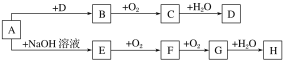
(1)寫出下列物質的化學式:A____________,B____________。
(2)寫出下列反應的化學方程式:
E→F___________________G→H__________________;D的溶液與木炭反應的化學方程式: ________________。
(3)檢驗某溶液中是否含D中陰離子的方法是_________________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】現有0.27kg質量分數為10%的CuCl2溶液。試計算:
(1)溶液中CuCl2的物質的量_______;
(2)溶液中Cu2+和Cl-的物質的量_______。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】二氧化硅又稱硅石,是制備硅及其含硅化合物的重要原料。部分轉化過程如圖所示,下列說法正確的是

A. SiO2既能與HF反應,又能與NaOH反應,屬于兩性氧化物
B. 因為在高溫條件下二氧化硅與碳酸鈉反應放出二氧化碳,所以H2SiO3的酸性比H2CO3強
C. SiO2在高溫條件下能與過量的碳反應生成SiC,體現了二氧化硅的氧化性
D. 除Si的制取過程中涉及的反應外,圖中所示其他反應都是非氧化還原反應
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列關于有機物的說法錯誤的是
A. CH4是沼氣、天然氣和煤礦坑道氣的主要成分
B. 乙烯和丙烯可通過石油裂解的方法大量獲得
C. 乙醇、乙酸和乙酸乙酯能用飽和Na2CO3溶液鑒別
D. 苯不能使KMnO4溶液退色,因此苯不能發生氧化反應
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列各組關于強電解質、弱電解質、非電解質的歸類,完全正確的是
選項 | A | B | C | D |
強電解質 | Fe | NaCl | CaCO3 | HNO3 |
弱電解質 | CH3COOH | NH3 | H3PO4 | Fe(OH)3 |
非電解質 | 蔗糖 | BaSO4 | 酒精 | H2O |
A.AB.BC.CD.D
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com