
【題目】金剛石、石墨烯和![]() 都是碳的同素異形體,其結構示意圖如圖:
都是碳的同素異形體,其結構示意圖如圖:

(1)金剛石屬立方晶系,每個晶胞所包括的C原子個數為_____________。
(2)金剛石、石墨烯、木炭和![]() 都是由碳元素組成的單質。下列關于碳的單質的敘述正確的是_______(填序號)。
都是由碳元素組成的單質。下列關于碳的單質的敘述正確的是_______(填序號)。
A.都是黑色固體
B.碳原子的排列方式不相同
C.這四種物質都很軟,可作潤滑劑
D.在氧氣中充分燃燒時都生成二氧化碳
E.一定條件下,木炭轉化成金剛石是物理變化
(3)金剛石質硬但脆,金剛石能被砸碎的原因是_______________________________。
(4)觀察計算一個![]() 分子結構中含有____________個正五邊形和_________個正六邊形。
分子結構中含有____________個正五邊形和_________個正六邊形。
(5)石墨烯是單層的石墨,它是世界上已知的最薄、最堅硬的新型材料,有良好的導電性,具有很好的應用前景。石墨烯中碳原子的雜化軌道類型為___________;碳碳鍵的鍵角是___________。
(6)碳化硅(![]() )的結構與金剛石類似,設碳化硅的密度為
)的結構與金剛石類似,設碳化硅的密度為![]() ,碳化硅晶體內碳硅鍵的鍵長為________________
,碳化硅晶體內碳硅鍵的鍵長為________________![]() (用NA表示阿伏加德羅常數的值,列表達式即可)。
(用NA表示阿伏加德羅常數的值,列表達式即可)。
【答案】8 BD 共價鍵具有方向性,當受到大的外力作用會發生原子間錯位而斷裂 12 20 ![]() 雜化 120°
雜化 120° 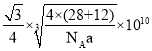
【解析】
(1)根據晶胞結構來數即可,頂點上的原子按![]() 來計算,面心上的原子按
來計算,面心上的原子按![]() 來計算,晶體內的原子按1個來計算;
來計算,晶體內的原子按1個來計算;
(2)對四種同素異形體進行分析即可,注意同素異形體為不同的物質,因此之間的轉化屬于化學變化;
(3)金剛石是由碳原子通過共價鍵形成的原子晶體,因此在討論其物理性質時應從共價鍵的角度來分析;
(4)可以根據假設法來進行推算(具體步驟見詳解部分);
(5)觀察石墨烯的結構不難發現,每個碳原子只與另外3個碳原子成鍵,而碳原子理論上應該形成4個共價鍵,因此說明必有一個鍵是雙鍵;
(6)一個金剛石晶胞內有8個碳原子,因此一個碳化硅晶胞內有4個![]() ,再列出密度的表達式來計算即可。
,再列出密度的表達式來計算即可。
(1)頂點![]() 面心
面心![]() 晶體內
晶體內![]() ;
;
(2)A.金剛石即鉆石,明顯不是黑色固體,A項錯誤;
B.正因為碳原子的排列方式不同,形成了不同同素異形體,B項正確;
C.金剛石的硬度極大,C項錯誤;
D.四種物質都可以被氧氣充分氧化,變為二氧化碳,D項正確;
E.木炭和金剛石是兩種物質,既然生成了新物質肯定是化學變化,E項錯誤;
答案選BD;
(3)共價鍵具有方向性,當受到大的外力作用會發生原子間錯位而斷裂;
(4)
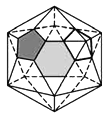
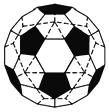
切掉的每個頂點由一個正五邊形面代替,每個正五邊形有5條邊,所以,一共新增加![]() 條棱。原來的正二十面體有30條棱(從圖中左圖很容易數出來)仍在,所以,
條棱。原來的正二十面體有30條棱(從圖中左圖很容易數出來)仍在,所以,![]() 就一共有
就一共有![]() 條棱。最后說面數的變化,原正二十面體的20個面還在(雖然形狀由正三角形變為正六邊形),又切出12個正五邊形面,所以一共是
條棱。最后說面數的變化,原正二十面體的20個面還在(雖然形狀由正三角形變為正六邊形),又切出12個正五邊形面,所以一共是![]() 個面;
個面;
(5)石墨烯為片層結構,雜化類型為![]() 雜化,碳碳原子之間形成六元環,鍵角是120°;
雜化,碳碳原子之間形成六元環,鍵角是120°;
(6)根據密度公式![]() 先求出晶胞的體積,化簡后進一步求出邊長為
先求出晶胞的體積,化簡后進一步求出邊長為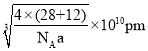 ,根據晶胞結構不難看出碳硅鍵為體對角線的
,根據晶胞結構不難看出碳硅鍵為體對角線的![]() ,因此給邊長乘以
,因此給邊長乘以![]() 即可。
即可。


科目:高中化學 來源: 題型:
【題目】氮氧化物(NOx)造成酸雨、光化學煙霧、臭氧層破壞等危害,不僅破壞自然生態環境,而且嚴重危害人類健康。采用合適的還原劑能夠實現煙氣的高效脫硝。
(1)活性炭還原脫硝可防止氮氧化物污染,已知:
①N2(g)+O2(g)═2NO(g) △H1=+180.5kJmol-1
②2C(s)+O2(g)═2CO(g) △H2=-221.0kJmol-1
③2CO(g)+O2(g)═2CO2(g) △H3=-556.0kJmol-1
則反應C(s)+2NO(g)![]() N2(g)+CO2(g)△H=__kJmol-1
N2(g)+CO2(g)△H=__kJmol-1
(2)用活性炭對NO進行還原,采用相同質量不同粒徑的同種催化劑M和N,測量相同時間內煙氣的脫氮率,結果如圖所示。
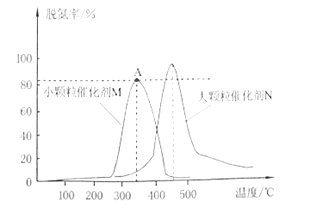
①在M、N兩種不同粒徑催化劑作用下,出現M和N兩條不同的脫氮率與溫度的變化曲線的原因是___。
②判斷M曲線上最高點A點對應的脫氮率__(填“是“或“不是”)該溫度下的平衡脫氮率。
③25℃下,用NaOH溶液作捕提劑吸收產生的CO2,不僅可以降低碳排放,而且可得到重要的化工產品。某次捕捉后得到pH=12的溶液,已知:25℃下Ka2(H2CO3)=5.6×10-11,試通過計算溶液中c(CO32-):c(HCO3-)=__。
(3)在一恒容密閉容器中,使用某種催化劑對反應NO2(g)+SO2(g)![]() SO3(g)+NO(g)△H<0進行相關實驗探究。改變投料比(n0(SO2):n0(NO2)]進行多組實驗(各次實驗的溫度可能相同,也可能不同),測定SO2的平衡轉化率[α(SO2)]。已知:KR=16,KZ=1,部分實驗結果如圖所示。
SO3(g)+NO(g)△H<0進行相關實驗探究。改變投料比(n0(SO2):n0(NO2)]進行多組實驗(各次實驗的溫度可能相同,也可能不同),測定SO2的平衡轉化率[α(SO2)]。已知:KR=16,KZ=1,部分實驗結果如圖所示。

①如果要將圖中R點的平衡狀態改變為X點的平衡狀態,應采取的措施是__。
②圖中R、X、Y、Z四點對應的實驗溫度分別為TR、TX、TY,TZ通過計算選擇下列選項中兩個溫度相等是__(填標號)。
A.TR和TY B.TR和TZ C.TX和TZ D.TY和TZ
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】已知:C是一種合成樹脂,用于制備塑料和合成纖維,D是一種植物生長調節劑,可用于催熟果實。根據以下化學反應框圖填空:
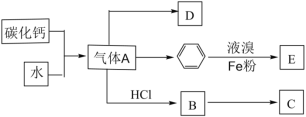
(1)寫出A的電子式_______;C的結構簡式_______;D中碳原子的雜化方式為_______
(2)寫出苯和液溴反應生成E的化學方程式_______;其反應類型是_______;
(3)B中最多有_______個原子共平面
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】氟他胺G是一種可用于治療腫瘤的藥物。實驗室由芳香烴A制備G的合成路線如圖:
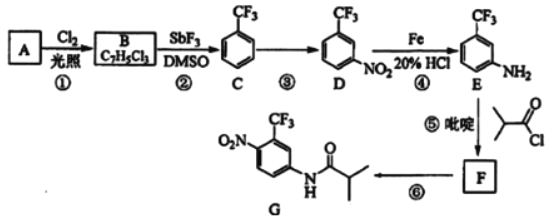
回答下列問題:
(1)A的結構簡式為__。C的化學名稱是__。
(2)③的反應試劑和反應條件分別是__,該反應的類型是__。
(3)⑤的反應方程式為__。吡啶是一種有機堿,其作用是__。
(4)G的分子式為__。
(5)H是G的同分異構體,其苯環上的取代基與G的相同但位置不同,則H可能的結構有__種。
(6)4甲氧基乙酰苯胺(![]() )是重要的精細化工中間體,寫出由苯甲醚(
)是重要的精細化工中間體,寫出由苯甲醚(![]() )制備4甲氧基乙酰苯胺的合成路線__(其他試劑任選)。
)制備4甲氧基乙酰苯胺的合成路線__(其他試劑任選)。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下表中給出了四個實驗裝置和對應的部分實驗現象,其中a、b、c、d為金屬電極,由此可判斷四種金屬的活動性順序是( )
實驗裝置 |
|
|
|
|
部分實驗現象 | a極質量減小 b極質量增加 | b極有氣泡產生 c極無變化 | d極溶解 c極有氣泡產生 | 電流計指示在導線中 電流從a極流向d極 |
A. d>a>b>cB. b>c>d>aC. a>b>c>dD. a>b>d>c
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】在2 L恒容絕熱(不與外界交換能量)容器中進行2A(g) +B(g) =2C(g)+D(s)反應,按下表數據投料,反應10 s后達到平衡狀態,測得體系壓強升高,前10s內v(A)= 0.025 mol/(Ls)。下列說法正確的是

A. 達平衡時,2v正(A)=v逆(B) B. 平衡后,增加D的量,平衡逆向移動
C. 到達平衡時,n(B) =0.5 mol D. 溫度升高,該反應的平衡常數減小
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】亞氯酸鈉(NaClO2)是一種高效的漂白劑和氧化劑,可用于各種纖維和某些食品的漂白。馬蒂遜(Mathieson)法制備亞氯酸鈉的流程如下:

下列說法錯誤的是( )
A.反應①階段,參加反應的NaClO3和SO2的物質的量之比為2:1
B.若反應①通過原電池來實現,則ClO2是正極產物
C.反應②中的H2O2可用NaClO4代替
D.反應②條件下,ClO2的氧化性大于H2O2
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】研究和深度開發CO、CO2的應用具有重要的社會意義。回答下列問題:
I.CO可用于高爐煉鐵,已知:
Fe3O4(s)+4CO(g)=3Fe(s)+4CO2(g) △H1=akJ/mol
3Fe2O3(s)+CO(g)=2Fe3O4(s)+CO2(g) △H2=bkJ/mol
則反應Fe2O3(s)+3CO(g)=2Fe(s)+3CO2(g)的△H=__kJ/mol。
Ⅱ.某溫度下,在容積為2L的密閉容器中投入8molCO2(g)、16molH2(g)發生反應:CO2(g)+H2(g)![]() CO(g)+H2O(g),15min后達到平衡,此時CO2的轉化率為75%。則
CO(g)+H2O(g),15min后達到平衡,此時CO2的轉化率為75%。則
①0~15min內用二氧化碳表示平均反應速率v(CO2)=__,
②計算此條件下該反應的平衡常數K=__。
Ⅲ.捕碳技術是指從空氣中捕獲二氧化碳的各種科學技術的統稱。目前NH3和(NH4)2CO3等物質已經被用作工業捕碳劑。
(1)下列物質中能作為CO2捕獲劑的是__。
A.Na2CO3 B.NaOH C.CH3CH2OH D.NH4Cl
(2)用(NH4)2CO3捕碳的反應:(NH4)2CO3(aq)+H2O(1)+CO2(g)![]() 2NH4HCO3(aq)。為研究溫度對(NH4)2CO3捕獲CO2效率的影響,將一定量的(NH4)2CO3溶液置于密閉容器中,并充人一定量的CO2氣體,保持其它初始實驗條件不變,分別在不同溫度下,經過相同時間測得CO2氣體濃度,得到趨勢圖:
2NH4HCO3(aq)。為研究溫度對(NH4)2CO3捕獲CO2效率的影響,將一定量的(NH4)2CO3溶液置于密閉容器中,并充人一定量的CO2氣體,保持其它初始實驗條件不變,分別在不同溫度下,經過相同時間測得CO2氣體濃度,得到趨勢圖:
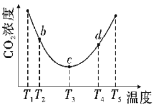
b、c、d三點的平衡常數Kb、Kc、Kd從大到小的順序為__。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】科學家研制的一種使沙漠變綠洲的新技術,即在沙漠中噴灑一定的![]() (聚丙烯酸酯)與水的混合物,使其與沙粒結合,形成既能阻止地下的鹽分上升,又能攔截、蓄積雨水作用。下列對聚丙烯酸酯的敘述中正確的是( )
(聚丙烯酸酯)與水的混合物,使其與沙粒結合,形成既能阻止地下的鹽分上升,又能攔截、蓄積雨水作用。下列對聚丙烯酸酯的敘述中正確的是( )
A.聚丙烯酸酯的單體結構式為CH3﹣CH2COORB.聚丙烯酸酯有固定的熔沸點
C.聚丙烯酸酯能發生加成反應D.合成聚丙烯酸酯的反應屬于加聚反應
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com