
【題目】下列解釋事實的化學用語錯誤的是
A.閃鋅礦(ZnS)經CuSO4溶液作用后,轉化為銅藍(CuS):ZnS + Cu2+=CuS + Zn2+
B.0.1 mol/L 的醋酸溶液pH約為3:CH3COOH ![]() CH3COO- + H+
CH3COO- + H+
C.電解NaCl溶液,陰極區溶液pH增大:2H2O + 2e-=H2↑+ 2OH-
D.鋼鐵發生吸氧腐蝕,負極反應為:Fe-3e-= Fe3+
【答案】D
【解析】
A.溶解度大的物質可以轉化為溶解度小的物質,溶解度ZnS>CuS,則閃鋅礦(ZnS)經CuSO4溶液作用后,轉化為銅藍(CuS),反應的離子方程式為ZnS+Cu2+=CuS+Zn2+,故A正確;
B.0.1mol/L醋酸溶液的pH約為3,說明醋酸為弱酸,部分電離,電離方程式為CH3COOHCH3COO-+H+,故B正確;
C.電解NaCl溶液時,陰極上水得電子生成氫氣和氫氧根離子,離子方程式為2H2O+2e-=H2↑+2OH-,陰極區溶液pH增大,故C正確;
D.鋼鐵發生吸氧腐蝕時,負極上Fe失電子生成亞鐵離子,電極反應式為Fe-2e-=Fe2+,故D錯誤;
故選D。


 閱讀快車系列答案
閱讀快車系列答案科目:高中化學 來源: 題型:
【題目】四氯化錫(SnCl4)常作有機合成的催化劑,在空氣中極易水解生成SnO2·xH2O,實驗室用熔融的錫(熔點為231.9℃)與氯氣反應來制備(同時有SnCl2生成),該反應是放熱反應。可選用的儀器及裝置如圖所示。
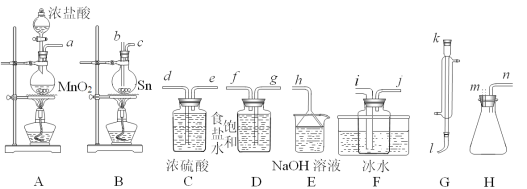
SnCl2、SnCl4有關物理性質如表:
物質 | 顏色、狀態 | 熔點/℃ | 沸點/℃ |
SnCl2 | 無色晶體 | 246 | 623 |
SnCl4 | 無色液體 | -33 | 114 |
(1)已知SnCl2、SnCl4晶體類型相同,SnCl2熔沸點高于SnCl4的原因是:___。
(2)選擇裝置進行連接(填各接口的字母,裝置可重復使用,空格可不填滿)。___
a→__,__→__,__→__,__→__,__→__,__→__,__→__,__→__。
(3)反應開始時,應先點燃裝置___(填“A”或“B”,下同)的酒精燈,待___時,再點然裝置___的酒精燈,并在反應進行中仍持續加熱,其目的是___。
(4)該方法制得的SnCl4中含有少量SnCl2,提純SnCl4的實驗名稱是___。
(5)測定產品純度。取ag產品溶于少量濃鹽酸,加入蒸餾水稀釋至250mL。取20mL稀釋溶液于錐形瓶,滴加幾滴淀粉溶液,用cmol·L-1I2溶液滴定至終點,消耗滴定溶液V mL。
①該產品中SnCl2含量為___%。(滴定反應:Sn2++I2=Sn4++2I-,SnCl2的相對分子質量為:190)
②若操作時間過長、振蕩劇烈,測得產品中SnCl4含量__(填“偏高”或“偏低”或“無影響”)。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】SBP電解法能大幅度提高電解槽的生產能力,如圖為SBP電解法制備MoO3的示意圖,下列說法錯誤的是( )
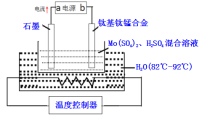
A.a極為電源的負極,發生氧化反應
B.電路中轉移4mol電子,則石墨電極上產生標準狀況下22.4LO2
C.鈦基鈦錳合金電極發生的電極反應為:3H2O+Mo4+-2e-=MoO3+6H+
D.電路中電子流向為:a極![]() 石墨,鈦基鈦錳電極
石墨,鈦基鈦錳電極![]() b極
b極
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】有A、B、C、D四種元素,其中A元素和B元素的原子都有1個未成對電子,A+比B-少一個電子層,B原子得一個電子填入3p軌道后,3p軌道已充滿;C原子的p軌道中有3個未成對電子,其氣態氫化物在水中的溶解度在同族元素所形成的氫化物中最大;D的最高化合價和最低化合價的代數和為4,其最高價氧化物中含D的質量分數為 40%,且其核內質子數等于中子數。R是由A、D兩元素形成的離子化合物,其中A+與D2-離子數之比為2∶1。回答下列問題:
(1)A元素形成的晶體屬于A2密堆積型式,則其晶體內晶胞類型應屬于______(填寫“六方”、“面心立方”或“體心立方”)。
(2)B-的電子排布式為____________,在CB3分子中C元素原子的原子軌道發生的是___________雜化。
(3)C的氫化物的空間構型為____________________,其氫化物在同族元素所形成的氫化物中沸點最高的原因是________________________。
(4)B元素的電負性_______D元素的電負性(填“>”、“<”或“=”);用一個化學方程式說明___________。
(5)如圖所示是R形成的晶體的晶胞,設晶胞的棱長為a cm。試計算R晶體的密度為_______。(阿伏加德羅常數用NA表示)
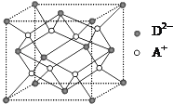
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】以苯酚為原料合成 ![]() 的路線如圖所示。請按要求作答
的路線如圖所示。請按要求作答

(1)寫出苯酚制取A的有機物的有關反應方程式:______。
(2)寫出以下物質的結構簡式:B__________,F____________。
(3)寫出反應④的化學反應方程式:④________,反應類型:_____。
(4)反應⑤可以得到E,同時可能得到的副產物的結構簡式為_______。
(5)寫出反應⑦的反應條件:__________,_________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】高純度單晶硅是典型的無機非金屬材料,又稱“半導體”材料,它的發現和使用曾引起計算機的一場“革命”。這種材料可以按下列方法制備:
SiO2![]() Si(粗)
Si(粗)![]() SiHCl3
SiHCl3![]() Si(純),下列說法正確的是( )
Si(純),下列說法正確的是( )
A.步驟①的化學方程式為SiO2+C![]() Si+CO2↑
Si+CO2↑
B.步驟①、②、③中每生成或反應1 mol Si,轉移4 mol電子
C.二氧化硅能與氫氟酸反應,而硅不能與氫氟酸反應
D.SiHCl3(沸點33.0 ℃)中含有少量的SiCl4(沸點67.6 ℃),通過蒸餾(或分餾)可提純SiHCl3
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】工業上通過氮氣和氫氣反應合成氨,氨經一系列反應可以得到硝酸。反應歷程如下圖所示,下列說法不正確的是( )
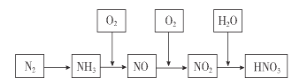
A. 氨可用作制冷劑
B. 銨態氮肥一般不能與堿性化肥共同使用
C. 硝酸可用于制化肥、農藥、炸藥、染料、鹽類等
D. 某濃硝酸中含有溶質2mol,標準狀況下,該濃硝酸與足量的銅完全反應能生成1mol![]()
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】某元素的一個原子形成的離子可表示為![]() n-,下列說法正確的是( )
n-,下列說法正確的是( )
A.![]() n-中含有的中子數為a+b
n-中含有的中子數為a+b
B.![]() n-中含有的電子數為a-n
n-中含有的電子數為a-n
C.X原子的質量數為a+b+n
D.一個X原子的質量約為![]() g
g
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】a、b、c、d、e均為周期表前四周期元素,原子序數依次增大,相關信息如下表所示。
a | 原子核外電子分別占3個不同能級,且每個能級上排布的電子數相同 |
b | 基態原子的p軌道電子數比s軌道電子數少1 |
c | 在周期表所列元素中電負性最大 |
d | 位于周期表中第4縱行 |
e | 基態原子M層全充滿,N層只有一個電子 |
請回答:
(1)d屬于________區的元素,其基態原子的價電子排布圖為_________。
(2)b與其同周期相鄰元素第一電離能由大到小的順序為________(用元素符號表示)。
(3)c的氫化物水溶液中存在的氫鍵有________種,任意畫出一種________。
(4)a與其相鄰同主族元素的最高價氧化物的熔點高低順序為________(用化學式表示)。若將a元素最高價氧化物水化物對應的正鹽酸根離子表示為A,則A的空間構型為________;A的中心原子的軌道雜化類型為________;與A互為等電子體的一種分子為________(填化學式)。
(5)e與Au的合金可形成面心立方最密堆積的晶體,在晶胞中e原子處于面心,該晶體具有儲氫功能,氫原子可進入到由e原子與Au原子構成的四面體空隙中,儲氫后的晶胞結構與金剛石晶胞結構相似,該晶體儲氫后的化學式為________,若該晶體的相對分子質量為M,密度為ag/cm![]() ,則晶胞的體積為________(NA用表示阿伏加德羅常數的值)。
,則晶胞的體積為________(NA用表示阿伏加德羅常數的值)。
(6)a形成的某種單質的層狀結構如圖,其中a原子數、a—a鍵數、六元環數之比為____。

查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com