
【題目】按要求寫出方程式:
(1)鐵和水蒸氣反應(寫出化學方程式)__________________________________________
(2)氫氧化鋇溶液和少量硫酸氫鈉溶液混合(寫出離子方程式)__________________________________
(3)Fe2(SO4)3溶于水(寫出電離方程式) _________________________
(4)CO32— +2H+=CO2↑+H2O(寫出對應的一個化學方程式)___________________
(5)鋁和氫氧化鈉溶液反應(寫出離子方程式)_______________________________________________
【答案】3Fe + 4H2O(g) ![]() Fe3O4 + 4H2 Ba2+ +OH-+H++ SO42— = BaSO4↓+H2O Fe2(SO4)3 = 2Fe3++3SO42- Na2CO3+2HCl=2NaCl+ H2O+CO2↑ 2Al + 2OH— + 2H2O =2AlO2— + 3H2↑
Fe3O4 + 4H2 Ba2+ +OH-+H++ SO42— = BaSO4↓+H2O Fe2(SO4)3 = 2Fe3++3SO42- Na2CO3+2HCl=2NaCl+ H2O+CO2↑ 2Al + 2OH— + 2H2O =2AlO2— + 3H2↑
【解析】
根據要求正確書寫電離方程式、化學方程式、離子方程式。
(1)鐵和水蒸氣反應生成四氧化三鐵,化學方程式為3Fe + 4H2O(g) ![]() Fe3O4 + 4H2;
Fe3O4 + 4H2;
(2)少量硫酸氫鈉與氫氧化鋇時,參加反應的H+、SO42-為1:1,離子方程式為Ba2+ +OH-+H++ SO42- = BaSO4↓+H2O;
(3)Fe2(SO4)3在水溶液中的電離方程式Fe2(SO4)3 = 2Fe3++3SO42-;
(4)CO32- +2H+=CO2↑+H2O表示可溶性碳酸鹽和強酸反應生成可溶性鹽、二氧化碳和水的反應,對應的化學方程式有Na2CO3+2HCl=2NaCl+ H2O+CO2↑等;
(5)鋁和氫氧化鈉溶液反應的離子方程式為2Al + 2OH-+ 2H2O =2AlO2- + 3H2↑。


科目:高中化學 來源: 題型:
【題目】Ⅰ.在有機化學分析中,根據反應的性質和反應產物,即可確定烯烴的組成和結構(雙鍵及支鏈的位置),例如: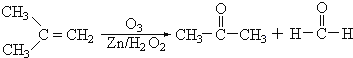
據以上線索和下列反應事實,確定C7H14的結構和名稱:
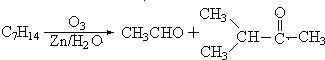
(1)該烴的結構簡式是_______________________________。
(2)名稱是_______________________________。
Ⅱ.把不飽和烴在催化劑存在下用O3氧化則生成有羰基的化合物,其規律可用下式表示:![]() 。現把一定量的以分子式為C4H8的不飽和烴的混合體。用上述方法進行氧化,生成0.5mol酮,1.5mol醛,其中含甲醛0.7mol,另外把1.0mol混合氣體進行加氫反應,生成1.0mol飽和烴的混合氣體。則上述混合氣體經臭氧氧化后 可生成的物質:(用結構簡式表示):_________________。
。現把一定量的以分子式為C4H8的不飽和烴的混合體。用上述方法進行氧化,生成0.5mol酮,1.5mol醛,其中含甲醛0.7mol,另外把1.0mol混合氣體進行加氫反應,生成1.0mol飽和烴的混合氣體。則上述混合氣體經臭氧氧化后 可生成的物質:(用結構簡式表示):_________________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】錫是第ⅣA族第五周期金屬元素,四氯化錫(SnCl4)是重要的媒染劑,易與水反應,熔點為-33℃、沸點為114℃,某研究性學習小組設計如下裝置(部分夾持裝置及加熱儀器省略,MnO2過量)制備SnCl4。
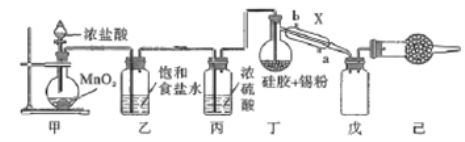
(1)儀器X的名稱是_____,加熱裝置丁前要先排出裝置內的空氣,排出空氣的目的是______,排出空氣的方法是_______
(2)錫粉被吸附在硅膠上,其優點是______,甲中反應的離子方程式_______
(3)裝置己中的試劑是________,實驗過程中,乙裝置內可觀察到的明顯現象是__________
(4)設計一種實驗方案,證明在MnO2過量的情況,鹽酸仍無法反應完______________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列敘述正確的是
A. 1mol任何氣體的體積都是22.4L
B. 同溫同壓下兩種氣體,只要它們的分子數相同,所占體積也一定相同
C. 在標準狀況下,體積為22.4L的物質都是1mol
D. 在非標準狀況下,1mol任何氣體的體積不可能是22.4L
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】標準狀況下,①6.72L NH3 ②1.204×1023個 H2S ③6.4g CH4 ④0.5mol HCl ,下列關系正確的是
A. 體積大小: ④>③>②>① B. 原子數目: ③>①>④>②
C. 密度大小: ④>②>③>① D. 質量大小: ④>③>②>①
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com