
【題目】鎮痛藥物J的合成方法如下:
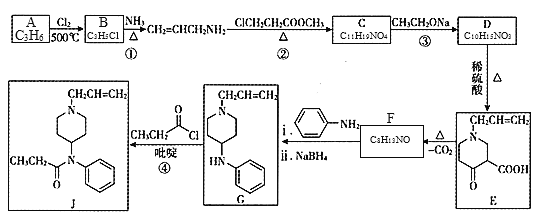
已知:
![]() +Cl-R3
+Cl-R3![]()
![]() +HCl
+HCl
R1COOR2+R3CH2COOR4![]()
![]() +R2OH
+R2OH
![]()
![]()
![]()
(R1、R2、R3、R4為氫或烴基)
(1)B的名稱為______;F的結構簡式為______。
(2)C中含氧官能團名稱為______;②的反應類型為______反應。
(3)③的化學方程式為______。
(4)有機物K分子組成比F少兩個氫原子,符合下列要求的K的同分異構體有______種。
A.遇FeCl3顯紫色 B.苯環上有三個取代基
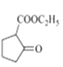
(5)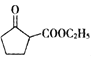 是一種重要的化工中間體。以環已醇(
是一種重要的化工中間體。以環已醇(![]() )和乙醇為起始原料,結合己知信息選擇必要的無機試劑,寫出
)和乙醇為起始原料,結合己知信息選擇必要的無機試劑,寫出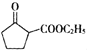 的合成路線______。(已知:RHC=CHR
的合成路線______。(已知:RHC=CHR![]() RCOOH+R′COOH,R、R′為烴基。用結構簡式表示有機物,用箭頭表示轉化關系,箭頭上注明試劑和反應條件)
RCOOH+R′COOH,R、R′為烴基。用結構簡式表示有機物,用箭頭表示轉化關系,箭頭上注明試劑和反應條件)
【答案】3-氯丙烯 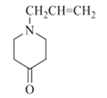 酯基 取代
酯基 取代 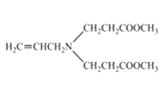
![]()
 +CH3OH 30
+CH3OH 30 ![]()
![]()
![]()
![]()
![]()
![]()
![]()
【解析】
由框圖![]() 可知A為CH3CH=CH2,A到B發生取代反應,B的結構簡式為CH2ClCH=CH2;由框圖
可知A為CH3CH=CH2,A到B發生取代反應,B的結構簡式為CH2ClCH=CH2;由框圖![]() 可知發生了取代反應,根據
可知發生了取代反應,根據![]() +Cl-R3
+Cl-R3![]()
![]() +HCl可知生成的C的結構簡式為
+HCl可知生成的C的結構簡式為![]() ,由
,由![]() 可知,③發生反應的方程式為:
可知,③發生反應的方程式為: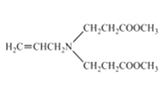
![]()
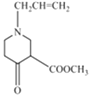 +CH3OH,生成的D的結構簡式
+CH3OH,生成的D的結構簡式  在硫酸作用下加熱發生水解反應生成E,E的結構簡式為
在硫酸作用下加熱發生水解反應生成E,E的結構簡式為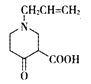 ,再通過
,再通過 得到F,則F的結構簡式為
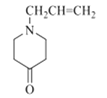 ;然后依次發生取代反應生成G、J;
;然后依次發生取代反應生成G、J;
(6)以環已醇![]() 和乙醇為起始原料合成
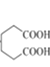
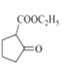
和乙醇為起始原料合成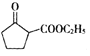 ,環己醇發生消去反應生成環己烯,環己烯發生氧化反應生成己二酸,己二酸發生酯化反應生成己二酸二乙酯,然后發生信息反應生成
,環己醇發生消去反應生成環己烯,環己烯發生氧化反應生成己二酸,己二酸發生酯化反應生成己二酸二乙酯,然后發生信息反應生成 。
。
(1)根據上述分析B的結構簡式為![]() ,則B的名稱為3-氯丙烯(或3-氯-1-丙烯);F的結構簡式為
,則B的名稱為3-氯丙烯(或3-氯-1-丙烯);F的結構簡式為 ,故答案為:3-氯丙烯(或3-氯-1-丙烯);
,故答案為:3-氯丙烯(或3-氯-1-丙烯); ;
;
(2) 根據上述分析C的結構簡式為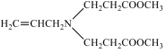 ,C中含氧官能團名稱為酯基;②的反應類型為取代反應,故答案為:酯基;取代;
,C中含氧官能團名稱為酯基;②的反應類型為取代反應,故答案為:酯基;取代;
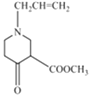
(3) 根據上述分析可知:③的化學方程式為
![]()
 +CH3OH,
+CH3OH,
故答案為:
![]()
 +CH3OH;
+CH3OH;
(4) 根據上述分析F的結構簡式為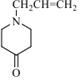 ,有機物K分子組成比F少兩個氫原子,K的同分異構體符合下列條件,A.遇
,有機物K分子組成比F少兩個氫原子,K的同分異構體符合下列條件,A.遇![]() 顯紫色,說明含有酚羥基;B.苯環上有三個取代基,F的不飽和度是3,K的不飽和度是4,苯環的不飽和度是4,所以K的同分異構體中除了苯環外不含其它雙鍵或三鍵,如果取代基為
顯紫色,說明含有酚羥基;B.苯環上有三個取代基,F的不飽和度是3,K的不飽和度是4,苯環的不飽和度是4,所以K的同分異構體中除了苯環外不含其它雙鍵或三鍵,如果取代基為![]() 、
、![]() 、
、![]() ,有10種,如果取代基為
,有10種,如果取代基為![]() 、
、![]() 、
、![]() ,有10種;如果取代基為
,有10種;如果取代基為![]() 、
、![]() 、
、![]() ,有10種,所以符合條件的同分異構體種類是30種,故答案為:30;
,有10種,所以符合條件的同分異構體種類是30種,故答案為:30;
(5)以環已醇(![]() )和乙醇為起始原料合成
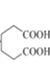
)和乙醇為起始原料合成 ,環己醇發生消去反應生成環己烯,環己烯發生氧化反應生成己二酸,己二酸發生酯化反應生成己二酸二乙酯,然后發生信息反應生成
,環己醇發生消去反應生成環己烯,環己烯發生氧化反應生成己二酸,己二酸發生酯化反應生成己二酸二乙酯,然后發生信息反應生成 ,其合成路線為
,其合成路線為![]()
![]()
![]()
![]()
![]()
![]()
![]()
 ,故答案為:
,故答案為:![]()
![]()
![]()
![]()

![]()
![]()
![]()
 。
。


 唐印文化課時測評系列答案
唐印文化課時測評系列答案 導學與測試系列答案
導學與測試系列答案科目:高中化學 來源: 題型:
【題目】水煤氣變換反應的能量變化如圖。下列敘述錯誤的是
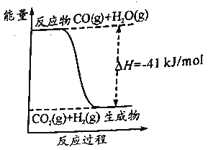
A.反應為:CO(g)+H2O(g)=CO2(g)+H2(g)B.反應物總能量高于生成物總能量
C.H2的燃燒熱為41 kJ·mol-1D.使用催化劑可以降低反應所需活化能
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】實驗室利用SO2和Cl2在活性炭作用下制取SO2C12,原理為SO2(g)+Cl2(g)SO2Cl2(l) H=-97.3kJ/mol。裝置如圖所示(部分裝置已省略)。已知SO2C12的熔點為-54.1℃,沸點為69.1℃,遇水能發生劇烈反應并產生白霧。下列說法正確的是

A.乙中盛放的試劑為無水氯化鈣
B.制備過程中需要將裝置甲置于冰水浴中
C.用來冷卻的水應該從a口入,b口出
D.可用硝酸與亞硫酸鈉反應制備二氧化硫
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列說法正確的是()
A.向 AgCl 、 AgBr 的飽和溶液中滴加少量 AgNO3 溶液,溶液中![]() 不變
不變
B.向0.1mol L1 的CH3COOH 溶液中加入少量水,溶液中![]() 減小
減小
C.0.1mol K2Cr2O7 被完全還原為Cr3 時,轉移的電子數約為1.806 1023
D.一定條件下,反應 2NO(g) 2CO(g) N 2(g) 2CO 2(g) 能自發進行,該反應的ΔH>0
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】C、N、S和Cl元素的單質及化合物在工業生產中的有效利用備受關注。請回答下列問題:
(1)已知:I.2SO2(g)+O2(g)+2H2O(1) =2H2SO4(aq) △H1;
Ⅱ.Cl2(g)+H2O(1)![]() HCl(aq)+HClO(aq) △H2;
HCl(aq)+HClO(aq) △H2;
Ⅲ.2HClO(aq) =2HCl(aq)+O2(g) △H3
SO2(g)+Cl2(g)+2H2O(1)=2HCl(aq)+H2SO4 (aq) △H4=__________(用含有△H1、△H2和△H3的代數式表示)。
(2)25℃時,H2SO3溶液中各含硫微粒的物質的量分數(δ)與溶液pH的變化關系如圖所示。

已知25℃時,NaHSO3的水溶液pH<7,用圖中的數據通過計算解釋原因 ____________________。
(3)利用“ Na-CO2”電池將CO2變廢為寶。我國科研人員研制出的可充電“ Na-CO2”電池,以鈉箔和多壁碳納米管(MWCNT)為電極材料,總反應為4Na+3CO2![]() 2Na2CO3+C。放電時該電池“吸入”CO2,其工作原理如圖所示:
2Na2CO3+C。放電時該電池“吸入”CO2,其工作原理如圖所示:

①放電時,正極的電極反應式為______。
②選用高氯酸鈉—四甘醇二甲醚做電解液的優點是_______(至少寫兩點)。
(4)氯氨是氯氣遇到氨氣反應生成的一類化合物,是常用的飲用水二級消毒劑,主要包括一氯胺、二氯胺和三氯胺(NH2C1、NHC12和NC13),副產物少于其它水消毒劑。
①一氯胺(NH2Cl)的電子式為_______。一氯胺是重要的水消毒劑,其原因是由于一氯胺在中性、酸性環境中會發生水解,生成具有強烈殺菌作用的物質,該反應的化學方程式為_______。
②在恒溫條件下,2molCl2和1molNH3發生反應2Cl2(g)+NH3(g)![]() NHCl2(l)+2HCl(g),測得平衡時Cl2和HCl的物質的量濃度與平衡總壓的關系如圖所示:
NHCl2(l)+2HCl(g),測得平衡時Cl2和HCl的物質的量濃度與平衡總壓的關系如圖所示:

計算C點時該反應的壓強平衡常數Kp(C)= _______ (Kp是平衡分壓代替平衡濃度計算,分壓=總壓×物質的量分數)
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】用 NA 表示阿伏加德羅常數的值,下列說法正確的是()
A.電解精煉銅,當外電路通過 NA 個電子時,陽極質量減小 32 g
B.反應 3H2(g)+N2(g)![]() 2NH3(g)ΔH=-92 kJ·mol-1,當放出 9.2 kJ 熱量時,反應的 N2 為2.24L
2NH3(g)ΔH=-92 kJ·mol-1,當放出 9.2 kJ 熱量時,反應的 N2 為2.24L
C.常溫常壓下 27 克 Al 與 33.6L 氯氣完全反應,電子轉移數小于 3NA
D.1 mol·L-1 氯化銅溶液中,若 Cl-的數目為 2NA,則 Cu2+的數目略小于 NA
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】常溫常壓下電解法合成氨的原理如圖所示。下列說法中錯誤的是( )
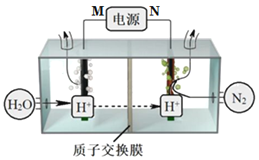
A.M為外接電源的正極
B.右室電極反應式為N2+6H++6e-=2NH3
C.理論上左、右室產生的氣體同溫同壓下體積比為3︰4
D.該合成氨反應是化合反應、放熱反應
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】一種環狀高分子P3的合成路線如圖:
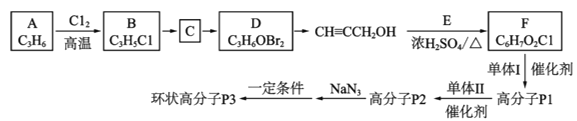
已知:①P2的結構為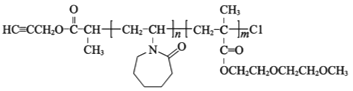
②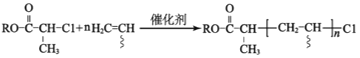 (
(![]() 表示取代基)
表示取代基)
③RCl![]() RN3
RN3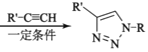
(1)A是一種常用的化工原料,其中包括的官能團是__。
(2)B→C的反應類型是__。
(3)D生成CH![]() CCH2OH的反應條件是__。
CCH2OH的反應條件是__。
(4)上述流程中生成F的反應為酯化反應,則該反應的化學方程式是__。
(5)單體II的結構簡式是__。
(6)下列說法正確的是__(填字母)
a.F→P1的反應類型為縮聚反應
b.P3的結構如圖所示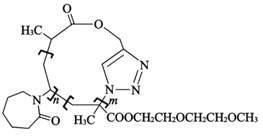
c.P2→P3的過程中可能得到線型高分子
d.堿性條件下,P3可能徹底水解成小分子物質
(7)已知: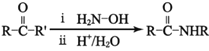 ;Q(C6H11NO)是用于合成單體I的中間體。如圖是以苯酚為原料合成Q的流程,M→N的化學方程式是__。
;Q(C6H11NO)是用于合成單體I的中間體。如圖是以苯酚為原料合成Q的流程,M→N的化學方程式是__。
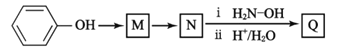
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】![]() 和
和![]() 充入體積不變的密閉容器中,在一定條件下發生下列反應:
充入體積不變的密閉容器中,在一定條件下發生下列反應:![]() ,到達平衡時,
,到達平衡時,![]() 為
為![]() ,如果此時移走
,如果此時移走![]()
![]() 和
和![]() ,在相同溫度下再達平衡時
,在相同溫度下再達平衡時![]() 的物質的量是( )
的物質的量是( )
A.![]() B.
B.![]() C.大于
C.大于![]() ,小于
,小于![]() D.小于
D.小于![]()
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com