
【題目】下表是元素周期表前四周期的一部分,X、Y、Z、R、Q、W、J是7種元素的代號。回答下列問題時,涉及元素書寫的請用相應的元素符號。

(1)J基態原子的核外電子排布式為________。基態Q2+中未成對電子數為________;R和Y的簡單離子與Na+半徑大小順序為________。
(2)X、Y、Z三種元素電負性由大到小的排序是________;X與Y的第一電離能:X________(填“>”“<”或“=”)Y,其理由是________。
(3)檢驗某溶液中是否含有Q3+的方法是_____________________________。
(4)已知WX3是一種引爆劑,受撞擊時分解為兩種單質,則其化學方程式為________________。
【答案】 1s22s22p63s23p63d104s24p5或[Ar]3d104s24p5 4 S2->O2->Na+ F>O>N > N原子的2p軌道電子數為半充滿狀態,較穩定 取少量未知溶液,加入KSCN溶液,若顯紅色,則含Fe3+(其他合理答案均可) 2CuN3![]() 2Cu+3N2↑
2Cu+3N2↑
【解析】由周期表可知:X為氮元素、Y為氧元素、Z為氟元素、R為硫元素、Q鐵元素、W為銅元素、J為溴元素;
(1) 溴元素基態原子的核外電子排布式為1s22s22p63s23p63d104s24p5或[Ar]3d104s24p5;基態Fe2+排布式為1s22s22p63s23p63d44s2,其未成對電子數為4個;S2-、O2-、Na+三種離子中,核外電子排布相同的離子,核電荷數越大,離子半徑越小,所以半徑O2-> Na+,電子層數多的,半徑較大,所以半徑S2-> O2-> Na+,正確答案:S2->O2->Na+。
(2)N、O、F三種元素中,F原子半徑最小,非金屬性最強,電負性最大,所以電負性由大到小的排序是F>O>N;由于N原子的2p軌道電子數為半充滿狀態,較穩定,所以第一電離能 N> O;正確答案:> ;N原子的2p軌道電子數為半充滿狀態,較穩定。
(3)檢驗某溶液中是否含有Fe3+的方法: 取少量未知溶液,加入KSCN溶液,若顯紅色,則含Fe3+;取少量未知溶液,加入苯酚溶液,若顯紫色,則含有Fe3+;正確答案:取少量未知溶液,加入KSCN溶液,若顯紅色,則含Fe3+(其他合理答案均可) 。
(4)已知CuN3是一種引爆劑,受撞擊時分解為兩種單質,一種為氮氣,另外一種為銅,則其化學方程式為2CuN3![]() 2Cu+3N2↑;正確答案:2CuN3
2Cu+3N2↑;正確答案:2CuN3![]() 2Cu+3N2↑。
2Cu+3N2↑。


科目:高中化學 來源: 題型:
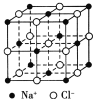
【題目】食鹽晶體是由鈉離子和氯離子組成的,且均為等距離的交錯排列,如圖所示。已知食鹽的密度是2.2 g/cm3,阿伏加德羅常數為6.02×1023/mol。在食鹽晶體中兩個距離最近的鈉離子間的距離最接近于 厘米(保留整數)。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】設NA為阿伏加德羅常數的值。下列說法正確的是
A. 0.1molSiO2晶體中含有Si-O鍵的數目為0.2NA
B. 56g鐵粉與高溫水蒸氣反應,生成H2數目為1.5NA
C. 標準狀況下,22.4 LCl2溶于水,轉移電子數為NA
D. 18gH218O和D2O的混合物中,所含中子數為9NA
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】以柏林綠Fe[Fe(CN)6]為代表的新型可充電鈉離子電池,其放電工作原理如圖所示。下列說法錯誤的是

A. 放電時,正極反應為Fe[Fe(CN)6]+2Na++2e-=Na2Fe[Fe(CN)6]
B. 充電時,Mo(鉬)箔接電源的負極
C. 充電時,Na+通過交換膜從左室移向右室
D. 外電路中通過0.2mol電子的電量時,負極質量變化為2.4g
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】A、B、C、D、E五種短周期元素,原子序數依次增大,B與C能層數相同,D與E能層數相同,C與D價電子結構相同,基態時B、C、D原子核外皆有2個未成對電子,A、E只有1個未成對電子,A能分別與B、C、D、E形成不同的分子。
(1)寫出基態時B的價電子排布圖 ,E—的原子結構示意圖 。
(2)寫出BCD的電子式 ,E2C的結構式 。
(3)根據題目要求完成以下填空:
EC3—中心原子雜化方式 ;DC3中心原子雜化方式 ;
EC4—微粒中的鍵角 ;BC32—微粒的鍵角 ;
DE2分子的立體構型 ;B2A2分子的立體構型 。
(4)一種由A、B、C三種元素組成的分子A2BC2,該分子中σ鍵數目為 ,π鍵數目為 。
(5)根據等電子原理,指出與BC2互為等電子體的離子 (一種即可)
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列有關氧化還原反應的敘述中正確的是( )
A.化合反應一定是氧化還原反應
B.氧化還原反應的本質是元素化合價的升降
C.金屬單質在化學反應中一定作還原劑
D.失電子的反應物在反應中作還原劑,反應中被還原
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】據報道,某些花崗巖會產生氡(![]() Rn),對人體產生傷害。請回答:
Rn),對人體產生傷害。請回答:
(1)該原子的質量數是________,質子數是________,中子數是________。
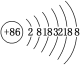
(2)請根據Rn的原子結構預測,氡氣的化學性質________。
A.非常活潑,容易與氧氣等非金屬單質反應
B.比較活潑,能與鈉等金屬反應
C.不太活潑
D.很難與其他物質發生反應
你選擇該選項的理由是______________________________________________。
(3)研究發現,鐳能蛻變為![]() Rn,故稱
Rn,故稱![]() Rn為鐳射氣;釷能蛻變為
Rn為鐳射氣;釷能蛻變為![]() Rn,故將
Rn,故將![]() Rn稱為釷射氣;錒能蛻變為
Rn稱為釷射氣;錒能蛻變為![]() Rn,故將
Rn,故將![]() Rn稱為錒射氣。則
Rn稱為錒射氣。則![]() Rn、
Rn、![]() Rn、
Rn、![]() Rn是________。
Rn是________。
A.同種元素 B.同位素
C.同種核素 D.同種原子
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列離子檢驗的方法正確的是( )
A.某溶液中加硝酸銀溶液生成白色沉淀,說明原溶液中有Cl-
B.某溶液中加Ba(OH)2溶液生成藍色沉淀,說明原溶液中有Cu2+
C.某溶液中加BaCl2溶液生成白色沉淀,說明原溶液中有SO42-
D.某溶液中加稀硫酸溶液產生無色氣體,說明原溶液中有CO32-
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】掌握儀器的名稱、組裝及使用方法是中學化學實驗的基礎,根據下圖所示實驗裝置,回答下列問題。
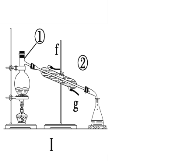
(1)寫出上圖中儀器的名稱:①____________,②_____________。
(2)若利用裝置Ⅰ分離酒精和水的混合物,還缺少的儀器___________;②中進水口是________(填“f”或“g”)。
(3)下列實驗需要在哪套裝置中進行(填序號):
a.從海水中提取蒸餾水:______; b.分離氯化鈉和水:______;
c.分離碳酸鈣和水:______; d.分離植物油和水:______。
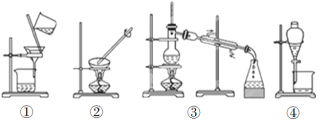
(4)裝置②中玻璃棒的作用是__________________________________。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com