
【題目】通過近一年的化學學習,你已經掌握了實驗室制取氣體的有關規律,以下是老師提供的一些實驗裝置,根據下圖回答下列問題:
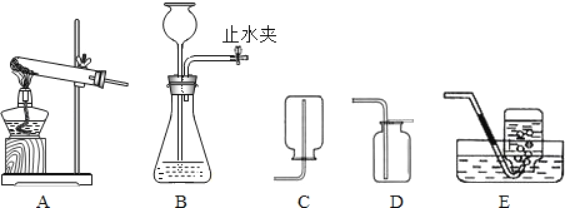
(1)關閉B裝置中的止水夾后,從長頸漏斗向錐形瓶中注入一定量的水,靜止后如圖所示,則B裝置是否漏氣?_____(填“漏氣”、“不漏氣”或“無法確定”).
(2)寫出實驗室用B裝置制取氧氣的化學方程式_____.
(3)如果實驗室用A裝置來制取氧氣,同時要收集一瓶用于做鐵絲燃燒實驗的氧氣,則最好選用_____(填上圖中裝置編號的字母,下同)收集氧氣.
(4)通過查閱資料得知:氨氣(NH3)是一種密度比空氣小且極易溶于水的氣體,其水溶液稱為氨水.小楓同學用加熱氯化銨和氫氧化鈣的固體混合物來制取氨氣,他應選擇的發生裝置是_____,收集裝置是_____.
(5)小雯同學將收集滿氨氣的集氣瓶倒扣在滴有無色酚酞的水中,觀察到的現象是集氣瓶內的水面上升,而且水變_____(填一種顏色).
【答案】漏氣 2H2O2![]() 2H2O+O2↑ E A C 紅
2H2O+O2↑ E A C 紅
【解析】
(1)現在裝置內的液面和長頸漏斗內的液面持平,說明裝置漏氣;
(2)實驗室制氧氣的三種方法中只有分解過氧化氫溶液的方法選用固﹣液不加熱型的發生裝置。反應的化學方程式為:2H2O2![]() 2H2O+O2↑;
2H2O+O2↑;
(3)做細鐵絲在氧氣中燃燒的實驗時,應在集氣瓶底部裝少量水,防止燃燒生成物濺落下來炸裂瓶底,所以最好用排水法收集,并且不要收集滿。故選:E;
(4)反應物的狀態是固態,反應條件是加熱,應選固﹣固加熱型的發生裝置,故選A;氨氣密度比空氣小,極易溶于水,用向下排空氣法收集,故選C;
(5)氨氣的水溶液是氨水,氨水顯堿性,能使無色酚酞溶液變成紅色。


 閱讀快車系列答案
閱讀快車系列答案科目:初中化學 來源: 題型:
【題目】以菱鎂礦(主要成分為MgCO3,含少量FeCO3,其他雜質不溶,也不參加反應)為原料制備硫酸鎂的實驗流程如下圖
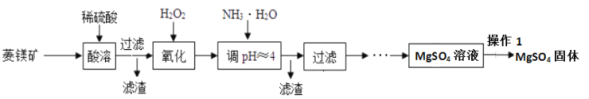
(1)菱鎂礦原料屬于________________。(“混合物”、“純凈物”)
(2)該過程中加入雙氧水的反應為:H2O2 + 2FeSO4 + H2SO4 = Fe2(SO4)3 + 2H2O,反應物H2O2中O元素的化合價為____________,溶液顏色由淺綠色變為_______色。
(3)實驗室模擬調節溶液pH≈4的步驟, 用________蘸取待測液點pH試紙的中部,然后迅速與標準比色卡對比讀數,且讀數為___________(“小數”、“整數”),該過程中若提前潤濕pH試紙,則可能導致________(填“升高”、“降低”或“不變”)。
(4)操作1與過濾均要用到一種玻璃儀器,該儀器在操作1中的作用是___________。
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】某化學興趣小組同學,用鹽酸和氫氧化鈉進行“酸堿中和反應”的探究,進行一段時間后發現沒有明顯變化,詢問老師才知道忘記滴加指示劑。因此,他們停止實驗,并在老師的指導下對燒杯內的溶液中的溶質的成分進行探究。
(提出問題)該燒杯內的溶質是什么?
(猜想假設)猜想一:NaCl 猜想二:NaCl和HCl
猜想三:NaCl和NaOH 猜想四:NaCl、NaOH和HCl
同學們討論后一致認為猜想四不合理,請你說出不合理的理由______________________(用化學方程式表示)。
(查閱資料)NaCl溶液呈中性。
(實驗探究)興趣小組甲、乙、丙三位同學分別設計了如下的實驗方案,請你幫助他們完成實驗報告的相關內容。
實驗方案 | 實驗現象 | 實驗結論 |
甲同學取少量燒杯內的溶液于試管中,滴入酚酞試液 | 溶液無變化 | 猜想一成立 |
乙同學另取少量燒杯內的溶液于試管中,加入_______。 | 有氣泡生成 | 猜想二成立 |
丙同學另取少量燒杯內的溶液于試管中,滴加適量的CuSO4溶液 | 沒有藍色沉淀產生 | 猜想____不成立 |
(評價反思)老師看了甲、乙、丙三位同學的實驗報告,指出甲同學的實驗結論不準確,請你分析甲同學實驗結論不準確的原因:___________。
(得出結論)猜想二成立
(拓展延伸)某同學在進行酸堿中和滴定實驗時,測得溶液的pH變化如下圖1所示,請回答下列問題:

(1)由圖1可知,該同學實驗操作是________________。
A.將鹽酸滴入氫氧化鈉溶液中
B.將氫氧化鈉溶液滴入鹽酸中
(2)由圖1可知,在b點處溶液中溶質是______________________。
(3)圖2為鹽酸和氫氧化鈉溶液反應的微觀過程,從微粒的角度分析,此反應的微觀實質_______________(合理答案即可)。
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】新能源汽車的研發和使用是時代發展的需要。
(1)目前人們利用最多的能源是煤、石油和___________等化石燃料。它們都是___________能源(填“可再生”或“不可再生”)煤燃燒會產生二氧化碳、二氧化硫、一氧化碳等氣體,這些氣體中,溶于雨水會形成酸雨的是___________。科學家正在努力開發和利用的新能源有__________(寫一種)等。
(2)鋰電池可為新能源汽車提供動力,下列結構示意圖表示的粒子與鋰原子的化學性質最為相似的是___(填序號)。

(3)鋰(Li)的金屬活潑性強于鋁,它與稀硫酸反應的化學方程式為________________。新能源汽車除了節約化石能源外,其主要優點是___________________________。
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】如圖表示稀硫酸和氫氧化鈉溶液發生反應時燒杯中溶液的pH隨加入液體體積的變化曲線,請回答下列問題:
(1)燒杯中盛放的液體是______(填字母:A.稀硫酸B.氫氧化鈉溶液),燒杯中發生反應的微觀實質是______。
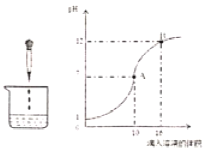
(2)曲線上A點表示______,B點時溶液中的離子有______(填離子符號)
(3)小強完成上述實驗幾天后發現,忘記蓋上盛放氫氧化鈉溶液試劑瓶的瓶塞。小強設計了如下實驗兩個方案來檢驗氫氧化鈉溶液是否變質以及變質的程度
實驗方案 | 實驗步驟 | 實驗現象 | 實驗結論 |
方案一 | 取少量溶液于試管中,滴加幾滴稀鹽酸 | 沒有氣體產生 | 沒有變質 |
方案二 | 取少量溶液于試管中,滴加幾滴氫氧化鈣溶液 | ① ______ | 已經變質 |
②小東認為方案一的實驗設計不嚴謹,其原因是:______。請寫出方案二中反應的化學方程式______。
③如果要確定氫氧化鈉溶液是部分變質還是完全變質,以下方案合理的是______(填字母,已知氯化鈣溶液呈中性)
A.另取溶液少許,加入適量氫氧化鈣溶液,過濾,再向濾液中加入酚酞
B.另取溶液少許,加入足量的氯化鈣溶液,過濾,再向濾液中加入酚酞
C.另取溶液少許,加入少量的氯化鈣溶液,過濾,再向濾液中加入酚酞
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】在元素周期表中,鎵元素的信息如圖所示。下列有關鎵的說法不正確的是
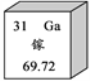
A. 屬于金屬元素B. 元素符號是Ga
C. 相對原子質量為69.72gD. 原子的核電荷數是31
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】我們日常生活中,食用的食鹽大多來自海水晾曬.海水經蒸發結晶后可獲得含有少量泥沙和雜質的粗鹽.
(1)為了除去粗鹽中含有的少量泥沙,某小組設計了如圖所示的實驗:在粗鹽提純的過程中,正確的操作順序是(填序號)______;
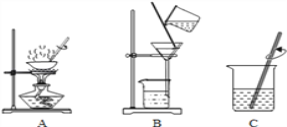
(2)準備過濾器時,為了讓折好的濾紙緊貼漏斗壁,應該怎樣操作:__________。
(3)實驗小組實驗數據如下:
稱取粗鹽/g | 溶解粗鹽/g | 剩余粗鹽/g | 精鹽/g | 精鹽產率/% |
5.0 | 3.6 | 1.4 | 2.8 | ? |
該同學的精鹽產率為:_______ 。(保留整數)
(4)某同學所得的產率與其他同學比較明顯偏低,下列哪些情況導致產率明顯偏低______(選填字母序號)
A.溶解時將5.0g粗鹽一次全部倒入10mL水中,立即過濾
B.蒸發時有少量液體、固體濺出
C.提純后的精鹽尚未完全干燥就稱其質量
(5)粗鹽提純后得到的“精鹽”中還含有少量可溶性雜質CaCl2、MgCl2.實驗小組的同學設計了以下實驗方案來除去可溶性雜質.
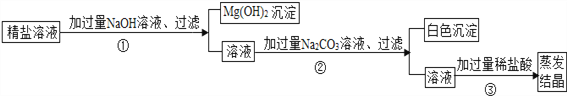
①步驟①的化學方程式為___________。
②步驟②中的白色沉淀為___________。
③步驟③中加稀鹽酸是為了除去溶液中_____________。
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】科技節活動中,化學興趣小組做了如圖實驗,請回答以下問題.
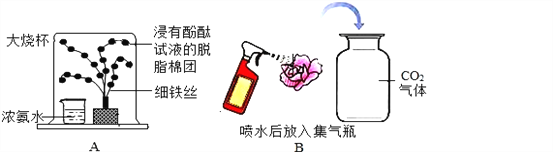
(1)圖A所示實驗可觀察到“鐵樹”上浸有無色酚酞試液的棉團由白色變為__________色,該實驗中沒有涉及的性質是__________(填字母).
A.氨分子是不斷運動的 B.氨分子有一定質量 C.濃氨水具有揮發性
(2)圖B所示實驗觀察到紫色小花變為紅色,小花變紅的原因是__________(用化學方程式表示).
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】學習小組欲從高錳酸鉀制氧氣剩余回收副產物,設計了如圖所示實驗方案;
(資料卡片)①KMnO4 能和纖維素反應,在中性溶液中比較穩定,加熱堿性條件中的 KMnO4 溶液會有部分KMnO4 和 H2O 反應,生成 MnO2;
②錳酸鉀溶于水為墨綠色,不穩定,在水溶液中能全都轉化為 KMnO4,MnO2 和 KOH,反應的化學方程式如下:3K2MnO42H2O2KMnO4MnO24KOH
(實驗方案)
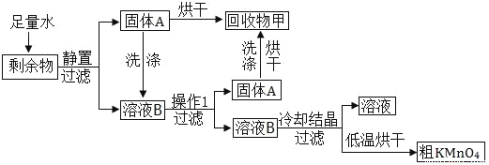
(1)將剩余物加入水中,觀察到的現象是:①部分固體溶解;②有少量不溶物出現;③_______。
(2)回收物甲是_______(填化學式)。
(3)濾液B中含有KOH,需要加入少量硫酸進行中和,反應的化學方程式是_______。
(4)冷卻結晶后,低溫烘干高錳酸鉀晶體是為了防止_______。
(5)加熱 31.6gKMnO4 使之完全分解,按以上實驗方案可得回收物甲的質量可能是_______。
A.8.7g B.11.5g C.12.8g D.28.4g
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com