
題目列表(包括答案和解析)
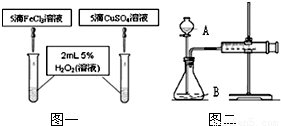
| 實驗步驟(夾持固定裝置已略去) | A、B、C三支試管中分別盛有等體積5%的過氧化氫溶液,如圖所示進行實驗.儀器a的名稱是 試管 試管 ,C中用于加熱儀器的名稱是酒精燈 酒精燈  | ||||
| 實驗現象 | A:試管壁有氣泡附著,帶火星的木條不復燃. B:有大量氣泡產生,帶火星的木條復燃. C:有大量氣泡產生,帶火星的木條不復燃. D:有大量氣泡產生,用帶火星的木條檢驗收集的氣體,木條復燃. | ||||
| 分析 | B試管中發生反應的文字表達式 過氧化氫
過氧化氫 .
實驗結束后儀器b中的液體質量都減少,原因是 反應生成了氧氣逸出 反應生成了氧氣逸出 加熱反應的過程中有水蒸氣逸出 加熱反應的過程中有水蒸氣逸出 | ||||
| 結論 | ①分析A、B實驗可以得出的結論是: 二氧化錳可以加快過氧化氫的分解 二氧化錳可以加快過氧化氫的分解 .②加熱 能 能 (填“能”或“不能”)促進過氧化氫分解產生氫氣. |
| 實驗次序 | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 |
| 二氧化錳( MnO2 )粉末用量(g) | 0.1 | 0.2 | 0.3 | 0.4 | 0.5 | 0.6 | 0.7 | 0.8 |
| 所用時間(t) | 170 | 80 | 70 | 50 | 40 | 30 | 20 | 20 |
 在我校實驗室實施的揚州市2011年中考化學實驗操作考查剛剛落下帷幕.實驗考查中H2O2分解制氧氣為何不采用MnO2作催化劑?同學們為之展開了探究.
在我校實驗室實施的揚州市2011年中考化學實驗操作考查剛剛落下帷幕.實驗考查中H2O2分解制氧氣為何不采用MnO2作催化劑?同學們為之展開了探究.| 催化劑及用量 | O2 平均產量 | 制氧所需時間 | 成本 | 反應情況 |
| MnO21.0g | 919mL | 10′03″ | 0.11元 | 分解先快后慢 |
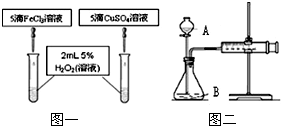
| 10%FeCl3溶液5滴 | 985mL | 4′50″ | 0.02元 | 均勻產生O2 |
| 15%CuSO4溶液5滴 | 955mL | 4′57″ | 0.03元 | 均勻產生O2 |
| ||
| ||
| 濃度 時間(min) 條件 |
30% H2O2 | 15% H2O2 | 5% H2O2 |
| 加入a g MnO2 | 0.2 | 0.8 | 2.0 |
 在我校實驗室實施的揚州市2011年中考化學實驗操作考查剛剛落下帷幕.實驗考查中H2O2分解制氧氣為何不采用MnO2作催化劑?同學們為之展開了探究.
在我校實驗室實施的揚州市2011年中考化學實驗操作考查剛剛落下帷幕.實驗考查中H2O2分解制氧氣為何不采用MnO2作催化劑?同學們為之展開了探究.| 催化劑及用量 | O2 平均產量 | 制氧所需時間 | 成本 | 反應情況 |
| MnO21.0g | 919mL | 10′03″ | 0.11元 | 分解先快后慢 |
| 10%FeCl3溶液5滴 | 985mL | 4′50″ | 0.02元 | 均勻產生O2 |
| 15%CuSO4溶液5滴 | 955mL | 4′57″ | 0.03元 | 均勻產生O2 |

| 濃度 時間(min) 條件 | 30% H2O2 | 15% H2O2 | 5% H2O2 |
| 加入a g MnO2 | 0.2 | 0.8 | 2.0 |
| 催化劑及用量 | O2 平均產量 | 制氧所需時間 | 成本 | 反應情況 |
| MnO21.0g | 919mL | 10′03″ | 0.11元 | 分解先快后慢 |
| 10%FeCl3溶液5滴 | 985mL | 4′50″ | 0.02元 | 均勻產生O2 |
| 15%CuSO4溶液5滴 | 955mL | 4′57″ | 0.03元 | 均勻產生O2 |
| 濃度 時間(min) 條件 | 30% H2O2 | 15% H2O2 | 5% H2O2 |
| 加入a g MnO2 | 0.2 | 0.8 | 2.0 |

| 催化劑及用量 | O2 平均產量 | 制氧所需時間 | 成本 | 反應情況 |
| MnO21.0g | 919mL | 10′03″ | 0.11元 | 分解先快后慢 |
| 10%FeCl3溶液5滴 | 985mL | 4′50″ | 0.02元 | 均勻產生O2 |
| 15%CuSO4溶液5滴 | 955mL | 4′57″ | 0.03元 | 均勻產生O2 |

| 濃度 時間(min) 條件 | 30% H2O2 | 15% H2O2 | 5% H2O2 |
| 加入a g MnO2 | 0.2 | 0.8 | 2.0 |

湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com