
科目: 來源: 題型:
【題目】為了合理利用化學能,確保安全生產,化工設計需要充分考慮化學反應的反應熱,并采取相應措施.化學反應的反應熱通常用實驗進行測定,也可進行理論推算.
(1)實驗測得,5g甲醇(CH3OH)液體在氧氣中充分燃燒生成二氧化碳氣體和液態水時釋放出113.5kJ的熱量,則表示甲醇標準燃燒熱的熱化學方程為:________________。
(2)今有如下兩個熱化學方程式:則a_________b(填“>”、“=”或“<”)
2H2(g)+O2(g)=2H2O(g)△H1=a kJmol﹣1
2H2(g)+O2(g)=2H2O(l)△H2=b kJmol﹣1
(3)已知反應N2(g)+3H2(g)═2NH3(g)△H=a kJmol﹣1.試根據表中所列鍵能數據估算a 的值:________________________(注明“+”或“﹣”)。
化學鍵 | H﹣H | N﹣H | N≡N |
鍵能/kJmol﹣1 | 436 | 391 | 945 |
(4)依據蓋斯定律可以對某些難以通過實驗直接測定的化學反應的反應熱進行推算.利用水煤氣合成二甲醚的三步反應如下:
①2H2(g)+CO(g)═CH3OH(g)△H=﹣90.8kJmol﹣1
②2CH3OH(g)═CH3OCH3(g)+H2O(g)△H=﹣23.5kJmol﹣1
③CO(g)+H2O(g)═CO2(g)+H2(g)△H=﹣41.3kJmol﹣1
總反應:3H2(g)+3CO(g)═CH3OCH3(g)+CO2(g)的△H=_________.
(5)已知H+(aq)+OH-(aq) =H2O(l) ΔH=-57.3 kJ·mol-1。
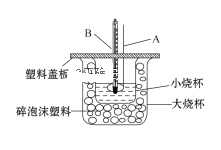
①儀器A的名稱___________________;碎泡沫塑料的作用是___________________。
②儀器A不能用銅質攪拌棒代替,其原因是________________________。
③若通過實驗測定中和熱的ΔH的絕對值常常小于57.3 kJ/mol,其原因可能是_______
a.實驗裝置保溫、隔熱效果差
b.量取NaOH溶液的體積時仰視讀數
c.分多次把NaOH溶液倒入盛有鹽酸的小燒杯中
d.用溫度計測定鹽酸初始溫度后,直接測定氫氧化鈉溶液的溫度
查看答案和解析>>
科目: 來源: 題型:
【題目】硼氫化鈉(NaBH4)為白色粉末,熔點400℃,容易吸水潮解,可溶于異丙胺(熔點:-101℃,沸點:33℃),在干燥空氣中穩定,吸濕而分解,是無機合成和有機合成中常用的選擇性還原劑。某研究小組采用偏硼酸鈉(NaBO2)為主要原料制備NaBH4,其流程如圖:下列說法不正確的是( )
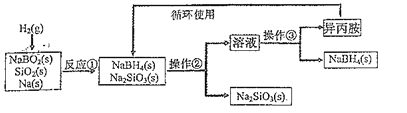
A.NaBH4中H元素顯+1價
B.操作③所進行的分離操作是蒸餾
C.反應①為NaBO2+SiO2+4Na+2H2═NaBH4+2Na2SiO3
D.實驗室中取用少量鈉需要用到的實驗用品有鑷子、濾紙、玻璃片和小刀
查看答案和解析>>
科目: 來源: 題型:
【題目】某化學小組為了研究外界條件對化學反應速率的影響,進行了如下實驗:
(實驗原理)2KMnO4 + 5H2C2O4 + 3H2SO4 = K2SO4 + 2MnSO4 + 10CO2↑ + 8H2O
(實驗內容及記錄)
實驗編號 | 室溫下,試管中所加試劑及其用量 / mL | 室溫下溶液顏色褪至無色所需時間 / min | |||
0.6 mol/L H2C2O4溶液 | H2O | 3 mol/L 稀硫酸 | 0.05mol/L KMnO4溶液 | ||
1 | 3.0 | 2.0 | 2.0 | 3.0 | 1.5 |
2 | 2.0 | 3.0 | 2.0 | 3.0 | 2.7 |
3 | 1.0 | 4.0 | 2.0 | 3.0 | 3.9 |
請回答:
(1)根據上表中的實驗數據,可以得到的結論是___________________________________。
(2)利用實驗1中數據計算,若用KMnO4的濃度變化表示的反應速率為:υ(KMnO4)= ________。
(3)該小組同學根據經驗繪制了n(Mn2+) 隨時間變化趨勢的示意圖,如圖1所示。但有同學查閱已有的實驗資料發現,該實驗過程中n(Mn2+) 隨時間變化的趨勢應如圖2所示。該小組同學根據圖2所示信息提出了新的假設,并繼續進行實驗探究。
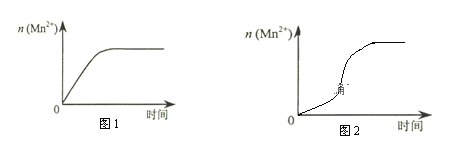
①該小組同學提出的假設是___________________________________________________。
②請你幫助該小組同學完成實驗方案,并填寫表中空白。
實驗編號 | 室溫下,試管中所加試劑及其用量 / mL | 再向試管中加入少量固體 | 室溫下溶液顏色褪至無色所需時間 / min | |||
0.6mol/L H2C2O4溶液 | H2O | 3mol/L稀硫酸 | 0.05mol/L KMnO4溶液 | |||
4 | 3.0 | 2.0 | 2.0 | 3.0 | _______ | t |
③若該小組同學提出的假設成立,應觀察到的現象是_____________________________________。
查看答案和解析>>
科目: 來源: 題型:
【題目】在已經發現的一百多種元素中,除稀有氣體外,非金屬元素只有十多種,但與生產生活有密切的聯系。
(1)氮是動植物生長不可缺少的元素,合成氨的反應對人類解決糧食問題貢獻巨大,反應如下:
N2(g)+3H2(g) ![]() 2NH3(g)。
2NH3(g)。
①合成氨的反應中的能量變化如圖所示。

該反應是___________反應(填“吸熱”或“放熱”),其原因是反應物化學鍵斷裂吸收的總能量_____(填“大于”或“小于”)生成物化學鍵形成放出的總能量。
②在一定條件下,將一定量的N2和H2的混合氣體充入某定容密閉容器中,一段時間后,下列敘述不能說明該反應達到平衡狀態的是___________(填序號)。
A.容器中混合氣體的密度不隨時間變化
B.單位時間內斷裂3 mol H-H鍵的同時斷裂6 mol N-H鍵
C. N2 、H2 、NH3的物質的量之比為1:3:2
D.容器中混合氣體的平均相對分子質量不隨時間變化
(2)容器容積為1L,T2℃在起始體系中加入1 mol N2 、3molH2,經過5 min反應達到平衡時放55.44kJ。保持容器體積和溫度不變,若起始時向容器內放入2 mol N2和6 mol H2,達平衡后放出的熱量為Q,則Q___110.88 kJ(填“>”、“<”或“=”)。
(3)目前工業上有一種方法是用CO2生產燃料甲醇。一定條件下發生反應:CO2(g)+3H2(g) ![]() CH3OH(g)+H2O(g),在體積為1 L的密閉容器中,充入1 molCO2和3 molH2,測得CO2和CH3OH(g)的濃度隨時間變化如下圖所示。
CH3OH(g)+H2O(g),在體積為1 L的密閉容器中,充入1 molCO2和3 molH2,測得CO2和CH3OH(g)的濃度隨時間變化如下圖所示。
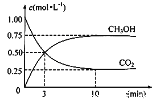
達平衡時容器內平衡時與起始時的壓強之比___。
(4)有可逆反應Fe(s)+CO2(g) ![]() FeO(s) + CO(g) △H>0。
FeO(s) + CO(g) △H>0。
①若起始時把Fe和CO2放入體積固定的密閉容器中,CO2的起始濃度為2.0mol/L,某溫度時達到平衡,此時容器中CO的濃度為1.0 mol/L,則該溫度下上述反應的平衡常數K=______________(保留二位有效數字)。
②若該反應在體積固定的密閉容器中進行,在一定條件下達到平衡狀態,如果改變下列條件,反應混合氣體中CO2的物質的量分數如何變化(選填“增大”、“減小”、“不變”)。升高溫度________________;再通入CO_________________。
③該反應的逆反應速率隨時間變化的關系如圖:
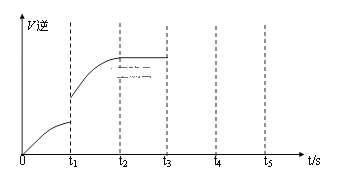
從圖中看到,反應在t2時達平衡, 在t1時改變了某種條件,改變的條件可能是(填序號)______________。(單選)
A.升溫 B.增大CO2濃度
④如果在t3時從混合物中分離出部分CO,t4~ t5時間段反應處于新平衡狀態,請在圖上畫出t3~ t5的V(逆)變化曲線____________________________。
查看答案和解析>>
科目: 來源: 題型:
【題目】已知甲、乙、丙三種物質均含有同種元素X,其轉化關系如下:
![]()
下列說法錯誤的是
A.若A為NaOH溶液,乙為白色沉淀,則X可能為短周期金屬元素
B.若A為硝酸,X為金屬元素,則甲與乙反應可生成丙
C.若A為氧氣,丙在通常狀況下為紅棕色氣體,則甲可能為非金屬單質
D.若乙為NaHCO3,則甲或丙可能是CO2
查看答案和解析>>
科目: 來源: 題型:
【題目】下列離子方程式中,正確的是( )
A.Fe3+的檢驗:Fe3++3KSCN═Fe(SCN)3+3K+
B.氯氣用于自來水消毒:Cl2+H2O═H++Cl-+HClO
C.證明H2O2具有還原性:2MnO4-+6H++3H2O2═2Mn2++4O2↑+6H2O
D.用CuCl2溶液做導電性實驗,燈泡發光:CuCl2 ![]() Cu2++2Cl-
Cu2++2Cl-
查看答案和解析>>
科目: 來源: 題型:
【題目】在容積相同的兩個密閉容器M和N中,保持溫度為150 ℃,向M容器中加入a mol HI,同時向N容器中加入b mol HI (a>b)。當反應2HI(g)![]() H2 (g) + I2 (g) 達到平衡后,下列說法正確的是
H2 (g) + I2 (g) 達到平衡后,下列說法正確的是
A.從反應開始到達到平衡,所需時間tM > tN
B.平衡時cM(I2) = c N(I2)
C.平衡時I2 蒸氣在混合氣體中的體積分數:M > N
D.HI的平衡分解率αM = αN
查看答案和解析>>
科目: 來源: 題型:
【題目】在20 L的密閉容器中按物質的量之比1∶2充入CO和H2,發生:CO(g)+2H2(g) ![]() CH3OH(g) ΔH。測得CO的轉化率隨溫度的變化及不同壓強下CO轉化率的變化、p2和195 ℃時n(H2)隨時間的變化結果如圖表所示。下列說法正確的是( )
CH3OH(g) ΔH。測得CO的轉化率隨溫度的變化及不同壓強下CO轉化率的變化、p2和195 ℃時n(H2)隨時間的變化結果如圖表所示。下列說法正確的是( )

A.0~3 min,平均速率v(CH3OH)=0.8 mol·L-1·min-1
B.p1<p2,ΔH>0
C.在p2和195 ℃時,該反應的平衡常數為25( mol·L-1)-2
D.在B點時,v正>v逆
查看答案和解析>>
科目: 來源: 題型:
【題目】已知2CO(g)+O2(g)=2CO2(g) ΔH= -566 kJmol-1
Na2O2(s)+CO2(g) = Na2CO3(s)+1/2O2(g) ΔH= -226 kJmol-1
下列表述正確的是
A.1molCO燃燒時放出的熱量為283kJmol-1
B.Na2O2(s)+CO(g)=Na2CO3(s)ΔH=-509kJmol-1
C.Na2O2(s)與CO2(g)反應放出226kJ熱量時電子轉移數為2NA
D.Na2O2和Na2CO3中陰陽離子個數比不同
查看答案和解析>>
科目: 來源: 題型:
【題目】某溫度時,Ag2SO4在水中的沉淀溶解平衡曲線如圖所示。該溫度下,下列說法正確的是

A. 含有大量SO42-的溶液中肯定不存在Ag+
B. Ag2SO4的溶度積常數(Ksp)為1×10-3
C. 0.02 mol·L-1的AgNO3溶液與0.02 mol·L-1的Na2SO4溶液等體積混合不會生成沉淀
D. a點表示Ag2SO4的不飽和溶液,蒸發可以使溶液由a點變到b點
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com