
【題目】孔雀石的主要成分是Cu2(OH)2CO3。我國古人用孔雀石和焦炭混合共熱的方法煉銅,其冶煉方法屬于
A. 熱還原法B. 濕法煉銅C. 熱分解法D. 電解冶煉法
【答案】A
【解析】
一般來說,活潑金屬K、Ca、Na、Mg、Al一般用電解熔融的氯化物(Al是電解熔融的三氧化二鋁)制得;較活潑的金屬Zn、Fe、Sn、Pb、Cu等用熱還原法制得,常用還原劑有(C、CO、H2等);不活潑金屬Hg、Ag用加熱分解氧化物的方法制得,Pt、Au用物理分離的方法制得,據此分析解答。
A.孔雀石受熱發生分解:Cu2(OH)2CO3![]() 2CuO+CO2↑+H2O,由CuO煉銅,可用焦炭還原法:2CuO+C
2CuO+CO2↑+H2O,由CuO煉銅,可用焦炭還原法:2CuO+C![]() 2Cu+CO2↑,屬于熱還原法,A正確;
2Cu+CO2↑,屬于熱還原法,A正確;
B. Cu2(OH)2CO3和CuO都不溶于水,且當時沒有強酸,也不可能采用濕法煉銅,B錯誤;
C.Al的活潑性大于Cu,所以掌握Cu的冶煉方法早于Al,雖然也可用鋁熱還原法:3CuO+2Al![]() Al2O3+3Cu,但我國古代還沒有掌握冶煉鋁的技術,因此不可能采用鋁熱法冶煉,C項錯誤;
Al2O3+3Cu,但我國古代還沒有掌握冶煉鋁的技術,因此不可能采用鋁熱法冶煉,C項錯誤;
D.我國古代沒有電,不可能用電解冶煉法,D錯誤;
故合理選項是A。


科目:高中化學 來源: 題型:
【題目】某探究小組用HNO3與大理石反應過程中質量減小的方法,研究影響反應速率的因素。所用HNO3濃度為1.00 mol·L-1、2.00 mol·L-1,大理石有細顆粒與粗顆粒兩種規格,實驗溫度為298 K、308 K,每次實驗HNO3的用量為25.0 mL、大理石用量為10.00 g。
(1)請完成以下實驗設計表,并在實驗目的一欄中填出對應的實驗編號:
實驗編號 | T/K | 大理石規格 | HNO3濃度/mol·L-1 | 實驗目的 |
① | 298 | 粗顆粒 | 2.00 | (Ⅰ)實驗①和②探究HNO3濃度對該反應速率的影響; (Ⅱ)實驗①和③探究溫度對該反應速率的影響; (Ⅲ)實驗①和④探究大理石規格(粗、細)對該反應速率的影響; |
② | _____ | _____ | _____ | |
③ | _____ | _____ | _____ | |
④ | _____ | _____ | _____ |
(2)實驗裝置如圖1所示,如何檢驗該裝置的氣密性________________________________

(3)實驗①中CO2質量隨時間變化的關系見下圖2:依據反應方程式CaCO3+2HNO3=Ca(NO3)2+CO2↑+H2O,計算實驗①在70-90 s范圍內HNO3的平均反應速率________________________
(4)請在答題卡的框圖中,畫出實驗②、③和④中CO2質量隨時間變化關系的預期結果示意圖。_______
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列反應中,屬于取代反應的是
①CH3CH=CH2+Br2![]() CH3CHBrCH2Br
CH3CHBrCH2Br
②CH3CH2OH![]() CH2=CH2+H2O
CH2=CH2+H2O
③CH3COOH+CH3CH2OH![]() CH3COOCH2CH3+H2O
CH3COOCH2CH3+H2O
④C6H6+HNO3![]() C6H5NO2+H2O
C6H5NO2+H2O
A. ①②B. ③④C. ①③D. ②④
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】葡萄酒中的酒精是葡萄果實中的糖發酵后的產物(C6H12O6![]() 2CH3CH2OH+2CO2↑)。
2CH3CH2OH+2CO2↑)。
Ⅰ、已知:實驗室制乙烯原理為CH3CH2OH![]() CH2=CH2↑+H2O,產生的氣體能使Br2的四氯化碳溶液褪色,甲、乙同學用下列實驗驗證。(氣密性已檢驗,部分夾持裝置略)。
CH2=CH2↑+H2O,產生的氣體能使Br2的四氯化碳溶液褪色,甲、乙同學用下列實驗驗證。(氣密性已檢驗,部分夾持裝置略)。

實驗操作和現象:
操 作 | 現 象 |
點燃酒精燈,加熱至170℃ | Ⅰ:A中燒瓶內液體漸漸變黑 |
…… | |
實驗完畢,清洗燒瓶 | Ⅲ:A中燒瓶內附著少量黑色顆粒狀物,有刺激性氣味逸出 |
(1)溶液“漸漸變黑”,說明濃硫酸具有 性。
(2)分析,甲認為是C2H4,乙認為不能排除SO2的作用。
①根據甲的觀點,使B中溶液褪色反應的化學方程式是 ;
②乙根據現象認為實驗中產生的SO2和 ,使B中有色物質反應褪色。
③為證實各自觀點,甲、乙重新實驗,設計與現象如下:
甲:在A、B間增加一個裝有某種試劑的洗氣瓶;現象:Br2的CCl4溶液褪色。
乙:用下列裝置按一定順序與A連接:(尾氣處理裝置略)

現象:C中溶液由紅棕色變為淺紅棕色時,E中溶液褪色。
請回答下列問題:
a.甲設計實驗中A、B間洗氣瓶中盛放的試劑是 ;乙設計的實驗D中盛放的試劑是 ,裝置連接順序為 。
b.能說明確實是SO2使E中溶液褪色的實驗是 。
c.乙為進一步驗證其觀點,取少量C中溶液,加入幾滴BaCl2溶液,振蕩,產生大量白色沉淀,淺紅棕色消失,發生反應的離子方程式是 。由此可得出的干燥的SO2不能使Br2的四氯化碳溶液褪色
Ⅱ、葡萄酒中常用Na2S2O5做抗氧化劑。
(3)0.5molNa2S2O5溶于水配成1L溶液,該溶液的pH=4.5。溶液中部分微粒濃度隨溶液酸堿性變化如圖所示。寫出Na2S2O5溶于水時發生的化學方程式 。

(4)已知:Ksp[BaSO4]=1×10-10,Ksp[BaSO3]=5×10-7。把部分被空氣氧化的該溶液的pH調為10,向溶液中滴加BaCl2溶液使SO42-沉淀完全[c(SO42-)≤1×10-5mol·L-1],此時溶液中c(SO32-)≤ mol·L-1。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】在一定溫度下的密閉容器中,可逆反應N2 + 3H2![]() 2NH3 達到平衡狀態的標志是
2NH3 達到平衡狀態的標志是
A. N2、H2、NH3在容器中共存
B. 混合氣體的總物質的量不再發生變化
C. 單位時間內生成n mol N2,同時生成3n mol H2
D. 單位時間內消耗n mol N2,同時消耗n mol NH3
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】(1)鑒別KCl溶液和K2CO3的試劑是____________,離子方程式為____________________。
(2)除去Na2CO3粉末中混入的NaHCO3雜質用______________________方法,化學方程式為_________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列依據熱化學方程式得出的結論正確的是
A. 等量固態硫燃燒比氣態硫燃燒放熱多
B. 已知2H2(g)+O2(g)![]() 2H2O(g) ΔH=-483.6 kJ·mol-1,則氫氣的燃燒熱為 241.8 kJ·mol-1
2H2O(g) ΔH=-483.6 kJ·mol-1,則氫氣的燃燒熱為 241.8 kJ·mol-1
C. 已知2C(s)+2O2(g)![]() 2CO2(g) ΔH=a 2C(s)+O2(g)
2CO2(g) ΔH=a 2C(s)+O2(g)![]() 2CO(g) ΔH=b,則a>b
2CO(g) ΔH=b,則a>b
D. 已知 NaOH(aq)+HCl(aq)![]() NaCl(aq)+H2O(l) ΔH=-57.3 kJ·mol-1,則含 40.0 g NaOH的稀溶液與稀醋酸完全中和,放出小于57.3 kJ 的熱量
NaCl(aq)+H2O(l) ΔH=-57.3 kJ·mol-1,則含 40.0 g NaOH的稀溶液與稀醋酸完全中和,放出小于57.3 kJ 的熱量
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】甲酸鈣廣泛用于食品、化工、石油等工業生產上,300~400℃左右分解。
Ⅰ、實驗室制取的方法之一是:Ca(OH)2+2HCHO + H2O2= Ca(HCOO)2+ 2H2O + H2↑實驗室制取時,將工業用氫氧化鈣和甲醛依次加入到質量分數為30-70%的過氧化氫溶液中(投料物質的量之比依次為1∶2∶1.2),最終可得到質量分數98%以上且重金屬含量極低的優質產品。
(1)反應溫度最好控制_______________(A.60℃左右 B. 200左右 C. 400℃左右),原因是_____________。
(2)制備時在混合溶液中要加入微量硼酸鈉抑制甲醛發生副反應外,還要加入少量的Na2S溶液,加硫化鈉的目的是 ____________________________。
(3)實驗時需強力攪拌45min,其目的是_________________。
(4)結束后需調節溶液呈堿性,其目的是__________________________。
Ⅱ、某研究性學習小組用工業碳酸鈣(主要成分為CaCO3;雜質為:Al2O3、FeCO3)為原料,先制備無機鈣鹽,再與甲酸鈉溶液混合制取甲酸鈣。結合如圖幾種物質的溶解度曲線及表中相關金屬離子生成氫氧化物沉淀的pH(開始沉淀的pH按金屬離子濃度為1.0 mol·L-1計算)。
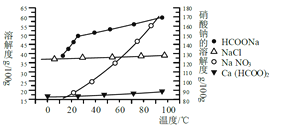
金屬離子 | 開始沉淀的pH | 沉淀完全的pH |
Fe3+ | 1. 1 | 3. 2 |
Al3+ | 3. 0 | 5. 0 |
Fe2+ | 5. 8 | 8. 8 |
請補充完整由碳酸鈣制備甲酸鈣晶體的實驗方案:稱取13.6g甲酸鈉溶于約20mL水,配成溶液待用,并稱取研細的碳酸鈣樣品10g待用,用__________溶解碳酸鈣樣品,調整溶液pH為5,過濾后,將濾液與甲酸鈉溶液混合,調整溶液為堿性;充分攪拌,所得溶液經__________、___________洗滌干燥得甲酸鈣晶體。(提供的試劑有:a.甲酸鈉,b.5mol·L-1硝酸,c. 5mol·L-1鹽酸,d. 5mol·L-1硫酸,e. 3%H2O2溶液,f.澄清石灰水)
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com