
【題目】目前低碳經濟已成為科學家研究的主要課題之一,如何降低大氣中![]() 的含量及有效地開發利用
的含量及有效地開發利用![]() ,引起全世界的關注:
,引起全世界的關注:
(1)用電弧法合成的儲氫材料常伴有大量的碳納米顆粒![]() 雜質
雜質![]() ,這些雜質顆粒通常用硫酸酸化的錳酸鉀氧化除去,在反應中,雜質碳被氧化為無污染氣體而除去,Mn元素轉變為
,這些雜質顆粒通常用硫酸酸化的錳酸鉀氧化除去,在反應中,雜質碳被氧化為無污染氣體而除去,Mn元素轉變為![]() ,請寫出對應的化學方程式并配平: ______ ;
,請寫出對應的化學方程式并配平: ______ ;
(2)將不同量的![]() 和
和![]() 分別通入到體積為2L的恒容密閉容器中,進行反應
分別通入到體積為2L的恒容密閉容器中,進行反應![]()
![]() ,得到如下兩組數據:
,得到如下兩組數據:
實驗組 | 溫度 | 起始量 | 平衡量 | 達到平衡所 需時間 | ||
| CO |
| CO | |||
1 | 650 | 2 | 4 |
|
| 5 |
2 | 900 | 1 | 2 |
|
| 3 |
①實驗2條件下平衡時![]() 體積分數為 ______ ;
體積分數為 ______ ;
②下列方法中可以證明上述已達平衡狀態的是 ______ ;
![]() 單位時間內生成nmol
單位時間內生成nmol![]() 的同時生成nmolCO
的同時生成nmolCO
![]() 容器內壓強不再變化
容器內壓強不再變化![]() 混合氣體密度不再變化
混合氣體密度不再變化
![]() 混合氣體的平均相對分子質量不再變化
混合氣體的平均相對分子質量不再變化![]() 的質量分數不再變化
的質量分數不再變化
③已知碳的氣化反應在不同溫度下平衡常數的對數值![]() 如下表,則反應
如下表,則反應![]() ,在900K時,該反應平衡常數的對數值
,在900K時,該反應平衡常數的對數值![]() ______ .
______ .
氣化反應式 | lgK | ||
700K | 900K | 1200K | |
|
|
|
|
|
|
|
|
(3)在高溫下一氧化碳可將二氧化硫還原為單質硫.已知:
![]()
![]()
![]()
![]()
![]()
![]()
請寫出CO除![]() 的熱化學方程式 ______ .
的熱化學方程式 ______ .
(4)![]() 時,
時,![]() 和
和![]() 的溶度積常數分別是
的溶度積常數分別是![]() 和
和![]() ,某含有
,某含有![]() 沉淀的懸濁液中
沉淀的懸濁液中![]() ,如果加入等體積的
,如果加入等體積的![]() 溶液,若要產生
溶液,若要產生![]() 沉淀,加入
沉淀,加入![]() 溶液的物質的量濃度最小是 ______
溶液的物質的量濃度最小是 ______ ![]() .
.
(5)![]() 時,在
時,在![]() 醋酸中加入V
醋酸中加入V![]() 溶液,測得混合溶液的pH變化曲線如圖所示,下列說法正確的是 ______ .
溶液,測得混合溶液的pH變化曲線如圖所示,下列說法正確的是 ______ .

A.![]() 的
的![]() 溶液和
溶液和![]() 的
的![]() 溶液中,由水電離出的
溶液中,由水電離出的![]() 相等
相等
B.①點時![]() ,此時溶液中,
,此時溶液中,![]()
C.②點時,溶液中的![]()
D.③點時![]() ,此時溶液中
,此時溶液中![]()
(6)如圖是一種新型燃料電池,它以CO為燃料,一定比例的![]() 和
和![]() 熔融混合物為電解質,圖2是粗銅精煉的裝置圖,現用燃料電池為電進行粗銅的精煉實驗.回答下列問題:
熔融混合物為電解質,圖2是粗銅精煉的裝置圖,現用燃料電池為電進行粗銅的精煉實驗.回答下列問題:

①寫出A極發生的電極反應式 ______ ;
②要用燃料電池為電進行粗銅的精煉實驗,則B極應該與 ______ 極![]() 填“C”或“D”
填“C”或“D”![]() 相連.
相連.
【答案】![]()
![]() ae
ae ![]()
![]()
![]() BC
BC ![]() D
D
【解析】
(1)由題目信息可知,C與K2MnO4在硫酸條件下反應生成CO2、MnSO4、K2SO4與H2O,反應中K2MnO4中錳元素化合價降低4價,碳元素化合價升高4價,化合價升降最小公倍數為4,故K2MnO4前的系數是1,碳單質前的系數是1,再根據原子守恒配平;
(2)①根據氫氣物質的量計算消耗水的物質的量,再計算平衡時水的物質的量,反應前后氣體物質的量不變,則平衡時混合氣體總物質的量為3mol,進而計算平衡時水的體積分數;
②可逆反應到達平衡時,同種物質的正逆速率相等,各組分的濃度、含量不變,由此衍生的其它一些物理量不變,判斷平衡的物理量應隨反應的進行發生改變,該物理量由變化到不變化說明到達平衡;
③已知:Ⅰ.C(s)+H2O(g)=CO(g)+H2(g),令平衡常數為K1,
Ⅱ.C(s)+2H2O(g)=CO2(g)+2H2(g),令平衡常數為K2,
則ⅡⅠ可得:CO(g)+H2O(g)CO2(g)+H2(g),故該反應平衡常數K=![]() ;
;
(3)已知:①C(s)+O2(g)=CO2(g) △H1=393.5kJmol1
②CO2(g)+C(s)=2CO(g) △H2=+172.5kJmol1
③S(s)+O2(g)=SO2(g) △H3=296.0kJmol1
根據蓋斯定律,①②③可得:2CO(g)+SO2(g)=S(s)+2CO2(g);
(4)某含有BaCO3沉淀的懸濁液中c(CO32)=0.2mol/L,根據碳酸鋇溶度積計算溶液中c(Ba2+),如果加入等體積的Na2SO4溶液,計算混合后溶液中c(Ba2+),如溶液中生成BaSO4沉淀,則應在混合液中滿足c(Ba2+)×c(SO42)>1×1010,計算混合溶液轉化硫酸根最小濃度,原硫酸鈉溶液最小濃度為混合后溶液中硫酸根離子最小濃度2倍;
(5)A.CH3COOH溶液、CH3COONa溶液氫氧根離子均源于水的電離;
B.根據電荷守恒:c(Na+)+c(H+)=c(CH3COO)+c(OH);
C.溶液呈中性,再根據電荷守恒c(Na+)+c(H+)=c(CH3COO)+c(OH)判斷;
D.溶液呈堿性,此時溶液中鈉離子濃度為0.05mol/L,結合電荷守恒c(Na+)+c(H+)=c(CH3COO)+c(OH)判斷;
(6)①由圖可知,A極CO發生氧化反應,CO失去電子與碳酸根離子結合生成二氧化碳;
②原電池中A為負極,B為正極,電解粗銅的精煉,粗銅作陽極,連接電源正極,精銅作陰極,連接電源負極。
(1)由題目信息可知,C與K2MnO4在硫酸條件下反應生成CO2、MnSO4、K2SO4與H2O,反應中K2MnO4中錳元素化合價降低4價,碳元素化合價升高4價,化合價升降最小公倍數為4,故K2MnO4前的系數是![]() ,故答案為:
,故答案為:![]() ;
;
(2)①實驗2條件下平衡時生成氫氣為0.4mol,由方程式可知消耗水為0.4mol,則平衡時水的物質的量為1mol0.4mol=0.6mol,反應前后氣體物質的量不變,則平衡時混合氣體總物質的量為3mol,故平衡時水的體積分數為![]() ×100%=20%,故答案為:20%;
×100%=20%,故答案為:20%;
②a.單位時間內生成n mol H2的同時生成n mol CO,生成的氫氣與消耗氫氣相等,反應到達平衡,故a正確;
b.反應前后氣體物質的量不變,恒溫恒容下,容器內壓強始終不變化,故b錯誤;
c.混合氣體總質量不變,容器容積不變,混合氣體密度為定值,故c錯誤;
d.混合氣體總質量不變,反應前后氣體物質的量不變,混合氣體的平均相對分子質量始終不變,故d錯誤;
e.隨反應進行二氧化碳質量增大,其質量分數增大,CO2的質量分數不再變化說明到達平衡,故e正確;
故答案為:ae;
③已知:Ⅰ.C(s)+H2O(g)=CO(g)+H2(g),令平衡常數為K1,
Ⅱ.C(s)+2H2O(g)=CO2(g)+2H2(g),令平衡常數為K2,
則ⅡⅠ可得:CO(g)+H2O(g)CO2(g)+H2(g),故該反應平衡常數K=![]() ,故lgK=lgK2lgK1=0.03(0.39)=0.36,故答案為:0.36;
,故lgK=lgK2lgK1=0.03(0.39)=0.36,故答案為:0.36;
(3)已知:已知:①C(s)+O2(g)=CO2(g) △H1=393.5kJmol1
②CO2(g)+C(s)=2CO(g) △H2=+172.5kJmol1
③S(s)+O2(g)=SO2(g) △H3=296.0kJmol1
根據蓋斯定律,①②③可得:2CO(g)+SO2(g)=S(s)+2CO2(g) △H=270kJmol1;
故答案為:2CO(g)+SO2(g)=S(s)+2CO2(g) △H=270kJmol1;
(4)某含有BaCO3沉淀的懸濁液中c(CO32)=0.2mol/L,溶液中c(Ba2+)=![]() mol/L=4×108mol/L,如果加入等體積的Na2SO4溶液,此時溶液中c(Ba2+)=2×108mol/L,如溶液中生成BaSO4沉淀,則應在混合液中滿足c(Ba2+)×c(SO42)>1×1010,則c(SO42)>
mol/L=4×108mol/L,如果加入等體積的Na2SO4溶液,此時溶液中c(Ba2+)=2×108mol/L,如溶液中生成BaSO4沉淀,則應在混合液中滿足c(Ba2+)×c(SO42)>1×1010,則c(SO42)>![]() mol/L=5×103mol/L,則加入Na2SO4溶液的物質的量濃度最小是2×5×103mol/L=0.01mol/L;故答案為:0.01;
mol/L=5×103mol/L,則加入Na2SO4溶液的物質的量濃度最小是2×5×103mol/L=0.01mol/L;故答案為:0.01;
(5)A.pH=3的CH3COOH溶液中氫氧根離子源于水電離,濃度為1010mol/L,為pH=11的CH3COONa溶液中,氫氧根離子也源于水的電離,溶液中氫氧根離子濃度為103mol/L,故錯誤;
B.①點時pH=6,此時溶液中c(H+)=106mol/L,c(OH)=108mol/L,由電荷守恒:c(Na+)+c(H+)=c(CH3COO)+c(OH),則c(CH3COO)c(Na+)=c(H+)c(OH)=106mol/L108mol/L=9.9×107mol/L,故B正確;
C.②點時溶液pH=7,則c(H+)=c(OH),根據電荷守恒:c(Na+)+c(H+)=c(CH3COO)+c(OH),故溶液中的c(CH3COO)=c(Na+),故C正確;
D.③點時V=20mL,溶液呈堿性,則c(H+)<c(OH),根據電荷守恒:c(Na+)+c(H+)=c(CH3COO)+c(OH),故溶液中的c(CH3COO)<c(Na+),此時c(Na+)=0.05mol/L,故D錯誤;
故答案為:BC;
(6)①由圖可知,A極CO發生氧化反應,CO失去電子與碳酸根離子結合生成二氧化碳,電極反應式為:CO2e+CO32=2CO2;故答案為:CO2e+CO32=2CO2;
②原電池中A為負極,B為正極,電解粗銅的精煉,粗銅作陽極,連接電源正極,精銅作陰極,連接電源負極,故B極應該與D極相連;故答案為:D。


科目:高中化學 來源: 題型:
【題目】反應①Fe(s)+CO2(g) ![]() FeO(s)+CO(g) △H1=a kJ/mol;
FeO(s)+CO(g) △H1=a kJ/mol;
②CO(g)+1/2O2(g) ![]() CO2(g) △H2=b kJ/mol
CO2(g) △H2=b kJ/mol
測得在不同溫度下,反應①的平衡常數 K 值隨溫度的變化如下:
![]()
(1)若 500℃時進行反應①,CO2起始濃度為 2 mol·L-1,CO2的平衡濃度為____________。
(2)反應①中的 a_____________0(填“大于”“小于”或“等于”)。
(3)700℃反應已經①達到平衡,要使該平衡正向移動,其他條件不變時,可以采取的措施有_____________(填序號)
A.縮小反應器體積 B.通入 CO2
C.升高溫度到 900℃ D.使用合適的催化劑
(4)下列圖像符合反應①的是_____(填序號)(圖中 v是速率、Φ為混合物中 CO2含量, T 為溫度且 T1> T2)
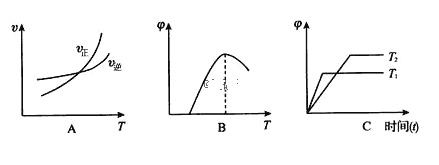
(5) 2Fe(s)+O2(g) ![]() 2FeO(s) △H3,該反應的△H3= ________kJ/mol。(用含 a、b的代數式表示)
2FeO(s) △H3,該反應的△H3= ________kJ/mol。(用含 a、b的代數式表示)
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】醋酸是一種常見的弱酸,在0.1mol·L﹣1醋酸中加入下列物質,醋酸的電離平衡及平衡時物質的濃度的變化:(填“正向”、“逆向”或“不移動”, “增大”、“減小”或“不變”, 填“>”、“<”或“=”)
(1)向醋酸中加入醋酸鈉固體,電離平衡向___________移動;pH __________
(2)向醋酸中加入碳酸鈣固體,電離平衡向________移動;c(CH3COOH)_________.
(3)向醋酸中加入大量的水,c(OH-)_________.導電能力__________.
(4)體積相同、物質的量濃度均為0.1 mol·L-1的①鹽酸、②醋酸兩種溶液,pH:①_____②;與完全相同的鎂條發生反應,開始時的反應速率:①______ ②;中和等量NaOH時消耗的體積:①______②;與足量的Zn反應生成H2的物質的量:①_______②。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】X、Y、Z、W均為短周期主族元素,它們在周期表中的相對位置如圖所示,下列說法中不正確的是( )

A.W的含氧酸的酸性比Z的強
B.Y的價層電子排布式可能是ns2np4
C.X、Z、W的最高價氧化物所對應的水化物可能都是強酸
D.四種元素所形成的氫化物中,沸點最高的可能是Y的氫化物
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列圖示與對應的敘述相符的是
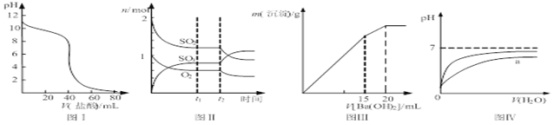
A. 圖Ⅰ表示鹽酸滴加到0.1 mol/L某堿溶液得到的滴定曲線,用已知濃度鹽酸滴定未知濃度該堿時最好選取酚酞作指示劑
B. 圖Ⅱ表示一定條件下進行的反應2SO2+O2![]() 2SO3 各成分的物質的量變化,t2時刻改變的條件可能是縮小容器體積
2SO3 各成分的物質的量變化,t2時刻改變的條件可能是縮小容器體積
C. 圖Ⅲ表示某明礬溶液中加入Ba(OH)2溶液,沉淀的質量與加入Ba(OH)2溶液體積的關系,在加入20 mL Ba(OH)2 溶液時鋁離子恰好沉淀完全
D. 圖Ⅳ表示pH相同的鹽酸與醋酸中分別加入水后溶液pH的變化,其中曲線a對應的是鹽酸
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】二茂鐵[(C5H5)2Fe]分子是一種金屬有機配合物,是燃料油的添加劑,用以提高燃燒的效率和去煙,可作為導彈和衛星的涂料等。它的結構如圖所示,下列說法不正確的是( )

A.二茂鐵分子中存在π鍵
B.lmol環戊二烯(![]() )中含有σ鍵的數目為11NA
)中含有σ鍵的數目為11NA
C.Fe2+的電子排布式為ls 22s 22p63s23p63d54s1
D.二茂鐵中Fe2+與環戊二烯離子(C5H5-)之間為配位鍵
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列說法或表示不正確的是( )
A.等質量的硫蒸氣和硫固體分別完全燃燒,前者放出的熱量多
B.C(金剛石,s)=C(石墨,s) △H=-1.19kJ·mol-1,所以石墨比金剛石穩定
C.含1mol H2SO4的濃硫酸與足量的NaOH溶液反應,放出熱量為57.3kJ
D.在101 kPa下,2 g H2 完全燃燒生成液態水放出285.8kJ熱量,其熱化學方程式為H2(g)+![]() O2
O2![]() H2O(l) △H=-285.8kJ·mol-1
H2O(l) △H=-285.8kJ·mol-1
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】在一定溫度下的定容密閉容器中進行反應:A(s)+2B(g)![]() C(g)+D(g),不能說明該反應已達到化學平衡的是
C(g)+D(g),不能說明該反應已達到化學平衡的是
A.B的體積分數不隨時間變化而變化
B.壓強不隨時間變化而變化
C.混合氣體的密度不再發生改變
D.單位時間內生成n mol A,同時生成n molC
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com