
【題目】我國某科研團隊以N2為原料合成了超高含能材料聚合氮——以氮氮單鍵(N-N)結合的具有網狀結構的聚合體。有關化學鍵的鍵能數據如下:
化學鍵 | N≡N | N=N | N-N |
鍵能/(kJ/mol) | 946 | 419 | 159 |
下列分析不正確的是
A. 氮原子的結構示意圖:![]() B. 聚合氮轉變為N2會釋放能量
B. 聚合氮轉變為N2會釋放能量
C. 高溫有利于聚合氮的合成 D. 低壓有利于聚合氮的合成
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小學生10分鐘應用題系列答案
小學生10分鐘應用題系列答案科目:高中化學 來源: 題型:
【題目】N2O5是一種新型硝化劑,在一定溫度下可發生以下反應:2N2O5(g) ![]() 4NO2(g)+O2(g)△H>0,T1溫度時,向密閉容器中通入N2O5,部分實驗數據見下表:
4NO2(g)+O2(g)△H>0,T1溫度時,向密閉容器中通入N2O5,部分實驗數據見下表:
時間/s | 0 | 500 | 1000 | 1500 |
c(N2O5)mol/L | 5.00 | 3.53 | 2.50 | 2.50 |
下列說法中不正確的是:
A. T1溫度下,500s時O2的濃度為0.74mol/L
B. 平衡后其他件不變,將容器的體積壓縮到原來的1/2,則再平衡時c(N2O5)>5.00 mol/L
C. T1溫度下的平衡常數為K1,T2溫度下的平衡常數為K2,若T1>T2,則K1<K2
D. T1溫度下的平衡常數為K1=125,平衡時N2O5的轉化率為0.5
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】有機物W在工業上常用作溶劑和香料,其合成方法如下:

下列說法正確的是
A. M、N、W均能發生加成反應、取代反應
B. N、W組成上相差一個CH2原子團,所以互為同系物
C. W屬于脂肪,能發生皂化反應
D. M的二氯代物有8種
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】把金屬A放入鹽B(NO3)2的溶液中,發生如下反應:A+B2+=A2++B,以下敘述正確的是( )
A.常溫下金屬A一定能與水反應,B一定不能與水反應
B.A與B用導線連接后放入酒精中,一定形成原電池
C.A、B用導線連接后放入B(NO3)2的溶液中,一定有電流產生
D.由A與B形成的原電池,A一定是正極,B一定是負極
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】金屬是不可再生的資源,通過回收廢舊的鋰電池提取鋰、鋁、鈷等重要的金屬具有重大的意義。已知鋰電池的正極材料為LiCoO2、炭黑、鋁箔及有機粘合劑,下面是回收的工藝流程:

(1)濾液X中通入過量CO2時發生的主要反應的離子方程式為___________
(2)寫出酸浸時加入H2SO4、H2O2反應的化學方程式______________________
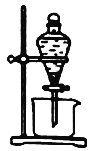
(3)實驗室中萃取分離CoSO4、Li2SO4溶液時需要加入有機物W,若實驗過程中使用如圖裝置,則該裝置中存在的主要錯誤有______________________
(4)已知部分物質的溶解度(g/100gH2O)情況如下表所示:
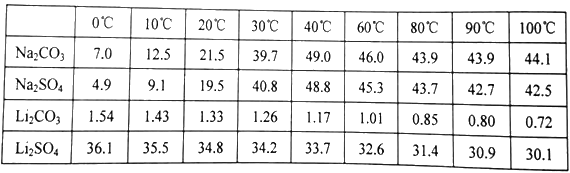
寫出濃縮后的溶液中加入飽和碳酸鈉溶液的離子反應方程式______________________;為提高Li2CO3的產率,最后過濾實驗中需要注意的問題是______________________
(5)若廢舊的鋰電池拆解后先使用酸溶解,最終也可以得到Al(OH)3、CoSO4、Li2CO3。在酸浸中若Al3+濃度為0.1moL·L-1,則常溫時pH>______________________才能夠開始形成氫氧化鋁沉淀(已知氫氧化鋁Ksp=1.3×10-33、lg4.26=0.6、![]() =2.35)
=2.35)
(6)已知100g廢舊的鋰電池中鈷酸鋰(LiCoO2)的含量為9.8%,若按照上述生產流程,可以生成2.4gLi2CO3,則其產率為______________________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】為驗證木炭可和濃硫酸反應生成的氣體產物,選用下圖中的儀器(含所盛物質)組裝成套實驗裝置,回答下列問題。

(1)在實驗進行中,按氣流方向從左到右的順序,導管口的三處連接應該是接___,__接__,__接__。
(2)D中右邊試管的作用是_____________________。
(3)試管B、C中各有什么現象,才能表示已檢驗出二氧化碳?__________。
(4)試管D中能否用飽和NaHCO3溶液代替酸性KMnO4溶液?說明理由:________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】向20 mL 0.40 mol/L H2O2溶液中加入少量KI溶液:ⅰ.H2O2+I-=H2O+IO﹣;ⅱ.H2O2+IO﹣= H2O+O2↑+ I﹣。H2O2分解反應過程中能量變化和不同時刻測得生成O2的體積(已折算標準狀況)如下。

t/min | 0 | 5 | 10 | 15 | 20 |
V(O2)/mL | 0.0 | 12.6 | 20.16 | 28.0 | 32.7 |
下列判斷不正確的是
A. 從圖中可以看出,KI能增大H2O2的分解速率
B. 反應ⅰ是放熱反應,反應ⅱ是吸熱反應
C. 0~10 min的平均反應速率:v(H2O2)≈9.0×10-3 mol/(L·min)
D. H2O2在反應過程中既體現了氧化性,又體現了還原性
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】高分子化合物G是一種重要的化工產品,可由烴A(C3H6)和苯合成。合成G的流程圖如下:

已知:①B和C中核磁共振氫譜分別有4種和3種峰。
②CH3Cl+NaCN→CH3CN+NaCl
③CH3CN![]() CH3COOH
CH3COOH
④![]()
請回答下列問題:
(1)A的名稱是___________。
(2)①的反應類型是___________,⑥的反應類型是___________。
(3)D的結構簡式是______________________。
(4)E中官能團的名稱是___________。
(5)⑦的反應方程式是_________________________________。
(6)F的同分異構體有多種,符合下列條件的有___________種。
①苯環對位上有兩個取代基,其中一個是NH2 ②能水解 ③核磁振譜有5個峰
寫出符合上述條件的一種同分異構體的結構簡式______________________。
(7)參照上述流程圖,寫出用乙烯、NaCN為原料制備聚酯 的合成路線___________(其它無機物任選)
的合成路線___________(其它無機物任選)
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com