
【題目】已知A、B、C、D、E是短周期的5種元素,它們的原子序數依次增大。A元素原子形成的離子核外電子數為零;C、D、E三種元素的最高價氧化物對應水化物之間可以兩兩反應;A與C同主族;B與E同主族;E的單質為黃色晶體,易溶于二硫化碳。
(1)請寫出B、D元素的名稱:B______________,D______________。
(2)畫出C元素的離子結構示意圖_____________________________。
(3)寫出D的單質與C的最高價氧化物對應水化物之間反應的離子方程式_________。
(4)A、B、C三種元素形成的化合物為_____________________, 所含的化學鍵類型為_______________________。
(5)B、C、D三種元素的離子半徑由大到小的排列順序為__________________(用離子符號表示)。
【答案】氧 鋁 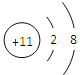 2Al + 2OH-+ 2H2O=2AlO2-+ 3H2↑ NaOH 離子鍵、共價鍵 O2->Na+>Al3+
2Al + 2OH-+ 2H2O=2AlO2-+ 3H2↑ NaOH 離子鍵、共價鍵 O2->Na+>Al3+
【解析】
A、B、C、D、E是短周期的5種元素,它們的原子序數依次增大。A元素原子形成的離子核外電子數為零,A為H;C、D、E三種元素的最高價氧化物對應水化物之間可以兩兩反應;A與C同主族,C是Na,D是Al;B與E同主族;E的單質為黃色晶體,易溶于二硫化碳,E是S,所以B是O。據此解答。
(1)B、D元素的名稱分別是氧、鋁。
(2)C是Na,Na元素的離子結構示意圖為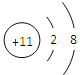 。
。
(3)D的單質Al與C的最高價氧化物對應水化物氫氧化鈉反應的離子方程式為2Al + 2OH-+ 2H2O=2AlO2-+ 3H2↑。
(4)A、B、C三種元素形成的化合物為NaOH,所含的化學鍵類型為離子鍵和共價鍵。
(5)B、C、D三種元素的離子均是10電子微粒,核電荷數越大,離子半徑越小,則離子半徑由大到小的排列順序為O2->Na+>Al3+。


科目:高中化學 來源: 題型:
【題目】2012年2月,江蘇鎮江自來水出現異味,引發鎮江及位于其下游的南通等地區發生居民搶購瓶裝飲用水的現象。經初步調查,韓國籍船舶“格洛里亞”號貨輪水下排放管道排出的苯酚是引起自來水異味的主要原因。請完成以下填空:
(1)苯酚與水混合,溶液變渾濁,向該渾濁液中滴加NaOH溶液,可觀察到的現象是____,向上述反應液中繼續通入過量CO2,又可觀察到的現象是____,則通入CO2時的反應為_____,說明苯酚具有_______性。
(2)A和B兩種物質的分子式都是C7H8O,它們都能跟金屬鈉反應放出氫氣。B能使適量溴水褪色,并產生白色沉淀,A不能。B苯環上的一溴代物有兩種。
①寫出A和B的結構簡式:A________,B_______________。
②寫出B與NaOH溶液反應的化學方程式:_______________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列有關說法正確的是( )
A.將![]() 通入酸性高錳酸鉀溶液,溶液褪色,體現
通入酸性高錳酸鉀溶液,溶液褪色,體現![]() 的還原性
的還原性
B.濃硫酸滴在白紙上,白紙變黑,體現了濃硫酸的吸水性
C.硅晶體具有半導體性能,可用于制造光導纖維
D.將![]() 為5.4的雨水樣品在空氣中放置一段時間后,測得
為5.4的雨水樣品在空氣中放置一段時間后,測得![]() 變小,是因為樣品吸收了空氣中的
變小,是因為樣品吸收了空氣中的![]()
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】已知常溫下二氯化二硫(S2 Cl2)為紅棕色液體,其結構式為Cl-S-S-Cl。其制備反應及與水反應的化學方程式如下:①CS2+3Cl2 ![]() CCl4+S2Cl2 ②2S2Cl2 +2H2O=4HCl+SO2↑+3S↓則下列說法正確的是 ( )
CCl4+S2Cl2 ②2S2Cl2 +2H2O=4HCl+SO2↑+3S↓則下列說法正確的是 ( )
A. 反應①中CS2作氧化劑
B. 反應②中S2Cl2既作氧化劑又作還原劑
C. 反應①中每生成1mol S2Cl2轉移4mol電子
D. 反應②中氧化產物與還原產物的物質的量之比為3:1
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】工業上利用CO和水蒸氣在一定條件下發生反應制取氫氣:
CO(g)+H2O(g)![]() CO2(g)+H2(g) △H=-41 kJ/mol
CO2(g)+H2(g) △H=-41 kJ/mol
某小組研究在相同溫度下該反應過程中的能量變化。他們分別在體積均為VL的兩個恒溫恒容密閉容器中加入一定量的反應物,使其在相同溫度下發生反應。相關數據如下:
容器編號 | 起始時各物質物質的量/mol | 達到平衡的時間/min | 達平衡時體系能量的變化/kJ | |||
CO | H2O | CO2 | H2 | |||
① | 1 | 4 | 0 | 0 | t1 | 放出熱量:32.8 kJ |
② | 2 | 8 | 0 | 0 | t2 | 放出熱量:Q |
(1)該反應過程中,反應物分子化學鍵斷裂時所吸收的總能量_____________(填“大于”、“小于”或“等于”)生成物分子化學鍵形成時所釋放的總能量。
(2)容器①中反應達平衡時,CO的轉化率為_____________。
(3)計算容器①中反應的平衡常數K=_____________。某時刻測得②中氫氣的物質的量為1.8mol,請問此刻V正 V逆(填大于,小于或等于)
(4)下列敘述正確的是_____________(填字母序號)。
a.平衡時,兩容器中H2的體積分數相等
b.容器②中反應達平衡狀態時,Q > 65.6 kJ
c.反應開始時,兩容器中反應的化學反應速率相等
d.平衡時,兩容器中CO的轉化率相同
(5)已知:2H2(g)+O2(g)=2H2O(g)ΔH=-484kJ/mol,請寫出CO完全燃燒生成CO2的熱化學方程式: 。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】⑴在①NaCl、②NaOH、③N2、④H2S、⑤Na2O2中,只含有離子鍵的是________,只含有極性鍵的是______,既含離子鍵又含非極性共價鍵的是____。
(2)寫出下列物質的電子式:
CO2____________NaCl____________ HClO_______________
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】掌握儀器名稱、組裝及使用方法是中學化學實驗的基礎,如圖為兩套實驗裝置。
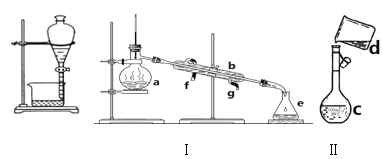
(1)寫出下列儀器的名稱:a.___,b.___,c.___,d.___。
(2)若利用裝置I分離四氯化碳和酒精的混合物,還缺少的儀器是___,冷凝水由___(填f或g)口通入。
(3)現需配制0.25mol/LNaOH溶液450mL,裝置II是某同學轉移溶液的示意圖。
①圖中的錯誤是___。
②根據計算得知,需稱量NaOH的質量為___g。
③下列操作使配制的NaOH溶液濃度偏低的有____。
A.將砝碼放在左盤上,NaOH放在右盤上進行稱量(使用游碼)
B.選用的容量瓶內有少量蒸餾水
C.定容搖勻后,液面下降,又加水至刻度線
D.整個配制過程中,容量瓶不振蕩
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】某有機物的結構簡式如圖所示,下列說法正確的是( )
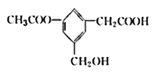
A. 分子中含有4種官能團
B. 1mol該物質可以和3molNaOH反應
C. 在水溶液中該有機物中的羥基和羧基均能電離出氫離子
D. 可發生加成反應、中和反應、水解反應、酯化反應、氧化反應和消去反應
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】有人設想合成具有以下結構的四種烴分子,下列有關說法不正確的是
![]() (b)、
(b)、![]() (d)、
(d)、![]() (p)
(p)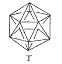
A.b、d和p互為同分異構體B.分子丁顯然是不可能合成的
C.b、d、p均可與酸性高錳酸鉀溶液反應D.b、d、p中只有b的所有原子處于同一平面
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com