
【題目】以黃鐵礦為原料制硫酸產生的硫酸渣中含Fe2O3、SiO2、Al2O3、CaO、MgO等。現(xiàn)以硫酸渣制備鐵紅(Fe2O3),過程如下:
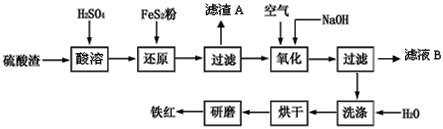
(1)酸溶過程中Fe2O3與稀硫酸反應的離子方程式是____。
(2)還原過程中加入FeS2是將溶液中的Fe3+ 還原為Fe2+,而本身被氧化為SO42-,寫出有關的離子方程式:_____。
(3)生產過程中,為了確保鐵紅的質量,氧化過程需要調節(jié)溶液的pH的范圍是__。
(部分陽離子以氫氧化物形式沉淀時溶液的pH見表)
沉淀物 | Fe(OH)3 | Al(OH)3 | Fe(OH)2 | Mg(OH)2 |
開始沉淀 | 2.7 | 3.8 | 7.5 | 9.4 |
完全沉淀 | 3.2 | 5.2 | 9.7 | 12.4 |
(二)把NaOH、MgCl2、AlCl3三種固體組成的混合物溶于足量水后,產生1.16g白色沉淀,再向所得濁液中逐漸加入1.00mol/LHCl溶液,加入HCl溶液的體積與生成沉淀的關系如圖所示。
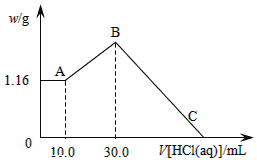
(1)原混合物中NaOH的質量是____g。
(2)C點(此時沉淀恰好完全溶解)HCl溶液的體積為___mL。
(三)二氧化氯(ClO2,黃綠色易溶于水的氣體)是高效、低毒的消毒劑。回答下列問題:
實驗室用NH4Cl、鹽酸、NaClO2(亞氯酸鈉)為原料,通過如圖1過程制備ClO2:
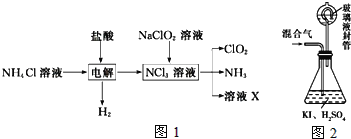
用如圖2裝置可以測定混合氣中ClO2的含量:
Ⅰ、在錐形瓶中加入足量的碘化鉀,用50mL水溶解后,再加入3mL稀硫酸;
Ⅱ、在玻璃液封裝置中加入水,使液面沒過玻璃液封管的管口;
Ⅲ、將一定量的混合氣體通入錐形瓶中吸收;
Ⅳ、將玻璃液封裝置中的水倒入錐形瓶中;
Ⅴ、用0.1000molL1硫代硫酸鈉標準溶液滴定錐形瓶中的溶液(I2+2S2O32-═2I+S4O62-),指示劑顯示終點時共用去20.00mL硫代硫酸鈉溶液。在此過程中:
①測得混合氣中ClO2的質量為___g。
②用ClO2處理過的飲用水會含有一定量的亞氯酸鹽。若要除去超標的亞氯酸鹽,下列物質最適宜的是___(填標號).
a.明礬 b.碘化鉀 c.鹽酸 d.硫酸亞鐵
【答案】Fe2O3+6H+=2Fe3++3H2O FeS2+14Fe3++8H2O=15Fe2++2SO42-+16H+ 3.2~3.8 5.20 130.0 0.02700 d
【解析】
硫酸渣中含Fe2O3、SiO2、Al2O3、MgO等,稀硫酸溶解主要除去不與酸反應的SiO2,加入FeS2將溶液中的Fe3+還原為Fe2+,再加氫氧化鈉和空氣,調節(jié)溶液的pH的范圍是3.2~3.8主要是使三價鐵沉淀,而二價鎂,三價鋁都不沉淀,最后洗滌、烘干、研磨使氫氧化鐵分解生成氧化鐵,從而得到鐵紅。
(1)氧化鐵與硫酸反應生成硫酸鐵和水,方程式為:Fe2O3+3H2SO4═Fe2(SO4) 3+3H2O;離子方程式為Fe2O3+6H+=2Fe3++3H2O,故答案為:Fe2O3+6H+=2Fe3+ +3H2O。
(2)FeS2中S元素的化合價從-1價升高到+6價,2個S原子轉移14個電子,Fe3+轉移1個電子,則二者的計量數(shù)之比為1:14,根據(jù)S守恒可知SO42-前面的化學計量數(shù)為2,根據(jù)氧守恒可知H20前面化學計量數(shù)為8,根據(jù)H守恒可知H+前化學計量數(shù)為16,則反應的離子方程式為:FeS2+14Fe3++8H2O═15Fe2++2SO42-+16H+,檢驗Fe3+被完全還原的實驗操作和現(xiàn)象為取少量試液于試管中,滴入幾滴KSCN溶液,若不顯紅色,則說明Fe3 +已被完全還原,故答案為:FeS2+14Fe3 + +8H2O=15Fe2++2SO42-+16H+。
(3)溶液pH>3.2時Fe3+沉淀完全,溶液pH=3.8時Al3+開始沉淀,故溶液的pH的范圍是3.2~3.8,根據(jù)幾種離子沉淀的pH,如果pH過大,Al3+、Mg2+形成沉淀,使制得的鐵紅不純;故答案為:3.2~3.8。
(二)A~B階段消耗鹽酸的物質的量=(0.03L-0.01L)×1.0mol/L=0.02mol,則根據(jù)方程式NaAlO2+HCl+H2O=Al(OH)3↓+NaCl可知生成氫氧化鋁的物質的量=0.02mol。所以根據(jù)原子守恒可知原混合物中氯化鋁的物質的量是0.02mol。B點沉淀達到最大值,此時的沉淀是氫氧化鎂和氫氧化鋁的混合物。而溶液則恰好是氯化鈉溶液。根據(jù)氯離子守恒可知氯化鈉的物質的量=0.03L×1.00mol/L+0.02mol×2+0.02mol×3=0.13mol。所以根據(jù)鈉離子守恒可知,氫氧化鈉的物質的量也是0.13mol,因此氫氧化鈉的質量m=n· M=40g/mol×0.13mol=5.2g。B~C階段加入的鹽酸開始溶解氫氧化鋁和氫氧化鎂,此時反應的方程式為Mg(OH)2+2HCl=MgCl2+2H2O;Al(OH)3+3HCl=AlCl3+3H2O。根據(jù)氫氧化鎂和氫氧化鋁均是0.02mol可知,該階段消耗鹽酸的物質的量是0.02mol×2+0.02mol×3=0.10mol,其體積是0.10mol÷1mol/L=0.1L=100mL,所以C點(此時沉淀恰好完全溶解)HCl溶液的體積為30mL+100mL=130.0mL,故答案為:130.0mL。
(三)①含有Na2S2O3物質的量為0.02L×0.1mol/L=0.002mol,則:
根據(jù)關系式:2ClO2~5I2~10Na2S2O3,
2 10
n(ClO2) 0.002mol
所以n(ClO2)=0.0004mol,所以m(ClO2)=0.0004 mol×67.5g/mol=0.02700g,故答案為:0.02700。
②若要除去超標的亞氯酸鹽,ac均不能還原亞氯酸鹽,b中KI具有還原性但氧化產物不適合飲用水使用,只有d中Fe2+將ClO2-還原成Cl-,Fe2+ 被氧化為鐵離子,且鐵離子水解生成膠體可凈化飲用水,則最適宜的是d,故答案為:d。


科目:高中化學 來源: 題型:
【題目】某化學興趣小組在實驗室中進行化學實驗,按如圖甲連接好線路發(fā)現(xiàn)燈泡不亮,按圖乙連接好線路發(fā)現(xiàn)燈泡亮,由此得出的結論正確的是( )

A.NaCl溶液是電解質
B.在通電的條件下,NaCl在水中電離出大量的離子而導電
C.NaCl固體中無陰陽離子,因此不能導電
D.同一溫度下,將乙中NaCl溶液換成等濃度的MgCl2溶液,溶液導電性增強
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】乙醇是制取飲料、香精、染料、涂料、洗滌劑等產品的原料.
完成下列填空:
(1)實驗室用乙醇制取乙烯時,濃硫酸的用量遠遠超過作為催化劑的正常用量,原因是______.
(2)驗證乙烯加成反應性質時,需對乙烯氣體中的干擾物質進行處理,可選用的試劑是______(填寫化學式);能確定乙烯通入溴水中發(fā)生了加成反應的事實是______.(選填編號)
a.溴水褪色 b.有油狀物質生成
c.反應后水溶液酸性增強 d.反應后水溶液接近中性
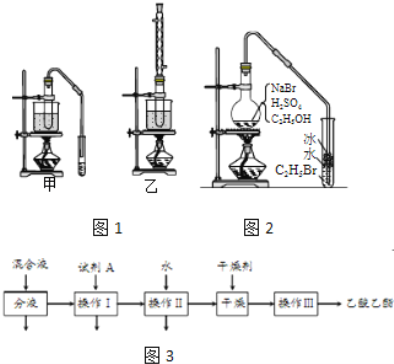
(3)實驗室用乙醇和乙酸制備乙酸乙酯時,甲乙兩套裝置如圖1都可以選用.關于這兩套裝置的說法正確的是______.(選填編號)
物質 | 沸點(℃) |
乙醇 | 78.5 |
乙酸 | 117.9 |
乙酸乙酯 | 77 |
a.甲裝置乙酸轉化率高 b.乙裝置乙酸轉化率高
c.甲裝置有冷凝回流措施 d.乙裝置有冷凝回流措施
(4)用乙裝置實驗時,提純乙中乙酸乙酯的流程如圖3,以上流程中試劑A的化學式是______;操作Ⅱ的名稱是______;操作Ⅲ一般適用于分離______混合物.
(5)如圖2是用乙醇制備溴乙烷的裝置,實驗中有兩種加料方案:
①先加溴化鈉→再加乙醇→最后加1:1濃硫酸;
②先加溴化鈉→再加1:1濃硫酸→最后加乙醇.
按方案①和②實驗時,產物都有明顯顏色,若在試管中加入______,產物可變?yōu)闊o色.與方案①相比較,方案②的明顯缺點是______.
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】已知A、B、D、E均為化學中的常見物質,它們之間的轉化關系如圖所示(部分產物略去),則下列有關物質的推斷不正確的是( )

A. 若A是鐵,則E可能為稀硝酸
B. 若A是CuO,E是碳,則B為CO
C. 若A是NaOH溶液,E是CO2,則B為NaHCO3
D. 若A是AlCl3溶液,E可能是氨水
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】圖是可逆反應A+2B![]() 2C+3D的化學反應速率與化學平衡隨外界條件改變(先降溫后加壓)而變化的情況,由此可推斷
2C+3D的化學反應速率與化學平衡隨外界條件改變(先降溫后加壓)而變化的情況,由此可推斷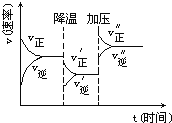
A. A、B、C、D均為氣體
B. 若A、B是氣體,則C、D是液體或固體
C. 溫度越高,K越大
D. 在整個過程中,A的轉化率一直增大
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】以Pt-g-C3N4為催化劑,用光催化氧化法脫除NO的過程如圖所示。
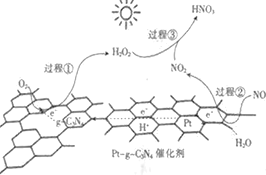
該脫除過程中,下列說法不正確的是
A. 該過程為太陽能轉化為化學能
B. Pt端發(fā)生的是氧化反應
C. 過程①發(fā)生的電極反應為H2O2-2e-=O2↑+2H+
D. 過生③的化學方程式為2NO2+H2O2=2HNO3
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】(1)對于反應2SiHCl3(g)===SiH2Cl2(g)+SiCl4(g),采用大孔弱堿性陰離子交換樹脂催化劑,在323 K和343 K時SiHCl3的轉化率隨時間變化的結果如圖所示。

①343 K時反應的平衡轉化率α=________%。平衡常數(shù)K343 K=________(保留2位小數(shù))。
②在343 K下:要提高SiHCl3轉化率,可采取的措施是________;要縮短反應達到平衡的時間,可采取的措施有________、________。
③比較a、b處反應速率大小:va________vb(填“大于”“小于”或“等于”)。反應速率v=v正-v逆=k正x2SiHCl3-k逆xSiH2Cl2xSiCl4,k正、k逆分別為正、逆向反應速率常數(shù),x為物質的量分數(shù),計算a處的v正/v逆=________(保留1位小數(shù))。
(2)不同溫度下水的離子積常數(shù)如表所示:
t/℃ | 0 | 10 | 20 | 25 | 40 | 50 | 100 |
Kw/10-14 | 0.114 | 0.292 | 0.681 | 1.01 | 2.92 | 5.47 | 55.0 |
①請用文字解釋隨溫度升高水的離子積增大的原因_______________;
②10℃時純水的電離平衡常數(shù)為_________;計算100℃時純水中電離產生的氫離子濃度為__________________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】如圖為發(fā)光二極管連接檸檬電池裝置,下列說法正確的是
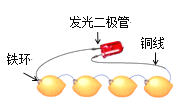
A. 鐵環(huán)作為檸檬電池的正極
B. 電子由發(fā)光二極管經導線流向Fe環(huán)
C. 負極的電極反應為:Fe-2 e-===Fe2+
D. 可將檸檬替換成盛裝酒精溶液的裝置
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】(1)利用I2O5可使CO與H2O(g)反應轉化為CO2和H2,從而有效減少大氣污染。該過程可通過圖1所示的兩步反應循環(huán)實現(xiàn)。
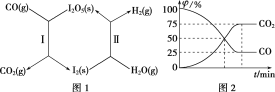
其中:反應Ⅰ為I2O5(s)+5CO(g)=I2(s)+5CO2(g) ΔH=a kJ·mol-1
反應Ⅱ中,生成1 mol H2(g)時,反應熱ΔH=b kJ·mol-1。
①總反應的熱化學方程式為(反應熱ΔH用含a、b的代數(shù)式表示)______。
②在恒溫密閉容器中加入一定量的CO(g)和I2O5(s),發(fā)生反應Ⅰ并達到平衡。測得體系中各氣體組分的體積分數(shù)φ隨時間t的變化如圖2所示。則此反應用氣體分壓表示的平衡常數(shù)Kp=______(已知:氣體分壓=氣體總壓×體積分數(shù))。
(2)已知鉛鹽中,Pb(NO3)2、(CH3COO)2Pb易溶于水,PbSO4、PbS難溶于水,室溫下其溶度積常數(shù)為Ksp(PbSO4)=1.06×10-8;Ksp(PbS)=3.40×10-28。
①將一定量的PbSO4加入足量飽和CH3COONH4溶液中,微熱,并不斷攪拌,因發(fā)生復分解反應,PbSO4緩慢溶解。能發(fā)生此復分解反應的原因是______。
②某溶液中主要含有S2-、SO42-等陰離子,向其中滴加Pb(NO3)2溶液,當PbSO4開始析出時,溶液中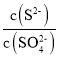 =________。
=________。
(3)鈦基二氧化鉛(Ti/PbO2)是重要的電極材料,工業(yè)上用電解法制作,主要流程如圖:
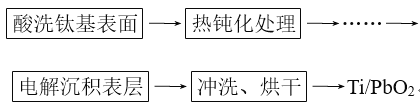
其中“電解沉積表層”是制作的關鍵,方法是電解可溶性鉛鹽溶液,使生成的PbO2沉積在陽極金屬鈦(Ti)上。主反應為2Pb2++2H2O=Pb+PbO2+4H+。
①必須預先將陽極金屬鈦進行“熱鈍化處理”,原因是_______。
②電解槽中,陽極主要的反應式為___;該法的缺點是陽極、陰極均會發(fā)生副反應。其中陰極上產生的氣體副產物是____。
③電解法制得的PbO2晶體中含有少量的+2價鉛,從而導致氧原子所在位置出現(xiàn)少量“空穴”(即化學式為PbOx,但x<2)。若電解時每生成1molPbOx轉移1.94NA個e-(NA為阿伏加德羅常數(shù)的值),則鉛元素中+2價鉛所占的質量分數(shù)為____。
查看答案和解析>>
國際學校優(yōu)選 - 練習冊列表 - 試題列表
湖北省互聯(lián)網違法和不良信息舉報平臺 | 網上有害信息舉報專區(qū) | 電信詐騙舉報專區(qū) | 涉歷史虛無主義有害信息舉報專區(qū) | 涉企侵權舉報專區(qū)
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com