
【題目】下列關于碳和碳的化合物的結構和性質中
(1)和碳同一主族的硅原子中能量最高的電子處在______電子層上(填寫電子層符號),最外層有___種運動狀態不同的電子,碳原子核外有______種能量不同的電子,有______種不同形狀的電子云.
(2)1個C原子的單鍵氫化物分子是CH4,2個C原子的單鍵氫化物分子則為C2H6.以下各對分子間不存在類似關系的是_________
A.NH3與N2H4 B.H2O與H2O2 C.SF6與S2F10 D.SCl4與S2Cl2
(3)金剛石的熔點低于石墨,原因可能是________
A.石墨中還有范德華力
B.石墨熔化也要破壞共價鍵,且鍵長更短
C.石墨熱穩定性更好
(4)已知常溫下,H2CO3:Ki1=4.3x10﹣7、Ki2=5.6x10﹣11.結合H+的能力Na2CO3溶液______(填”>”、”<”或“=”)NaHCO3溶液,設計簡單實驗證明:______.
(5)在1L 0.3mol/L的NaOH溶液中,通入4.48LCO2(標準狀況),反應后所得溶液中離子的濃度之間有一些等量關系,例如:.c(Na+)+c(H+)=c(HCO3﹣)+2c(CO32﹣)+c(OH﹣),另外對此溶液中存在的離子按濃度由大到小排序為______.
【答案】M 4 3 2 D B > 取等濃度等體積的NaHCO3和Na2CO3溶液混于同一燒杯中,加入稀鹽酸,邊滴邊攪拌,若一段時間無氣泡,則Na2CO3結合H+能力強 c(Na+)>c(HCO3﹣)>c(CO32﹣)>c(OH﹣)>c(H+)
【解析】
(1)離核越遠電子的能量越高,Si原子最外層含有4個電子;碳原子核外電子填充在三個軌道內,s軌道為球形,p軌道為紡錘形;
(2)根據兩個中心原子形成一條共價單鍵,相應的減少2個H或F或Cl原子分析,2個中心原子結合的原子(H、F、Cl)數等于一個中心原子的2倍﹣2;
(3)石墨與金剛石在熔化時破壞共價鍵,共價鍵鍵長越短,鍵能越大,共價鍵越穩定,熔點越高,據此分析;
(4)電解質越弱,其相應的陰離子結合質子能力越強,常溫下,H2CO3:Ki1=4.3x10﹣7>Ki2=5.6x10﹣11,電離強弱順序是碳酸的一級電離大于其二級電離,即結合H+的能力Na2CO3溶液大于NaHCO3溶液,根據同濃度的兩溶液與鹽酸反應生成氣體的速率進行設計實驗證明;
(5)n (CO2)=![]() =0.2mol、n(NaOH)=0.3mol/L×1L=0.3mol,則反應的可能方程式有:CO2+2NaOH=Na2CO3+H2O,CO2+NaOH=NaHCO3,由于2>
=0.2mol、n(NaOH)=0.3mol/L×1L=0.3mol,則反應的可能方程式有:CO2+2NaOH=Na2CO3+H2O,CO2+NaOH=NaHCO3,由于2>![]() =
=![]() >1,所以反應后產物為Na2CO3和NaHCO3,設所得產物中含Na2CO3為xmol,NaHCO3為ymol,則:x+y=0.1、2x+y=0.3,解得:x=0.1、y=0.1,在含等物質的量的碳酸鈉、碳酸氫鈉的溶液中,碳酸根離子水解大于碳酸氫根離子的水解,水解使溶液顯堿性,以此來解答。
>1,所以反應后產物為Na2CO3和NaHCO3,設所得產物中含Na2CO3為xmol,NaHCO3為ymol,則:x+y=0.1、2x+y=0.3,解得:x=0.1、y=0.1,在含等物質的量的碳酸鈉、碳酸氫鈉的溶液中,碳酸根離子水解大于碳酸氫根離子的水解,水解使溶液顯堿性,以此來解答。
(1)離核越遠電子的能量越高,Si原子核外電子分三層排布,最外層為M層,則能量最高的電子處在M層上,Si原子最外層含有4個電子,4個電子的運動狀態均不同,所以最外層有4種運動狀態不同的電子;碳原子核外電子填充在三個軌道內,三個軌道上的電子各不相同,所以碳原子核外有3種能量不同的電子,s軌道為球形,p軌道為紡錘形,則有2種不同形狀的電子云;
(2)A.每個N原子能形成3條單鍵,兩個N原子形成N﹣N,氫原子減少2個,2×3﹣2=4,故A正確;
B.一個O原子形成兩條單鍵,兩個O原子形成O﹣O單鍵,氫原子減少2個,2×2﹣2=2,故B正確;
C.一個S原子形成6條單鍵,兩個S原子形成了S﹣S單鍵,F原子減少2個,2×6﹣2=10,故C正確;
D.在SCl4中一個S原子形成4條單鍵,2×4﹣2=6,兩個S形成S﹣S單鍵所得到的分子式應為S2Cl6,故D錯誤;
答案選D;
(3)石墨與金剛石在熔化時破壞共價鍵,共價鍵鍵長越短,鍵能越大,共價鍵越穩定,熔點越高,石墨中共價鍵的鍵長比金剛石中共價鍵鍵長短,鍵能更大,所以石墨的熔點比金剛石的高,故答案選B;
(4)電解質越弱,其相應的陰離子結合質子能力越強,常溫下,H2CO3:Ki1=4.3x10﹣7>Ki2=5.6x10﹣11,電離強弱順序是:碳酸的一級電離大于其二級電離,即結合H+的能力Na2CO3溶液大于NaHCO3溶液,取等濃度等體積的NaHCO3和Na2CO3溶液混于同一燒杯中,加入稀鹽酸,邊滴邊攪拌,若一段時間無氣泡,則Na2CO3結合H+能力強;
(5)n (CO2)=![]() =0.2mol、n(NaOH)=0.3mol/L×1L=0.3mol,則反應的可能方程式有:CO2+2NaOH=Na2CO3+H2O,CO2+NaOH=NaHCO3,根據2>
=0.2mol、n(NaOH)=0.3mol/L×1L=0.3mol,則反應的可能方程式有:CO2+2NaOH=Na2CO3+H2O,CO2+NaOH=NaHCO3,根據2>![]() =
=>1可知反應后產物為:Na2CO3和NaHCO3,設所得產物中含Na2CO3為xmol,NaHCO3為ymol,則:x+y=0.1、2x+y=0.3解得:x=0.1、y=0.1,在含等物質的量的碳酸鈉、碳酸氫鈉的溶液中,c(Na+)最大,碳酸根離子水解大于碳酸氫根離子的水解,則c(HCO3﹣)>c(CO32﹣),水解使溶液顯堿性,則c(OH﹣)>c(H+),顯性離子大于隱性離子,則:c(HCO3﹣)>c(CO32﹣)>c(OH﹣)>c(H+),所以離子濃度大小為:c(Na+)>c(HCO3﹣)>c(CO32﹣)>c(OH﹣)>c(H+)。


 閱讀快車系列答案
閱讀快車系列答案科目:高中化學 來源: 題型:
【題目】工業冶煉鈦的第一步反應為:TiO2(s)+2C(s)+2Cl2![]() TiCl4(g)+2CO。下列關于該反應的說法正確的是( )
TiCl4(g)+2CO。下列關于該反應的說法正確的是( )
A.TiCl4既是氧化產物又是還原產物
B.氧化劑與還原劑的物質的量之比為1:1
C.當轉移電子數目為0.2NA時,氣體體積增大1.12L
D.當有26g固體參加反應時,轉移電子數目為NA
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】高溫、催化劑條件下,某反應達到平衡,平衡常數K=![]() 恒容時,溫度升高,H2濃度減小.下列說法正確的是( )
恒容時,溫度升高,H2濃度減小.下列說法正確的是( )
A. 該反應的焓變為負值
B. 2CO2(g)+2H2(g)2CO(g)+2H2O(g) 的平衡常數K1=K2
C. 升高溫度,正反應速率增大,逆反應速率減小,平衡正向移動
D. 若恒容、恒溫下充入CO,則K值變大
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】寫出或完成下列熱化學方程式。
(1)0.5molCH4完全燃燒生成CO2和液態水時,放出445kJ 的熱量。寫出CH4燃燒的熱化學方程式__________。
(2)通常人們把拆開1mol某化學鍵吸收的能量看成該化學鍵的鍵能。下表是一些化學鍵的鍵能。
化學鍵 | C-H | C-F | H-F | F-F |
鍵能kJ/mol | 414 | 489 | 565 | 155 |
根據鍵能數據估算下列反應:CH4(g) + 4F2(g)=CF4(g) + 4HF(g)的反應熱△H為_____。
(3)1840年瑞士的化學家蓋斯(Hess)在總結大量實驗事實(熱化學實驗數據)的基礎上提出:“定壓或定容條件下的任意化學反應,在不做其它功時,不論是一步完成的還是幾步完成的,其熱效應總是相同的(反應熱的總值相等)。”
已知:Fe2O3(s)+3CO(g)=2Fe(s)+3CO2(g) ΔH1
3Fe2O3(s)+CO(g)=2Fe3O4(s)+CO2(g) ΔH2
Fe3O4(s)+CO(g)=3FeO(s)+CO2(g) ΔH3
請寫出CO還原FeO的熱化學方程式:______。
(4)在101KP下,1g氫氣完全燃燒生成液態水放出142.9kJ的熱量,請回答下列問題:
①氫氣的燃燒熱為__________;
②氫氣燃燒熱的熱化學方程式為________;
(5)氫能的存儲是氫能利用的前提,科學家研究出一種儲氫合金Mg2Ni,已知:
Mg(s)+H2(g)=MgH2(s) ΔH1=-74.5kJ·mol-1;
Mg2Ni(s)+2H2(g)=Mg2NiH4(s) ΔH2;
Mg2Ni(s)+2MgH2(s)=2Mg(s)+Mg2NiH4(s) ΔH3=+84.6kJ·mol-1。
則ΔH2=_______kJ·mol-1;
(6)白磷與氧氣可發生如下反應:P4+5O2=P4O10。已知斷裂下列化學鍵需要吸收的能量分別為P—P a kJ·mol-1、P—O b kJ·mol-1、P=O c kJ·mol-1、O=O d kJ·mol-1。根據圖示的分子結構和有關數據估算該反應的ΔH為_____。
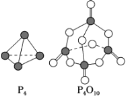
(7)同素異形體相互轉化的反應熱相當小而且轉化速率較慢,有時還很不完全,測定反應熱很困難。現在可根據蓋斯提出的“不管化學過程是一步完成或分幾步完成,這個總過程的熱效應是相同的”觀點來計算反應熱。已知:
①P4(白磷,s)+5O2(g)=P4O10(s) ΔH1=-2 983.2 kJ·mol-1
②P(紅磷,s)+5/4O2(g)=1/4P4O10(s) ΔH2=-738.5 kJ·mol-1
相同狀況下,能量較低的是________;白磷的穩定性比紅磷________(填“大”或“小”)。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】高鐵酸鉀(K2FeO4)是一種集強氧化性、吸附、絮凝于一體的新型多功能處理劑,其生產工藝如圖所示:
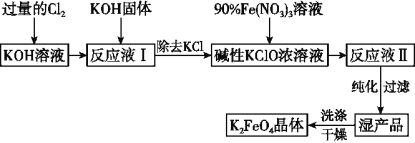
已知K2FeO4具有下列性質:
①可溶于水、微溶于濃KOH溶液
②在0~5 ℃、強堿性溶液中比較穩定
③在Fe3+和Fe(OH)3催化作用下發生分解
④在酸性至堿性條件下,能與水反應生成Fe(OH)3和O2
請完成下列填空:
(1)已知Cl2與KOH在較高溫度下反應生成KClO3。在不改變KOH溶液的濃度和體積的條件下,生產KClO應在溫度___________的情況下進行(填“較高”或“較低”)。
(2)生產K2FeO4的反應原理是:Fe(NO3)3+KClO+KOH→K2FeO4+KNO3+KCl+H2O(未配平),則該反應中氧化劑與還原劑的物質的量之比為______________。
(3)K2FeO4在弱堿性條件下能與水反應生成Fe(OH)3和O2,則該反應的化學方程式為________________。
(4)在“反應液Ⅰ”中加KOH固體的目的是___________。
A. 為下一步反應提供反應物
B. 與“反應液Ⅰ”中過量的Cl2繼續反應,生成更多的KClO
C. KOH固體溶解時會放出較多的熱量,有利于提高反應速率
D. 使副產物KClO3轉化為KCl
(5)制備K2FeO4時,須將90%的Fe(NO3)3溶液緩慢滴加到堿性的KClO濃溶液中,并且不斷攪拌。采用這種混合方式的原因是_______________________ (答出1條即可)。
(6)從“反應液Ⅱ”中分離出K2FeO4晶體后,可以得到的副產品有________ (寫化學式)。
(7)工業上常用“間接碘量法”測定高鐵酸鉀樣品中高鐵酸鉀的含量,其方法是:用堿性的碘化鉀溶液(pH為11~12)溶解3.96 g高鐵酸鉀樣品,調節pH為1,避光放置40分鐘至反應完全(高鐵酸根離子全部被還原成鐵離子),再調節pH為3~4(弱酸性)。以1.0 mol/L的硫代硫酸鈉標準溶液為滴定劑進行滴定(2Na2S2O3+I2=Na2S4O6+2NaI),當達到滴定終點時,用去硫代硫酸鈉標準溶液15.00 mL,則原高鐵酸鉀樣品中高鐵酸鉀的質量分數為______________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】阿伏伽德羅常數可用NA表示,下列敘述中正確的是( )
A.1mol H2O所含的原子數為NA個
B.16g O2-含有的電子數為10NA個
C.常溫常壓下,11.2L Cl2所含分子數為0.5NA個
D.1L 1mol/L NaClO溶液中含ClO-個數為NA個
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】從宏觀現象探究微觀本質是重要的化學學科素養。以亞硫酸納(Na2SO3)為實驗對象,探究其性質。實驗如下:
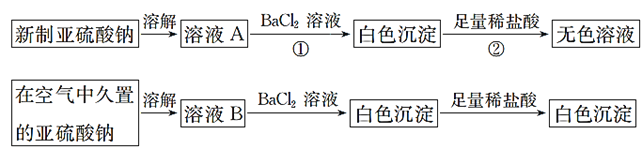
(1)寫出上述實驗中②的離子方程式:__________。
(2)通過上述實驗可知,在空氣中久置的亞硫酸納固體中會混有____________ (填化學式)。
(3)亞硫酸納晶體樣品若變質,下列說法錯誤的是 _______________。
A.晶體表面變黃 B.其水溶液pH 將減小 C.其樣品質量將增加
(4)將碳酸納溶液加熱到40 ℃通入二氧化硫飽和后,再加入等量的碳酸鈉溶液,在避免與空氣接觸的情況下結晶可制得亞硫酸鈉,該制備過程總反應的化學方程式 ___________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】某溫度下,在一個2 L的密閉容器中加入4 mol A和2 mol B進行如下反應:3A(g)+2B(g)![]() 4C(s)+D(g),反應2 min后達到平衡,測得生成1.6 mol C,下列說法正確的是
4C(s)+D(g),反應2 min后達到平衡,測得生成1.6 mol C,下列說法正確的是
A. 前2 min,D的平均反應速率為0.2 mol·L-1·min-1 B. 此時,B的平衡轉化率是40%
C. 升高該體系的溫度,化學平衡常數不變 D. 增加C,逆向速率增大
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】聯堿法(侯氏制堿法)和氨堿法的生產流程簡要表示如下:
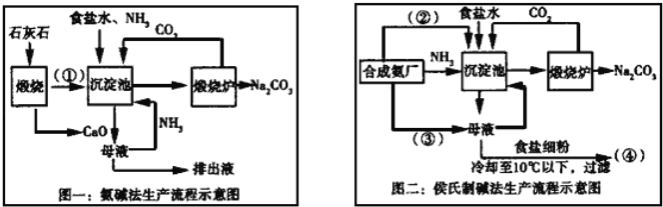
完成下列填空:
(1)寫出化學式:②_____、③____
(2)從理論上分析,氨堿法生產過程中_____(選填“需要”、“不需要”)補充氨氣,寫出該工藝中生成CaCl2的化學方程式________________。
(3)對聯堿法中從母液中提取氯化銨晶體的過程進行分析,所得結論合理的是______。
a.常溫時氯化銨的溶解度比氯化鈉小
b.通入氨氣可把碳酸氫鈉轉化為碳酸鈉,防止碳酸氫鈉析出
c.加入食鹽細粉目的是提高Na+的濃度,促進碳酸氫鈉結晶析出
(4)取“侯氏制堿法”生產的純堿樣品5.500g,配成500mL溶液,取25mL溶液用0.1000mol/L的標準鹽酸滴定(設其中的雜質不與鹽酸反應),用酚酞作指示劑,三次滴定消耗鹽酸的平均量為25.00mL.計算樣品中純堿的質量分數______。(已知25℃時0.1mol/L的NaHCO3溶液的pH約為8.3)某活動小組根據上述制堿原理,用如下所示裝置(夾持裝置省略)制備碳酸氫鈉.
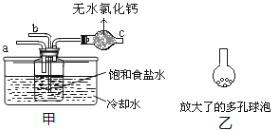
(5)實驗時,須先從____管通入_____氣體,再從_____管中通入_____氣體。
(6)有同學建議在甲裝置的b管下端連接乙裝置,目的是________________________________。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com