
【題目】有一無色溶液,其中可能含有 Fe3+、Al2+ 、Fe2+、Mg2+、Cu2+、NH4+、K+、CO32-、SO42-等離子的幾種,為分析其成分,取此溶液分別進行了四個實驗,其探作和有關現象如下圖所示:
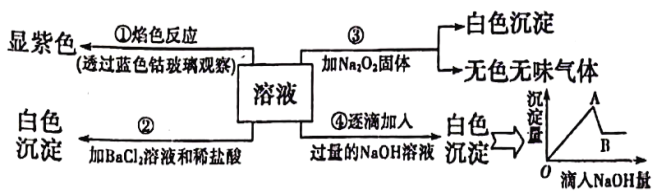
請你根據上圖推斷:
(1)原溶液中一定存在的陰離子有(寫化學式):_________________________。
(2)寫出實驗④中產生的沉淀有:______________________。
寫出由A→B過程中所發生反應的離子方程式: ______________________。
(3)實驗③中產生無色無味氣體所發生的化學方程式為:______________________。
(4)實驗②中加入稀鹽酸的目的是______________________。
【答案】SO42- Al(OH)3、Mg(0H)2 Al(0H)3+0H-=Al02-+2H20 2Na202+2H20= 4Na0H+02↑ 確定白色沉淀不是碳酸鋇沉淀,而是硫酸鋇沉淀
【解析】
根據常見離子的顏色、焰色反應等特征性質,結合實驗現象分析回答。
無色溶液中不可能含有 Fe3+(黃色)、Fe2+(淡綠色)、Cu2+(藍色)。
(1)據實驗②,原溶液中加入BaCl2溶液和稀鹽酸生成的白色沉淀只能是BaSO4,一定存在的陰離子SO42-;
(2)據實驗④中產生的沉淀與滴入NaOH溶液的關系圖,A→B是Al(OH)3溶解,離子方程式是Al(OH)3+OH-=AlO2-+2H2O,B點后是Mg(OH)2不溶于堿,故生成的沉淀有Al(OH)3、Mg(OH)2;
(3)實驗③中,Na2O2與水反應2Na2O2+2H2O= 4NaOH+O2↑,所得氣體無色無味,則不含氨氣,原溶液中無NH4+。
(4)BaCO3能溶于稀鹽酸,而BaSO4不溶。實驗②中加入稀鹽酸,保證生成的白色沉淀中只有BaSO4。


科目:高中化學 來源: 題型:
【題目】下圖為實驗室制取純凈、干燥的 Cl2,并進行檢驗 Cl2性質的實驗裝置。其中 D 瓶中放有干燥的紅色布條;E 中為銅網,E 右端出氣管口附近為棉球。試回答:
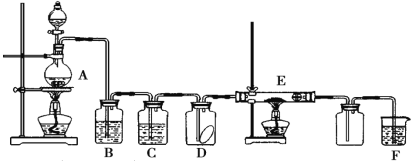
(1)A 中發生反應的化學方程式為_____; 制得 2mol Cl2時,轉移的電子為______mol。
(2)為得到干燥純凈的氯氣,一般在 B 瓶中加入_____; 裝置 C 的作用是______。
(3)D 中現象為_______。
(4)F 中反應的離子方程式為______。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】BHT是一種常用的食品抗氧化劑,從![]() 出發合成BHT的方法有如圖兩種.下列說法錯誤的是( )
出發合成BHT的方法有如圖兩種.下列說法錯誤的是( )
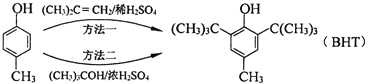
A.從綠色化學角度分析方法一優于方法二
B.BHT在水中的溶解度小于苯酚
C.兩種方法的反應類型都是加成反應
D.BHT與![]() 都能使酸性KMnO4褪色
都能使酸性KMnO4褪色
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】兩份質量均為mg的Na2CO3、NaHCO3固體混合物,加熱第一份充分反應得到CO2質量是xg,向加熱后所得固體中加入足量的鹽酸得到CO2 ag;向第二份中直接加入足量鹽酸得到CO2的質量是bg.則x等于
A.2bB.2aC.b-2aD.b-a
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】二甲醚又稱甲醚,簡稱DME,熔點為-141.5℃,沸點為-24.9℃。二甲醚與液化石油氣(LPG)相似,被譽為“21世紀的清潔燃料”。由合成氣(CO、H2)制備二甲醚的反應原理如下:
①CO(g)+2H2(g)![]() CH3OH(g) △H1= -90.0 kJ·mol-1
CH3OH(g) △H1= -90.0 kJ·mol-1
②2CH3OH(g)![]() CH3OCH3(g)+H2O(g) △H2=-20.0kJ·mol-l
CH3OCH3(g)+H2O(g) △H2=-20.0kJ·mol-l
回答下列問題:
(1)反應①為熵___________(填“增加”或“減少”)的反應,__________ (填“低溫”或“高溫”)下易自發進行。
(2)寫出由合成氣(CO、H2) 直接制備二甲醚的熱化學方程式:__________________________________。
(3)溫度為500K時,在2L的密閉容器中充入2 mol CO和6 molH2發生反應①、②,5 min時達到平衡,平衡時CO的轉化率為60%,c(CH3OCH3)=0.2 mol·L-1,用H2表示反應①的速率是______________,反應②的平衡常數K=________________。
若在500K時,測得容器中n(CH3OCH3)=2n (CH3OH),此時反應②的v正__ v逆(填“>”、 “< ”或“=”)。
(4)研究發現,在體積相同的容器中加入物質的量相同的CO和H2發生反應①、②,在不同溫度和有無催化劑組合下經過相同反應時間測得如下實驗數據:
T(K) | 催化劑 | CO轉化率(%) | CH3OCH3選擇性(%) |
473 | 無 | 10 | 36 |
500 | 無 | 12 | 39 |
500 | Cu/ZnO | 20 | 81 |
[備注]二甲醚選擇性:轉化的CO中生成CH3OCH3的百分比
①相同溫度下,選用Cu/ZnO作催化劑,該催化劑能____________ (填標號)。
A.促進平衡正向移動 B.提高反應速率 C.降低反應的活化能
D.改變反應的焓變 E.提高CO的平衡轉化率
②表中實驗數據表明,在500K時,催化劑Cu/ZnO對CO轉化成CH3OCH3的選擇性有顯著的影響,其原因是_________________________________________________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】在兩份相同的Ba(OH)2溶液中,分別滴入物質的量濃度相等的H2SO4、NaHSO4溶液,其導電能力隨滴入溶液體積變化的曲線如圖所示,下列分析正確的是
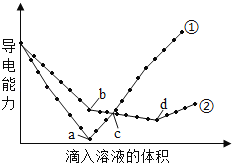
A. ②代表滴加H2SO4溶液的變化曲線
B. b點,兩反應物物質的量之比為1: 2
C. a、d兩點對應的溶液均顯中性
D. c點,兩溶液中含有相同物質的量濃度的OH﹣
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列儀器用酒精燈加熱時,需墊石棉網的是( )
①燒杯 ②坩堝 ③錐形瓶 ④蒸發皿 ⑤試管 ⑥燒瓶 ⑦表面皿
A.②④⑤B.①⑥⑦C.③④⑥D.①③⑥
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】t℃時,AgX(X=Cl、Br)的溶度積與c(Ag+)和c(X-)的相互關系如下圖所示,其中A線表示AgCl,B線表示AgBr,已知p(Ag+)=-lgc(Ag+),p(X-)=-lgc(X-)。下列說法正確的是( )

A. c點可表示AgCl的不飽和溶液
B. b點的AgCl溶液加入AgNO3晶體可以變成a點
C. t℃時,AgCl(s)+Br-(aq)![]() AgBr(s)+Cl-(aq)平衡常數K=10-4
AgBr(s)+Cl-(aq)平衡常數K=10-4
D. t℃時,取a點的AgCl溶液和b點AgBr溶液等體積混合,會析出AgBr沉淀
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】將SO2氣體與足量Fe2(SO4)3溶液完全反應后,再加入K2Cr2O7溶液,發生如下兩個化學反應:SO2+2Fe3++2H2O===![]() +2Fe2++4H+,Cr2O72-+6Fe2++14H+===2Cr3++6Fe3++ 7H2O,有關說法正確的是
+2Fe2++4H+,Cr2O72-+6Fe2++14H+===2Cr3++6Fe3++ 7H2O,有關說法正確的是
A. 還原性Cr3+>Fe2+>SO2
B. 氧化性Cr2O72->SO2>Fe3+
C. 兩個反應中Fe2(SO4)3均作還原劑
D. Cr2O72-能將Na2SO3氧化成Na2SO4
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com