
【題目】氟是一種鹵族元素。但它與其他鹵素在單質和化合物的制備與性質上存在較明顯的差異
(1)研究發現,SbF5能將MnF4從離子[MnF6]2-的鹽中反應得到,SbF5轉化成穩定離子[SbF6]-的鹽。而MnF4很不穩定,受熱易分解為MnF3和F2。根據以上研究寫出以K2MnF6和SbF5為原料,在423 K的溫度下制備F2的化學方程式:____________________。
(2)現代工業以電解熔融的氟氫化鉀(KHF2)和氟化氫(HF)混合物制備氟單質,電解制氟裝置如圖所示。
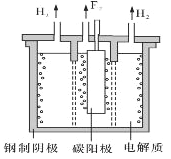
①已知KHF2是一種酸式鹽,寫出陰極上發生的電極反應式______________。
②電解制氟時,要用鎳銅合金隔板將兩種氣體產物嚴格分開的原因是____________ 。
③HF的水溶液能用于蝕刻玻璃,其化學反應方程式為:_____________________。
④已知25℃時,氫氟酸(HF)的電離平衡常數Ka=3.6×10-4。某pH=2的氫氟酸溶液,由水電離出的c(H+)=_________mol/L;若將0.01 mol/L HF溶液與pH=12的NaOH溶液等體積混合,則溶液中離子濃度大小關系為:__________________。
⑤又已知25℃時,溶度積常數Ksp(CaF2)=1.46×10-10。現向1L0.2 mol/L HF溶液中加入1L0.2 mol/L CaCl2溶液,____________(填“是”、“否”) 有沉淀產生,并通過列式計算說明__________________。
【答案】 2K2MnF6+4SbF5![]() 4KSbF6+2MnF3+F2↑ 2HF2-+2e-=H2↑+4F- 氟氣和氫氣能發生劇烈反應,引發爆炸 SiO2+4HF=SiF4↑+2H2O 10-12 c(Na+)>c(F-)>c(OH-)>c(H+) 是 c(H+)=c(F-)=6×l0-3mol ·L-1,c(Ca2+)=0.lmol·L-1,c(F-)2·c(Ca2+)=3.6×10-5×0.1=3.6×10-6>1.46×10-10, 該體系有CaF2 沉淀
4KSbF6+2MnF3+F2↑ 2HF2-+2e-=H2↑+4F- 氟氣和氫氣能發生劇烈反應,引發爆炸 SiO2+4HF=SiF4↑+2H2O 10-12 c(Na+)>c(F-)>c(OH-)>c(H+) 是 c(H+)=c(F-)=6×l0-3mol ·L-1,c(Ca2+)=0.lmol·L-1,c(F-)2·c(Ca2+)=3.6×10-5×0.1=3.6×10-6>1.46×10-10, 該體系有CaF2 沉淀
【解析】本題綜合考查化學反應原理。(1)①以K2MnF6和SbF5為原料,在423 K的溫度下, K2MnF6和SbF5反應先生成KSbF6和MnF4,MnF4受熱易分解為MnF3和F2,故其化學方程式:2K2MnF6+4SbF5![]() 4KSbF6+2MnF3+F2↑;(2)①陰極上為氫離子(HF2-中的氫離子)放電生成氫氣,其電極反應為:2HF2—+2e—=4F—+ H2↑;②F2與H2在暗處發生爆炸,因此電解制氟時,要用鎳銅合金隔板將兩種氣體產物嚴格分開;③玻璃的主要成分為二氧化硅,故HF與二氧化硅反應的化學方程式為:SiO2+4HF=SiF4↑+2H2O;④pH=2的氫氟酸溶液,水的電離受到抑制,由水電離出的c(H+)水=c(OH—)水=c(OH—)==
4KSbF6+2MnF3+F2↑;(2)①陰極上為氫離子(HF2-中的氫離子)放電生成氫氣,其電極反應為:2HF2—+2e—=4F—+ H2↑;②F2與H2在暗處發生爆炸,因此電解制氟時,要用鎳銅合金隔板將兩種氣體產物嚴格分開;③玻璃的主要成分為二氧化硅,故HF與二氧化硅反應的化學方程式為:SiO2+4HF=SiF4↑+2H2O;④pH=2的氫氟酸溶液,水的電離受到抑制,由水電離出的c(H+)水=c(OH—)水=c(OH—)== 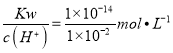 =10-12 mol/L;將0.01 mol/L HF溶液與pH=12的NaOH溶液等體積混合,恰好完全中和,所得溶液溶質為NaF,因F—水解,溶液呈堿性,結合電荷守恒可知溶液中離子濃度大小為:c(Na+)>c(F-)>c(OH-)>c(H+),⑤兩溶液混合后,c(Ca2+)=0.1 mol/L,c(F—)=
=10-12 mol/L;將0.01 mol/L HF溶液與pH=12的NaOH溶液等體積混合,恰好完全中和,所得溶液溶質為NaF,因F—水解,溶液呈堿性,結合電荷守恒可知溶液中離子濃度大小為:c(Na+)>c(F-)>c(OH-)>c(H+),⑤兩溶液混合后,c(Ca2+)=0.1 mol/L,c(F—)= ![]() ,則Qc(CaF2)= c2(F-)×c(Ca2+)=(6×10-3mol/L)2×0.1 mol/L=3.6×10-6>Ksp(CaF2),說明有沉淀產生。
,則Qc(CaF2)= c2(F-)×c(Ca2+)=(6×10-3mol/L)2×0.1 mol/L=3.6×10-6>Ksp(CaF2),說明有沉淀產生。


 口算心算速算應用題系列答案
口算心算速算應用題系列答案 同步拓展閱讀系列答案
同步拓展閱讀系列答案科目:高中化學 來源: 題型:
【題目】(1)有下列幾組物質,請將序號填入下列空格內:
A、CH2=CH-COOH和油酸(C17H33COOH) B、12C60和石墨 C、 ![]() 和
和![]() D、35Cl和37Cl E、乙醇和乙二醇
D、35Cl和37Cl E、乙醇和乙二醇
①互為同位素的是______________;②互為同系物的是_________________;
③互為同素異形體的是__________;④互為同分異構體的是_____________;
⑤既不是同系物,又不是同分異體,也不是同素異形體,但可看成是同一類物質的是______
(2)請寫出下列反應的化學方程式:
①丙氨酸縮聚形成多肽:____________________________________________________________
②淀粉水解:______________________________________________________________________
③丙醛與新制的氫氧化銅懸濁液反應:________________________________________________
(3)已知滌綸樹脂的結構簡式如下圖所示,請寫出合成滌綸樹脂所需要單體的結構簡式:
 ________________和_________________
________________和_________________
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列水解離子方程式正確的是
A. HCO3-+H2O![]() H3O++CO32- B. NH4++H2O
H3O++CO32- B. NH4++H2O![]() NH3·H2O+H+
NH3·H2O+H+
C. CO32-+2H2O![]() H2CO3+2OH- D. Fe3++3H2O
H2CO3+2OH- D. Fe3++3H2O![]() Fe(OH)3↓+3H+
Fe(OH)3↓+3H+
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】在體積為V L的硫酸鋁溶液中加入足量的氨水,過濾得沉淀,將沉淀洗凈后灼燒至質量不再變化時冷卻、稱量,得mg白色固體.原溶液中c(SO42﹣)為( )
A.![]() mol?L﹣1
mol?L﹣1
B.![]() mol?L﹣1
mol?L﹣1
C.![]() mol?L﹣1
mol?L﹣1
D.![]() mol?L﹣1
mol?L﹣1
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】氫氣可以在氯氣中燃燒,下列說法正確的是
A. 反應在點燃條件下發生,是吸熱反應
B. 反應中的能量變化與反應物的用量多少無關
C. 反應物的總能量高于生成物的總能量
D. 化學鍵斷裂吸收的總能量高于化學鍵形成放出的總能量
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com