
【題目】前四周期元素![]() 、
、![]() 、
、![]() 、
、![]() 、
、![]() 的原子序數依次增大。
的原子序數依次增大。![]() 與
與![]() 同周期且相鄰,
同周期且相鄰,![]() 的基態原子的
的基態原子的![]() 電子數與
電子數與![]() 電子數相等,乙是地殼中含量最多的金屬元素,
電子數相等,乙是地殼中含量最多的金屬元素,![]() 的原子核外價電子排布式為
的原子核外價電子排布式為![]() ,
,![]() 的基態原子的未成對電子數是同周期元素中最多的。下列說法錯誤的是( )
的基態原子的未成對電子數是同周期元素中最多的。下列說法錯誤的是( )
A.簡單氣態氫化物的穩定性:![]()
B.簡單離子的半徑:![]()
C.![]() 的最高價氧化物對應的水化物既能與強酸反應,又能與強堿反應
的最高價氧化物對應的水化物既能與強酸反應,又能與強堿反應
D.由![]() 、
、![]() 、
、![]() 三種元素形成的某種化合物可用于檢查司機是否酒后駕車
三種元素形成的某種化合物可用于檢查司機是否酒后駕車
【答案】B
【解析】
前四周期元素X、Y、Z、W、Q的原子序數依次增大.Z是地殼中含量最多的金屬元素,則Z為Al;Y原子序數小于Al,Y的基態原子s電子數與p電子數相等,核外電子排布為1s22s22p4或1s22s22p63s2,X與Y同周期相鄰的非金屬元素,則Y為O,X為N元素;W的價電子排布為4s1,則W為K;結合原子序數可知,Q處于第四周期,基態Q原子的未成對電子是同周期元素中最多的,原子外圍電子排布為3d54s1,則Q為Cr,結合元素周期律解元素化合物性質解答。
A.非金屬性O>N,故簡單氫化物穩定性:O>N,故A正確;
B.電子層結構相同,核電荷數越大離子半徑越小,故離子半徑N3->O2->Al3+,故B錯誤;
C.氫氧化鋁是兩性氫氧化物,與強酸反應生成鋁鹽與水,與強堿反應都生成偏鋁酸鹽與水,故C正確;
D.由O、K、Cr形成的化合物K2Cr2O7,可用于檢查司機酒后駕車,故D正確;
答案選B。


 名師金手指領銜課時系列答案
名師金手指領銜課時系列答案科目:高中化學 來源: 題型:
【題目】某化學科研小組研究在其他條件不變時,改變某一條件對化學平衡的影響,得到如圖所示變化規律(p表示壓強,T表示溫度,n表示物質的量):
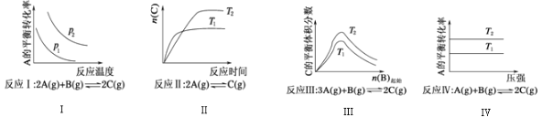
根據以上規律判斷,下列結論正確的是( )
A.反應Ⅰ:△H>0,p2>p1
B.反應Ⅲ:△H>0,T2>T1或△H<0,T2<T1
C.反應Ⅱ:△H>0,T1>T2
D.反應Ⅳ:△H<0,T2>T1
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】一種釕(Ru)基配合物光敏染料敏化太陽能電池的工作原理及電池中發生的主要反應如圖所示。下列說法錯誤的是

A. 電池工作時,光能轉變為電能,X為電池的負極
B. 鍍鉑導電玻璃上發生氧化反應生成I-
C. 電解質溶液中發生反應:2Ru3++3I-![]() 2Ru2++I3-
2Ru2++I3-
D. 電池工作時,電解質溶液中I-和I3-的濃度基本不變
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】已知A、B、R、D都是周期表中前四周期的元素,它們的原子系數依次增大。其中A元素基態原子第一電離能比B元素基態原子的第一電離能大,B的基態原子的L層、R基態原子的M層均有2個單電子,D是第Ⅷ族中原子序數最小的元素。
(1)寫出基態D原子的電子排布式__________。
(2)已知高純度R的單質在現代信息技術與新能源開發中具有極為重要的地位。工業上生產高純度R的單質過程如下:
![]()
寫出過程③的反應方程式___________,已知RHCl3的沸點是31.5oC,則該物質的晶體類型是__________,中心原子的軌道雜化類型為__________,該物質的空間構型是______。
(3)A的第一電離能比B的第一電離能大的原因是_________,A、B兩元素分別與R形成的共價鍵中,極性較強的是________。A、B兩元素間能形成多種二元化合物,其中與A3-互為等電子體的物質的化學式為_______。
(4)已知D單質的晶胞如圖所示,則晶體中D原子的配位數為______,一個D的晶胞質量為____,已知D原子半徑為r pm,則該晶胞的空間利用率為_____________ (寫出計算過程)。
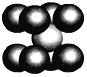
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】有機化合物M是一種藥品輔料的中間體,下圖是該有機化合物的合成線路。請回答下列問題。
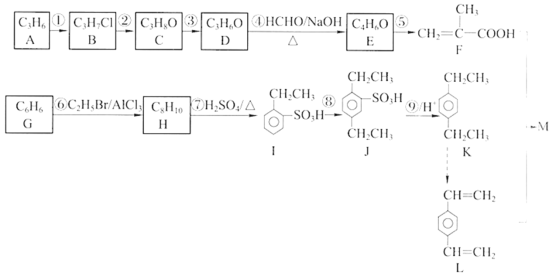
已知: i.
ii.兩種或兩種以上的單體發生的加聚反應稱為共聚反應,如:

(1)A的結構簡式是_________。
(2)反應②的化學方程式是_________。
(3)合成線路①~⑤中屬于氧化反應的有_________(填序號)。
(4)反應④的化學方程式是_________。
(5)若1mol D與2mol HCHO反應,該反應產物的結構簡式是_________。
(6)反應⑧的反應物及反應條件是_________。
(7)合成線路中⑦~⑨的目的是_________。
(8)在一定條件下,F與L按物質的量之比1 : 1發生共聚反應合成M,其鏈節中不含碳碳雙鍵,且除苯環外不含其他環狀結構,則M的結構簡式是_________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】高分子材料聚酯纖維H的一種合成路線如下:

已知:CH2=CHCH3![]() CH2=CHCH2Cl+HCl
CH2=CHCH2Cl+HCl
請回答下列問題:
(1)C的名稱是____,D的結構簡式為____。
(2)E—F的反應類型是____,E分子中官能團的名稱是 ___。
(3)寫出C和G反應生成H的化學方程式____。
(4)在G的同分異構體中,同時滿足下列條件的結構有 ___種(不考慮立體異構)。
①屬于芳香族化合物,能發生銀鏡反應和水解反應,遇FeCl3溶液發生顯色反應
②1mol該有機物與3molNaOH恰好完全反應
③分子結構中不存在![]()
其中,核磁共振氫譜顯示4組峰的結構簡式為____。
(5)參照上述流程,以1-丁烯為原料合成HOCH2(CHOH)2CH2OH,設計合成路線____(無機試劑任選)。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】我國科學家研制出一種能在室溫下高效催化空氣中的甲醛氧化的催化劑,其反應如下:HCHO+O2 ![]() CO2+H2O。下列有關說法正確的是( )
CO2+H2O。下列有關說法正確的是( )
A.反應物和生成物都是非極性分子
B.HCHO 的空間構型為四面體形
C.HCHO、CO2 分子的中心原子的雜化類型不同
D.液態水中只存在一種作用力
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列有關說法正確的是
①二氧化硅可與NaOH溶液反應,因此可用NaOH溶液雕刻玻璃;
② 明礬溶于水可水解生成Al(OH)3膠體,因此可以用明礬對自來水進行殺菌消毒;
③ 可用蒸餾法、電滲析法、離子交換法等對海水進行淡化;
④ 從海帶中提取碘只需用到蒸餾水、H2O2溶液和四氯化碳三種試劑;
⑤地溝油可用來制肥皂、提取甘油或者生產生物柴油;
⑥石英玻璃、Na2O·CaO·6SiO2、淀粉、氨水的物質類別依次為純凈物、氧化物、混合物、弱電解質。
A. ③⑤⑥ B. ①④⑤ C. 除②外都正確 D. ③⑤
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】T℃時,三種鹽的沉淀溶解平衡曲線如圖所示,已知pM為陽離子濃度的負對數,pR為陰離子濃度的負對數,下列說法正確的是

A.Y點:![]() ,Z點:
,Z點:![]()
B.溶度積:Ksp(MnCO3)>Ksp(CaCO3)>Ksp(CaSO4)
C.X點對應的CaCO3溶液為不飽和溶液,可以繼續溶解CaCO3
D.T℃時,![]() 的平衡常數K的數量級為103
的平衡常數K的數量級為103
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com