
【題目】室溫下,某容積固定的密閉容器由可移動的活塞隔成 A、B 兩室,向 A 中充入一定量 H2、O2 的混合氣體,向 B 中充入 1 mol 空氣,此時活塞的位置如圖所示。

(1)A 室混合氣體的物質的量為______,所含分子總數約______。
(2)實驗測得 A 室混合氣體的質量為 34 g,則該混合氣體的密度是同溫同壓條件下氦氣密度的______倍。
(3)若將 A 室 H2、O2的混合氣體點燃引爆,恢復原溫度后,最終活塞停留的位置在______刻度,容器內氣體壓強與反應前氣體壓強之比為______。
【答案】2mol 1.204×1024 4.25 2 1:2
【解析】
(1)同溫同壓下,氣體的物質的量之比等于其氣體之比;根據N=nNA計算分子數目;
(2)計算A室中混合氣體的平均摩爾質量,同溫同壓下氣體的密度之比等于其摩爾質量之比;
(3)根據總質量、總物質的量列方程計算氫氣與氧氣物質的量,根據方程式計算反應后剩余氣體物質的量,恢復原溫度后最終兩室中壓強相等,體積之比等于其物質的量之比,可以確定活塞停留的位置;B室中空氣物質的量不變、溫度不變,反應前后壓強之比與反應前后體積成反比。
(1)相同條件下,氣體的體積之比等于其物質的量之比,1mol空氣占容器總體積的1/3,空氣和H2、O2 的混合氣體的體積之比為1:2,則其物質的量之比為1:2,所以混合氣體的物質的量為2mol,所含分子總數約為2×6.02×1023=1.204×1024,故答案為:2mol;1.204×1024;
(2)設H2的物質的量為x,O2的物質的量為y,則有關系式:x+y=2,2x+32y=34,解聯立方程得,x= 1mol、y=1mol,該混合氣體的平均相對分子質量=2×1/2+32×1/2=17,由同溫同壓條件下密度之比等于摩爾質量之比可知,則該混合氣體的密度是同溫同壓條件下氦氣密度的17/4=4.25倍, 故答案為:4.25;
(3) 若將 A 室 H2、O2的混合氣體點燃引爆,由方程式可知氧氣有誰剩余,剩余氧氣為1mol-1mol×1/2=0.5mol,恢復原溫度后最終兩室中壓強相等,體積之比等于其物質的量之比,則A、B兩室的體積之比為0.5mol:1mol=1:2,則活塞停留在2刻度處;A室中空氣物質的量不變、溫度不變,反應前后壓強之比與反應前后體積成反比,則容器內氣體壓強與反應前氣體壓強之比為2:4=1:2,故答案為:2;1:2。


科目:高中化學 來源: 題型:
【題目】下列事實不能用勒夏特列原理解釋的是
A. 實驗室中用排飽和食鹽水法收集氯氣
B. 合成氨工廠生產過程中通常采用較高壓強
C. 工業上生產硫酸過程中,通入過量空氣以提高SO2利用率
D. 由NO2(g)、N2O4(g)組成的平衡體系加壓后最終顏色比加壓前深
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】鎂與稀硝酸的反應為:4Mg+10HNO3(稀)=4Mg(NO3)2+NH4NO3+3H2O
(1)用“雙線橋法”表示該反應中電子轉移的方向和數目__________。
(2)該反應中,Mg發生了__________反應,氧化劑與還原劑的物質的量之比為__________________。
(3)還原產物是_________,HNO3表現了__________________。
(4)若反應過程中轉移的電子數為1.505×1023,則參加反應的Mg的質量為________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列關于熱化學反應的描述中正確的是
A.HCl和NaOH反應的中和熱ΔH=-57.3kJ/mol,則H2SO4和Ca(OH)2反應的中和熱ΔH=2×(-57.3)kJ/mol
B.CO(g)的燃燒熱是283.0 kJ/mol,則2CO(g)+O2(g) =2CO2(g)反應的ΔH=—(2×283.0)kJ/mol
C.需要加熱才能發生的反應一定是吸熱反應
D.1 mol甲烷燃燒生成氣態水和二氧化碳所放出的熱量是甲烷的燃燒熱
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】烴A的質譜圖中,質荷比最大的數值為42。碳氫兩元素的質量比為6:1,其核磁共振氫譜有三個峰,峰的面積比為1:2:3。A與其他有機物之間的關系如下:

已知:CH2=CH2![]() HOCH2CH2OH,回答下列問題:
HOCH2CH2OH,回答下列問題:
(1)有機物B的分子式___________________________。
(2)高聚物F結構簡式為___________________。
(3)寫出C與新制的氫氧化銅反應的化學方程式___________________________。
(4)E在一定條件下可以相互反應生成一種六元環有機物H,H的結構簡式________.。
(5)寫出生成G的化學方程式_____________________________________________;
【答案】 )C3H8O2 ![]()
![]()
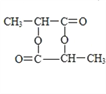 n
n![]()
![]()
![]() +(n-1)H2O
+(n-1)H2O
【解析】試題分析:本題考查有機推斷,涉及有機物分子式和結構簡式的確定、有機物分子式和結構簡式的書寫、有機反應方程式的書寫。A的質譜圖中質荷比最大的數值為42,A的相對分子質量為42,烴A中n(C):n(H)=![]() :
: ![]() =1:2,A的實驗式為CH2,A的分子式為(CH2)x,14x=42,解得x=3,A的分子式為C3H6,A的核磁共振氫譜有三個峰且峰的面積比為1:2:3,A的結構簡式為CH2=CHCH3。A發生加聚反應生成的高聚物F的結構簡式為
=1:2,A的實驗式為CH2,A的分子式為(CH2)x,14x=42,解得x=3,A的分子式為C3H6,A的核磁共振氫譜有三個峰且峰的面積比為1:2:3,A的結構簡式為CH2=CHCH3。A發生加聚反應生成的高聚物F的結構簡式為![]() ;A→B發生題給已知的反應,B的結構簡式為
;A→B發生題給已知的反應,B的結構簡式為![]() ;B→C發生醇的催化氧化,C的結構簡式為
;B→C發生醇的催化氧化,C的結構簡式為![]() ;C與Cu(OH)2加熱時,C中-CHO被氧化,酸化后得到的D的結構簡式為
;C與Cu(OH)2加熱時,C中-CHO被氧化,酸化后得到的D的結構簡式為![]() ;D與H2發生加成反應生成E,E的結構簡式為
;D與H2發生加成反應生成E,E的結構簡式為![]() ;E中含羥基和羧基,E發生縮聚反應生成高聚物G,G的結構簡式為
;E中含羥基和羧基,E發生縮聚反應生成高聚物G,G的結構簡式為![]() 。
。
(1)B的結構簡式為![]() ,B的分子式為C3H8O2。
,B的分子式為C3H8O2。
(2)高聚物F的結構簡式為![]() 。
。
(3)C的結構簡式為![]() ,C與新制Cu(OH)2反應的化學方程式為
,C與新制Cu(OH)2反應的化學方程式為![]() +2Cu(OH)2+NaOH
+2Cu(OH)2+NaOH![]()
![]() +Cu2O↓+3H2O。
+Cu2O↓+3H2O。
(4)E的結構簡式為![]() ,2分子E通過酯化反應形成六元環有機物H,H的結構簡式為
,2分子E通過酯化反應形成六元環有機物H,H的結構簡式為 。
。
(5)G由E發生縮聚反應生成,生成G的化學方程式為n![]()
![]()
![]() +(n-1)H2O。
+(n-1)H2O。
【題型】推斷題
【結束】
18
【題目】苯甲酸乙酯(C9H10O2)稍有水果氣味,用于配制香水香精和人造精油,大量用于食品工業中,也可用作有機合成中間體、溶劑等。其制備方法為:
已知: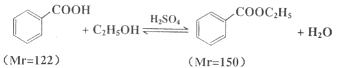
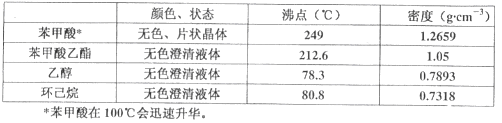

實驗步驟如下:①在100 mL圓底燒瓶中加入12.20 g苯甲酸、25mL乙醇(過量)、20mL環己烷,以及4mL濃硫酸,混合均勻并加入沸石,按左上圖所示裝好儀器,控制溫度在65~70℃加熱回流2h。反應時環己烷-乙醇-水會形成“共沸物”(沸點62.6℃)蒸餾出來。再利用分水器不斷分離除去反應生成的水,回流環己烷和乙醇。
②反應結束,打開旋塞放出分水器中液體后,關閉旋塞。繼續加熱,至分水器中收集到的液體不再明顯增加,停止加熱。
③將燒瓶內反應液倒入盛有適量水的燒杯中,分批加入Na2CO3至溶液呈中性。
④用分液漏斗分出有機層,水層用25mL乙醚萃取分液,然后合并有機層。加入氯化鈣,對粗產品進行蒸餾(裝置如圖所示)。低溫蒸出乙醚后繼續升溫,接收210~213℃的餾分。
⑤檢驗合格,測得產品體積為12.86mL.
(1)步驟①中使用分水器不斷分離除去水的目的是_________________。
(2)步驟②中應控制餾分的溫度在___________________。
A.65~70℃ B.78~80℃ C.85~90℃ D.215~220℃
(3)步驟③中若Na2CO3加入不足,在步驟④蒸餾時,蒸餾燒瓶中可見到白煙生成,產生該現象的原因是_____________。
(4)步驟④中分液操作敘述正確的是__________。
A.水溶液中加入乙醚,轉移至分液漏斗中,塞上玻璃塞。將分液漏斗倒轉用力振搖
B.振搖幾次后需打開分液漏斗下口的玻璃塞放氣
C.經幾次振搖并放氣后,手持分液漏斗靜置待液體分層
D.分液操作時,分液漏斗中的下層液體由下口放出,然后再將上層液體由下口放出
蒸餾裝置圖中儀器A的名稱是___________,在步驟④中加入氯化鈣的作用是_________。
(5)該實驗產品的產率為____________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列各組中的兩物質相互反應時,若改變反應條件(溫度、反應物用量比),化學反應并不改變的是( )
A.Na和O2
B.NaOH和CO2
C.Na2O2和CO2
D.木炭和O2
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】以下是由苯乙烯為原料合成有機高分子化合物M的一種合成路線(部分反應條件及副產物已略去):

已知:I.RCHBr-CH2Br![]() RC≡CH
RC≡CH
II.CH≡CH+CH2=CH-CH=CH2![]()
III. 
請回答下列問題:
(1)D的結構簡式為______,E的結構簡式為________。
(2)C+D→E的反應類型為______,I中含氧官能團的名稱為___________。
(3)H+I→M的化學方程式為___________。
(4)在催化劑加熱條件下,G與氧氣反應生成Q(C9H8O3),同時滿足下列條件的Q的同分異構體有_____種(不考慮立體異構),其中核磁共振氫譜有6組吸收峰的結構簡式為____。
①除苯環外不含其他環狀結構
②能與FeCl3溶液發生顯色反應
③能與NaHCO3溶液反應生成CO2
(5)參照上述合成路線和相關信息,以甲醇和一氯環己烷為有機原料(無機試劑任選),設計制備己二酸二甲酯的合成路線_____________________。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com