
【題目】向一定量的NaOH溶液中逐滴加入AlCl3溶液,生成沉淀Al(OH)3的量隨AlCl3加入量的變化關系如圖所示。則下列離子組在對應的溶液中一定能大量共存的是( )
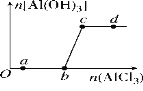
A. a點對應的溶液中:Na+、Fe3+、SO42-、HCO3-
B. b點對應的溶液中:Na+、S2-、SO42-、Cl-
C. c點對應的溶液中:Ag+、Ca2+、NO3-、F-
D. d點對應的溶液中:K+、NH4+、I-、CO32-
 永乾教育寒假作業快樂假期延邊人民出版社系列答案
永乾教育寒假作業快樂假期延邊人民出版社系列答案科目:高中化學 來源: 題型:
【題目】下列有關說法不正確的是( )
A. 鍍銅鐵制品鍍層受損后,鐵制品比受損前更容易生銹
B. 手機上用的鋰離子電池屬于二次電池
C. 燃料電池能把化學能轉化成電能
D. 已知反應2CO(g)=2C(s)+O2(g)的△H>0、△S<0,那么高溫下可自發進行
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】霧霾嚴重影響人們的生活與健康,某地區的霧霾中可能含有如下離子中的若干種:NH4+、Ba2+、Fe2+、Cl-、NO3-、CO32- 、SO42-.某同學收集了該地區的霧霾,經必要的預處理后得到試樣溶液,設計并完成如下實驗:

試回答下列問題:
(1)實驗①中加入稀鹽酸后,有無色氣體A生成,溶液B依然澄清,且溶液中陰離子種類不變,據此可知原溶液中一定不含__________。(填離子符號)
(2)實驗①中發生反應的離子方程式為__________________________________________。
(3)實驗②中逐滴加入碳酸氫鈉溶液,立即有氣泡產生,一段時間后又有沉淀出現,這時的離子方程式為_______________________________________________ 。
(4)氣體F的成分為______________。(填化學式)
(5)根據實驗③現象該同學認為原溶液中一定含有SO42-,有其他同學認為其結論不合理,又進行了后續實驗 ④,最終確認原溶液中含有SO42-,試寫出實驗④可行的操作方法及現象________________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】(1)一定溫度下,Ksp[Mg3(PO4)2]=6.0×10-29,Ksp[Ca3(PO4)2]=6.0×10-26。向濃度均為0.20mol·L-1的MgCl2和CaCl2混合溶液中逐滴加入Na3PO4,先生成________沉淀(填化學式);當測得溶液其中一種金屬陽離子沉淀完全(濃度小于10-5mol·L-1)時,溶液中的另一種金屬陽離子的物質的量濃度為________。
(2)毒重石的主要成分BaCO3(含Ca2+、Mg2+、Fe3+等雜質),實驗室利用毒重石制備BaCl2·2H2O的流程如下:

①毒重石用鹽酸浸取前需充分研磨,目的是________。
②加入NH3·H2O調節pH=8可除去________(填離子符號),濾渣Ⅱ中含________(填化學式)。加入H2C2O4時應避免過量,原因是________。
Ca2+ | Mg2+ | Fe3+ | |
開始沉淀時的pH | 11.9 | 9.1 | 1.9 |
完全沉淀時的pH | 13.9 | 11.1 | 3.7 |
已知:Ksp(BaC2O4)=1.6×10-7,Ksp(CaC2O4)=2.3×10-9。
(3)已知25℃時,CaSO4在水中的沉淀溶解平衡曲線如圖所示,向100mL該條件下的CaSO4飽和溶液中加入400mL 0.01mol·L-1 Na2SO4溶液,下列敘述正確的是___(填字母)。

A.溶液中析出CaSO4沉淀,最終溶液中c(SO42-)比原來的大
B.溶液中無沉淀析出,溶液中c(Ca2+)、c(SO42-)都變小
C.溶液中析出CaSO4沉淀,溶液中c(Ca2+)、c(SO42-)都變小
D.溶液中無沉淀析出,但最終溶液中c(SO42-)比原來的大
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】糖類、油脂和蛋白質是生命活動所必需的營養物質。下列敘述正確的是
A.植物油不能發生水解反應B.葡萄糖能發生氧化反應和水解反應
C.淀粉水解的最終產物是葡萄糖D.蛋白質遇濃硫酸變為黃色
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】某學生做如下實驗:第一步,在淀粉KI溶液中,滴入少量NaClO溶液,并加入少量稀硫酸,溶液立即變藍;第二步,在上述藍色溶液中,滴加足量的Na2SO3溶液,藍色逐漸消失。下列有關該同學對實驗原理的解釋和所得結論的敘述不正確的是( )
A. 氧化性:ClO->I2>SO42—
B. 藍色消失的原因是Na2SO3溶液具有漂白性
C. 淀粉KI溶液變藍是因為I-被ClO-氧化為I2,I2使淀粉變藍
D. 若將Na2SO3溶液加入氯水中,氯水褪色
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】溫度為T℃時,向2.0 L恒容密閉容器中充入2.08 mol PCl5,反應PCl5(g) ![]() PCl3(g) + Cl2(g)經過一段時間后達到平衡。反應過程中測定的部分數據見下表:
PCl3(g) + Cl2(g)經過一段時間后達到平衡。反應過程中測定的部分數據見下表:
t / s | 0 | 50 | 150 | 250 | 350 |
n(PCl3) / mol | 0 | 0. 56 | 0. 75 | 0. 80 | 0. 80 |
回答下列問題:
(1)反應在前50 s 的平均速率v(PCl3)= _______mol/( L·s) 。
(2)T℃時,起始時向容器中充入1. 2 mol PCl5、0. 40 mol PCl3 和0. 20 mol Cl2,反應達到平衡前v(正)__________(選填“>”、“=”或“ <”)v(逆) 。
(3)T℃時,若起始時向容器中充入6. 0 mol PCl3 和6. 0 mol Cl2,達到平衡時,平衡混合氣體中PCl5的體積分數為多少?(寫出解題過程)。_________________
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】NA代表阿伏加德羅常數的值。下列敘述正確的是( )
A. 60g丙醇中存在的共價鍵總數為10NA
B. 1L 0.1mol·L-1的NaHCO3溶液中HCO3-和CO32-離子數之和為0.1NA
C. 鈉在空氣中燃燒可生成多種氧化物。23g鈉充分燃燒時轉移電子數為1NA
D. 235g核互U![]() 發生裂變反應:
發生裂變反應:![]() +
+![]() n
n![]()
![]() +
+![]() +10
+10![]() n,凈產生的中子(
n,凈產生的中子(![]() n)數為10NA
n)數為10NA
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com