
【題目】T℃時,在恒容密閉容器中充入一定量的H2和CO,在催化劑作用下發生如下反應:CO(g)+2H2(g)![]() CH3OH(g)△H<0。反應達到平衡時,CH3OH體積分數與
CH3OH(g)△H<0。反應達到平衡時,CH3OH體積分數與![]() 的關系如圖所示。下列說法正確的是
的關系如圖所示。下列說法正確的是

A. 反應達平衡時,升高體系溫度,CO轉化率升高
B. 反應達平衡時,再充入一定量Ar,平衡右移,平衡常數不變
C. 容器內混合氣體的密度不再變化說明該反應達到平衡狀態
D. ![]() =2.5時達到平衡狀態,CH3OH的體積分數可能是圖中的F點
=2.5時達到平衡狀態,CH3OH的體積分數可能是圖中的F點
科目:高中化學 來源: 題型:
【題目】標準狀況下,向100 mL H2S飽和溶液中通入SO2氣體,所得溶液pH變化如圖中曲線所示。

下列分析正確的是
A. 原H2S溶液的物質的量濃度為0.05 mol/L
B. 氫硫酸的酸性比亞硫酸的酸性強
C. b點水的電離程度比c點水的電離程度大
D. a點對應溶液的導電性比d點強
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】秦皮是一種常用的中藥,具有抗炎鎮痛、抗腫瘤等作用。“秦皮素”是其含有的一種有效成分,結構簡式如下圖所示,有關其性質敘述不正確的是
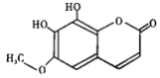
A. 1mol 該化合物最多能與3 mol NaOH 反應 B. 該有機物分子式為C10H8O5
C. 該有機物能發生加成、氧化、取代等反應 D. 分子中有四種官能團
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】短周期元素A、B、C在周期表中所處的位置如圖所示。A、B、C三種元素原子的質子數和為32。D元素原子的最外層電子數是其次外層電子數的2倍。則下列說法正確的是

A. 元素D的某種同位素質量數為14,則其中子數為6
B. 四種元素形成的氣態氫化物中,C元素的氫化物的穩定性最強
C. B、C兩種元素可形成BC6型化合物,該化合物屬于離子化合物
D. A、B兩種元素的氣態氫化物均能與它們對應的最高價氧化物對應的水化物發生反應,且都屬于氧化還原反應
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】某同學為探究元素周期表中元素性質的遞變規律,設計了如下系列實驗。利用如圖裝置可驗證同主族元素非金屬性的變化規律

(1)儀器A的名稱為_____,干燥管D的作用為__________。
(2)若要證明非金屬性:Cl>I,則A中加濃鹽酸,B中加KMnO4(KMnO4與濃鹽酸常溫下反應生成氯氣),C中加淀粉碘化鉀混合溶液,觀察到C中溶液____(填現象),即可證明。從環境保護的觀點考慮,此裝置缺少尾氣處理裝置,可用____溶液吸收尾氣。
(3)若要證明非金屬性:C>Si,則在A中加鹽酸、B中加CaCO3、C中加Na2SiO3溶液,觀察到C中溶液_______(填現象),即可證明。但有的同學認為鹽酸具有揮發性,可進入C中干擾試驗,應在兩裝置間添加裝有______溶液的洗氣瓶除去。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】某溶液中可能含有OH-、CO32-、[Al(OH)4]-、SiO32-、SO42-、Na+、Fe3+、Mg2+、Al3+等離子。當向該溶液中逐滴加入一定物質的量濃度的鹽酸時,發現生成沉淀的物質的量隨鹽酸溶液的體積變化如圖所示。下列說法正確的是
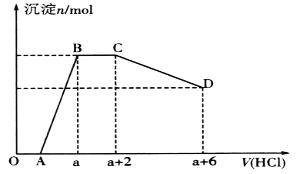
A. BC段是OH-與鹽酸反應
B. 反應后最終溶液中的溶質只有NaC1
C. 原溶液中含有CO32-與[Al(OH)4]-的物質的量之比為3:4
D. 原溶液中一定含有的離子是Na+、OH-、SiO32-、SO42-、[A1(OH)4]-、CO32-
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】X、Y、Z、R、Q、M是六種短周期元素,原子序數依次增大。X是原子半徑最小的元素,Y的氣態氫化物能使濕潤的紅色石蕊試紙變藍,Z為地殼中含量最多的元素,R與X同主族;Y、R、Q最外層電子數之和為8,M的單質為黃綠色有害氣體。請回答下列問題:
(1)R在元素周期表中的位置為__________________。
(2)Z、Q、M簡單離子半徑由大到小的順序為(寫元素離子符號)_____________________。
(3)YX4M的電子式為___________________,Q3Y2與水可劇烈反應,產生沉淀與氣體,反應的化學方程式為___________________________________。
(4)X、Z兩元素形成的原子個數比為1∶1的化合物的結構式____________。
(5)M的單質與R的最高價氧化物對應的水化物反應的離子方程式為_________________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】為了探究原電池和電解池的工作原理,某研究性學習小組分別用下圖所示的裝置進行實驗。據圖回答問題。

I.用圖甲所示裝置進行第一組實驗時:
(1)在保證電極反應不變的情況下,不能替代Cu作電極的是_____ (填字母)。
A石墨 B. 鎂 C.銀 D.鉑
(2)實驗過程中,SO42-____(填“從左向右”“從右向左”或“不”)移動;濾紙上能觀察到的現象是________________。
II.該小組同學用圖乙所示裝置進行第二組實驗時發現,兩極均有氣體產生,且Y極處溶液逐漸變成紫紅色;停止實驗觀察到鐵電極明顯變細,電解液仍然澄清。查閱資料知,高鐵酸根(FeO42-)在溶液中呈紫紅色。請根據實驗現象及所查信息,回答下列問題:
(3)電解過程中,X極處溶液的OH-濃度____(填“增大”“減小”或“不變)。
(4)電解過程中,Y極發生的電極反應為___________________,_________________。
(5)電解進行一段時間后,若在Y電板(鐵電極)質量減小2.8g,在Y極收集到氣體為1.68 L 則X極收集到氣體__________L(均己折算為標準狀況時氣體體積)。
(6)K2FeO4-Zn也可以組成堿性電池,K2FeO4在電池中作為正極材料,其電池反應總反應式為2K2FeO4+3Zn=Fe2O3+ZnO+2K2ZnO2,該電池正極發生的電極反應式為_______________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】在標準狀況下,將aLNH3完全溶于水得到VmL氨水,溶液的密度為ρg/cm3,溶質的質量分數為ω,溶質的物質的量濃度為cmol/L。下列敘述中正確的是()
①![]()
② ![]()
③ 若上述溶液中再加入VmL水后,所得溶質的質量分數大于0.5ω
④ 若上述溶液中再加入0.5mL同濃度稀鹽酸,充分反應后溶液中離子濃度大小關系為:
c(NH4+)>c(Cl-)>c(OH-)>c(H+)
A.①④ B.②③ C.②④ D.①③
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com