
【題目】二氧化氯(ClO2)是一種新型消毒劑,可用氯酸鈉(NaClO3)為原料制備。
(1)隔膜電解法制備ClO2的裝置示意圖如下:

已知:ClO2在酸性溶液中比較穩定,在堿性溶液中不能穩定存在。
①產生O2的電極反應式:________。
②結合反應方程式,簡述ClO2的產生過程:_________。
(2)過氧化氫還原法制備ClO2:![]() 研究發現Cl-對上述反應有影響,實驗記錄如下:
研究發現Cl-對上述反應有影響,實驗記錄如下:
加入NaCl 的濃度/(g·L1) | ClO2的生成速率/(g·L-1·min-1) | 相同時間 | |||
10 min | 30 min | 60 min | ClO2 產率/% | Cl2 的量 | |
0 | 0.0035 | 0.0124 | 0.0159 | 97.12 | 極微量 |
1.00 | 0.0138 | 0.0162 | 0.0163 | 98.79 | 極微量 |
①NaCl的主要作用是_______。
②上述反應可能的過程如下:
反應i:![]() +
+ ![]() + +
+ +
反應ii: Cl2 + H2O2 = 2Cl- + O2↑ + 2H+
將反應i填寫完整_________。
③進一步研究發現,未添加Cl-時,體系中首先會發生反應生成Cl-,反應為:ClO3- + 3H2O2 = Cl- + 3O2↑+3H2O(反應iii)。分析反應i、ii、iii的速率大小關系并簡要說明理由:_________。
(3)國家規定,飲用水中ClO2的殘留量不得高于0.8 mg·L-1,檢測步驟如下:
Ⅰ.取1.0L的酸性水樣,加入過量的碘化鉀,再用氫氧化鈉溶液調至中性,使ClO2轉化為![]() 。加入淀粉溶液,溶液變藍。
。加入淀粉溶液,溶液變藍。
Ⅱ.用0.0010 mol/LNa2S2O3溶液滴定步驟I中產生的I2。已知:步驟II中發生反應的離子方程式是![]()
①步驟I中發生的氧化還原反應的離子方程式是________。
②當步驟II中出現________(填現象)時,停止滴加Na2S2O3溶液,記錄其體積為10.00 mL。
③上述水樣中ClO2的殘留濃度是______mg·L-1。
【答案】![]() 陰極反應:
陰極反應:![]() ,產生的
,產生的![]() 在溶液中與
在溶液中與![]() 發生反應:
發生反應:
![]() 。
。![]() 一部分逸出,一部分循環反應 催化劑
一部分逸出,一部分循環反應 催化劑 ![]() 反應i較快,反應ii 與反應i 速率相當或更快,反應iii 較慢。因為ClO2產率很高并且Cl2的量極微量,并且不添加Cl- 時起始生成ClO2的速率很慢
反應i較快,反應ii 與反應i 速率相當或更快,反應iii 較慢。因為ClO2產率很高并且Cl2的量極微量,并且不添加Cl- 時起始生成ClO2的速率很慢 ![]() 溶液藍色恰好消失,30 s 內不變為藍色 0.675
溶液藍色恰好消失,30 s 內不變為藍色 0.675
【解析】
(1)①氧元素化合價升高產生O2,氧氣在陽極生成;
②根據裝置圖,![]() 在陰極得電子生成
在陰極得電子生成![]() ,
,![]() 與溶液中ClO3-反應生成
與溶液中ClO3-反應生成![]() ;
;
(2)①根據表格數據,可知加入NaCl,生成![]() 的速率明顯增大;
的速率明顯增大;
②總反應-反應ii可得反應i;
③根據ClO2產率很高并且Cl2的量極微量,并且不添加Cl- 時起始生成ClO2的速率很慢分析反應i、ii、iii的速率大小;
(3)①步驟I中ClO2與碘離子反應生成![]() 和碘單質;
和碘單質;
②當碘單質完全反應時,溶液藍色消失;
③根據![]() 、
、![]() ,可知ClO2與
,可知ClO2與![]() 的關系式,根據關系式計算ClO2殘留濃度。
的關系式,根據關系式計算ClO2殘留濃度。
(1)①水中氧元素化合價升高產生O2,氧氣在陽極生成,陽極反應式是![]() ;
;
②根據裝置圖,ClO2的產生過程是:陰極發生反應![]() ,產生的
,產生的![]() 在溶液中與
在溶液中與![]() 發生反應:
發生反應:![]() 。
。![]() 一部分逸出,一部分循環反應;
一部分逸出,一部分循環反應;
(2)根據表格數據,可知加入NaCl,生成![]() 的速率明顯增大,所以NaCl的主要作用是作反應的催化劑;
的速率明顯增大,所以NaCl的主要作用是作反應的催化劑;
②總反應的離子方程式是![]() ,總反應-反應ii可得
,總反應-反應ii可得
![]() ;
;
③根據ClO2產率很高并且Cl2的量極微量,并且不添加Cl- 時起始生成ClO2的速率很慢,所以反應i較快,反應ii 與反應i 速率相當或更快,反應iii 較慢;
(3)①步驟I中ClO2與碘離子反應生成![]() 和碘單質,反應的離子方程式是
和碘單質,反應的離子方程式是![]() ;
;
②當碘單質完全反應時,溶液藍色消失,當步驟II中藍色恰好消失,30 s 內不變為藍色時,達到滴定終點,停止滴加Na2S2O3溶液。
③根據![]() 、
、![]() ,可知ClO2與
,可知ClO2與![]() 的物質的量比是1:1;
的物質的量比是1:1;
設水樣中ClO2的物質的量是nmol;
ClO2―――――![]()
1 1
nmol 0.0010 mol/L×0.01L
解得n=1×10 -5mol;
ClO2的殘留濃度是1×10 -5mol×67.5g/mol×103÷1L=0.675 mg·L-1。


科目:高中化學 來源: 題型:
【題目】實驗室從含碘廢液(除H2O外,含有CCl4、I2、I- 等)中回收碘,實驗過程如下:
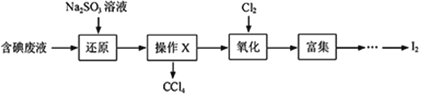
(1)向含碘廢液中加入稍過量的Na2SO3溶液,將廢液中的I2還原為I-,其離子方程式為___________;該操作將I2還原為I-的目的是________。
(2)操作X的名稱為__________。
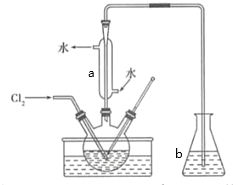
(3)氧化時,在三頸瓶中將含I-的水溶液用鹽酸調至pH約為2,緩慢通入Cl2,在40℃左右反應(實驗裝置如圖所示)。實驗控制在較低溫度下進行的原因是________;儀器a的名稱為__________;儀器b中盛放的溶液為________。
(4)已知:![]() ;某含碘廢水(pH約為8)中一定存在I2,可能存在I-、
;某含碘廢水(pH約為8)中一定存在I2,可能存在I-、![]() 中的一種或兩種。請補充完整檢驗含碘廢水中是否含有I-、IO3-的實驗方案(實驗中可供選擇的試劑:稀鹽酸、淀粉溶液、FeCl3溶液、Na2SO3溶液)。
中的一種或兩種。請補充完整檢驗含碘廢水中是否含有I-、IO3-的實驗方案(實驗中可供選擇的試劑:稀鹽酸、淀粉溶液、FeCl3溶液、Na2SO3溶液)。
①取適量含碘廢水用CCl4多次萃取、分液,直到水層用淀粉溶液檢驗不出有碘單質存在;
②______________________;
③另從水層中取少量溶液,加入1-2mL淀粉溶液,加鹽酸酸化后,滴加Na2SO3溶液,若溶液變藍說明廢水中含有IO3-;否則說明廢水中不含有IO3-。
(5)二氧化氯(ClO2,黃綠色易溶于水的氣體)是高效、低毒的消毒劑和水處理劑。現用氧化酸性含廢液回收碘。完成ClO2氧化I-的離子方程式:_____ClO2+ ____I-+_______=_____![]() +_____Cl-+(_________)________。
+_____Cl-+(_________)________。
(6)“碘量法”是一種測定S2-含量的有效方法。立德粉ZnS·BaSO4是一種常用的白色顏料,制備過程中會加入可溶性的BaS,現用“碘量法”來測定立德粉樣品中S2-的含量。稱取m g樣品,置于碘量瓶中,移取25.00mL 0.1000mol/L 的I2-KI溶液于其中,并加入乙酸溶液,密閉,置暗處反應5min,有單質硫析出。以淀粉為指示劑,過量的I2用0.1000mol/L Na2S2O3 滴定,反應式為![]() 。測定消耗Na2S2O3溶液體積V mL。立德粉樣品S2-含量為__________(寫出表達式)
。測定消耗Na2S2O3溶液體積V mL。立德粉樣品S2-含量為__________(寫出表達式)
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】某溫度下,將pH和體積均相同的HCl和CH3COOH溶液分別加水稀釋,其pH隨加水體積的變化如圖所示。下列敘述正確的是
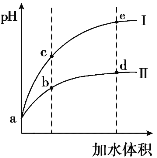
A.曲線II代表HCl的稀釋過程
B.溶液中水的電離程度:b點>c點
C.從b點到d點,溶液中![]() 保持不變
保持不變
D.該溫度下,b點Kw的數值比e點大
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】CO2資源化利用的方法之一是合成二甲醚(CH3OCH3)。
(1)CO2 催化加氫合成二甲醚的過程中主要發生下列反應:反應I:CO2(g) + H2(g) ![]() CO(g) + H2O(g) H= +41.2 kJmol-1;反應II: 2CO2(g) + 6H2(g)
CO(g) + H2O(g) H= +41.2 kJmol-1;反應II: 2CO2(g) + 6H2(g) ![]() CH3OCH3(g) + 3H2O(g) H = - 122.5 kJmol-1;其中,反應II 分以下①②兩步完成,請寫出反應①的熱化學方程式。
CH3OCH3(g) + 3H2O(g) H = - 122.5 kJmol-1;其中,反應II 分以下①②兩步完成,請寫出反應①的熱化學方程式。
① _____
②2 CH3OH(g) ![]() CH3OCH3(g) + H2O(g) H = -23.5 kJmol-1
CH3OCH3(g) + H2O(g) H = -23.5 kJmol-1
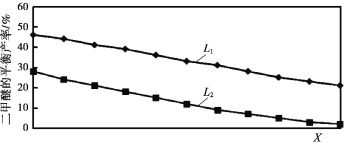
(2)L(L1、L2)、X分別代表壓強或溫度,如圖表示L一定時,反應II中二甲醚的平衡產率隨X變化的關系,其中X代表的物理量是_____。判斷L1、L2的大小,并簡述理由:_____。
(3)恒壓時,在CO2和H2起始量一定的條件下,CO2平衡轉化率和平衡時CH3OCH3的選擇性![]() )隨溫度變化如圖。
)隨溫度變化如圖。
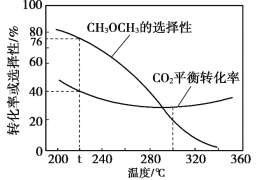
①t ℃ 時,起始投入a molCO2,b mol H2,達到平衡時反應II消耗的H2的物質的量為______mol。
②溫度高于300℃,CO2平衡轉化率隨溫度升高而增大的原因是______。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】某消毒液的主要成分為NaClO,還含有一定量的NaOH,下列用來解釋事實的方程式中不合理的是(已知:飽和NaClO溶液的pH約為11)
A. 該消毒液可用NaOH溶液吸收Cl2制備:Cl2+2OH-="==" Cl-+ ClO-+ H2O
B. 該消毒液的pH約為12:ClO-+ H2O![]() HClO+ OH-
HClO+ OH-
C. 該消毒液與潔廁靈(主要成分為HCl)混用,產生Cl2:2H++ Cl-+ ClO-= Cl2↑+H2O
D. 該消毒液加白醋生成HClO,可增強漂白作用:CH3COOH+ ClO-= HClO+CH3COO—
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】Ⅰ.CO2是重要的化工原料,也是應用廣泛的化工產品。CO2與過氧化鈉或超氧化鉀反應可產生氧氣。完成下列計算:
(1)CO2通入氨水生成NH4HCO3,NH4HCO3很容易分解。2.00mol NH4HCO3完全分解,分解產物經干燥后的體積為_________L(標準狀況)。
(2)某H2中含有2.40 molCO2,該混合氣體通入2.00 L NaOH溶液中,CO2被完全吸收。如果NaOH完全反應,該NaOH溶液的濃度為_______。
(3)CO2和KO2有下列反應:
4KO2+2CO2→2K2CO3+3O2 4KO2+4CO2+2H2O→4KHCO3+3O2
若9 mol CO2在密封艙內和KO2反應后生成9 molO2,則反應前密封艙內H2O的量應該是______________。
(4)甲烷和水蒸氣反應的產物是合成甲醇的原料:CH4+H2O![]() CO+3H2
CO+3H2
已知:CO+2H2![]() CH3OH CO2+3H2
CH3OH CO2+3H2![]() CH3OH+H2O
CH3OH+H2O
300 mol CH4完全反應后的產物中,加入100 mol CO2后合成甲醇。若獲得甲醇350 mol,殘留氫氣120 mol,計算CO2的轉化率_______
Ⅱ.氨堿法制純堿包括石灰石分解、粗鹽水精制、氨鹽水碳酸化等基本步驟。完成下列計算:
(5)CaCO3質量分數為0.90的石灰石100 kg完成分解產生CO2_______L(標準狀況)。石灰窯中,該石灰石100 kg與焦炭混合焙燒,產生CO2 29120 L(標準狀況),如果石灰石中碳酸鈣完全分解,且焦炭完全燃燒,不產生CO,則焦炭的物質的量為_______mol。
(6)已知粗鹽水含MgCl2 6.80 mol/m3,含CaCl2 3.00mol/m3。向粗鹽水中加入Ca(OH)2除鎂離子:MgCl2 + Ca(OH)2 → Mg(OH)2↓ + CaCl2然后加入Na2CO3除鈣離子。處理上述粗鹽水10 m3,至少需要加Na2CO3______g。如果用碳酸化尾氣(含NH3體積分數為0.100、CO2體積分數0.040)代替碳酸鈉,發生如下反應:Ca2+ + 2NH3 + CO2 + H2O → CaCO3↓ + 2NH4+處理上述10 m3粗鹽水至少需要通入_____________L(標準狀況)碳酸化尾氣。
(7)某氨鹽水含氯化鈉1521 kg,通入二氧化碳后析出碳酸氫鈉晶體,過濾后溶液中含氯化銨1070 kg。
①過濾后溶液中氯化鈉的質量______________。
②析出的碳酸氫鈉晶體的質量__________________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】—定溫度下,水溶液中H+和OH-的濃度變化曲線如圖,下列說法正確的是( )

A. 升高溫度,可能引起由c向b的變化
B. 該溫度下,水的離子積常數為l.0×10-13
C. 該溫度下,加入FeCl3可能引起由b向a的變化
D. 該溫度下,稀釋溶液可能引起由c向d的變化
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】如圖所示是部分短周期元素原子半徑與原子序數的關系,則下列說法正確的是( )
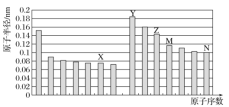
A.Z、N兩種元素形成的化合物是離子化合物
B.通過M、N含氧酸的酸性強弱,可以比較兩者的非金屬性
C.Z的氧化物能分別溶解于Y的氫氧化物和N的氫化物的水溶液中
D.由X與M兩種元素組成的化合物能與水反應
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】電解質的水溶液中存在電離平衡。
(1)醋酸是常見的弱酸。
①醋酸在水溶液中的電離方程式為____________。
②下列方法中,可以使醋酸溶液中CH3COOH電離程度增大的是_______(填字母序號)。
a 滴加少量濃鹽酸 b 微熱溶液
c 加水稀釋 d 加入少量醋酸鈉晶體
(2)用0.1 mol·L-1 NaOH溶液分別滴定體積均為20mL、濃度均為0.1 mol·L-1的鹽酸和醋酸溶液,得到滴定過程中溶液pH隨加入NaOH溶液體積而變化的兩條滴定曲線。
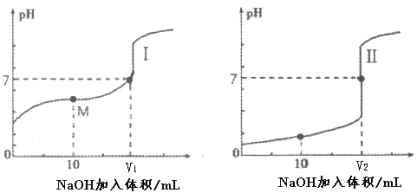
①滴定醋酸的曲線是___________(填“I”或“Ⅱ”)。
②滴定開始前,0.1 mol·L-1 NaOH、0.1 mol·L-1的鹽酸和0.1 mol·L-1醋酸三種溶液中由水電離出的c(H+)最大的是_______溶液。
③圖I中,V=10時,溶液中的c(H+)_________c(OH-) (填“>”、“=”或“<”,下同),c(Na+)_________c(CH3COO-)。
(3)下表為某同學所測25℃時,甲、乙兩種溶液的pH。
甲 | 乙 | |
pH | 11 | 11 |
溶液 | 氨水 | 氫氧化鈉溶液 |
①甲溶液中的c(OH-) =___________mol/L。
②25℃時,等體積的甲、乙兩溶液與等濃度的鹽酸反應,消耗的鹽酸體積:甲_____乙。
③甲、乙溶液均加水稀釋10倍后,所得溶液的pH:甲_____乙。
(4)煤炭工業中經常會產生大量SO2,為防止污染環境,常采用吸收法進行處理。以下物質可用于吸收SO2的是____________。
A H2O2 B Na2CO3 C Na2SO3 D Ca(OH)2
(5)下表是幾種常見弱酸的電離常數
化學式 | CH3COOH | H2SO3 | HClO | H2CO3 |
電離 常數 | 1.8×10-5 | K1=1.23×10-2 K2=6.6×10-8 | 3.0×10-8 | K1=4.4×10-7 K2=4.7×10-11 |
/span>
以下反應對應的離子方程式正確的是___________。
A Na2CO3溶液吸收少量SO2:CO32-+SO2+H2O = SO32-+HCO3-
B 漂白液生效的原理:ClO-+CO2+H2O = HClO+HCO3-
C 次氯酸鈉溶液吸收少量SO2:ClO-+SO2+H2O = HClO+SO32-
D 醋酸除水垢中的CaCO3:2CH3COOH+CaCO3 = Ca2++2CH3COO-+H2O+CO2↑
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com