
【題目】下列說法正確的是
A.按系統命名法,化合物![]() 的名稱是2,3,5,5-四甲基-4,4-二乙基己烷
的名稱是2,3,5,5-四甲基-4,4-二乙基己烷
B.等物質的量的苯和苯甲酸完全燃燒消耗氧氣的量不相等
C.苯和甲苯互為同系物,均能使KMnO4酸性溶液褪色
D.結構片段 的高聚物,其單體是苯酚和甲醛
的高聚物,其單體是苯酚和甲醛
 孟建平錯題本系列答案
孟建平錯題本系列答案 超能學典應用題題卡系列答案
超能學典應用題題卡系列答案科目:高中化學 來源: 題型:
【題目】NiCl2是化工合成中最重要的鎳源,在實驗室中模擬工業上以金屬鎳廢料(含Fe、Al等雜質)為原料生產NiCl2的工藝流程如下:
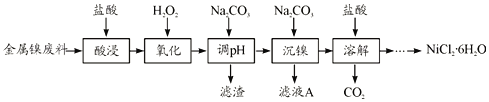
下表列出了相關金屬離子生成氫氧化物沉淀的pH
氫氧化物 | Fe(OH)3 | Fe(OH)2 | Al(OH)3 | Ni(OH)2 |
開始沉淀的pH | 2.1 | 6.5 | 3.7 | 7.1 |
沉淀完全的pH | 3.3 | 9.7 | 4.7 | 9.2 |
(1)為了提高鎳元素的浸出率,在“酸浸”時可采取的措施有__________(寫一條即可)。
(2)加入H2O2時發生主要反應的離子方程式為__________。
(3)“調pH”時,控制溶液pH的范圍為__________。
(4)“沉鎳”過程中,若濾液A中c(Ni2+)=1.0mol/L,欲使100mL該濾液中的Ni2+沉淀完全[即溶液中c(Ni2+)≤1.0×10-5],則需用托盤天平稱取Na2CO3固體的質量至少為_____g。(已知Ksp(NiCO3)=6.5×10-6,忽略溶液體積的變化)
(5)流程中由溶液得到NiCl2·6H2O的實驗操作步驟依次為______、過濾、洗滌、干燥。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】(2017·天津卷)常壓下羰基化法精煉鎳的原理為:Ni(s)+4CO(g)![]() Ni(CO)4(g)。230℃時,該反應的平衡常數K=2×105。已知:Ni(CO)4的沸點為42.2℃,固體雜質不參與反應。
Ni(CO)4(g)。230℃時,該反應的平衡常數K=2×105。已知:Ni(CO)4的沸點為42.2℃,固體雜質不參與反應。
第一階段:將粗鎳與CO反應轉化成氣態Ni(CO)4;
第二階段:將第一階段反應后的氣體分離出來,加熱至230℃制得高純鎳。
下列判斷正確的是
A. 增加c(CO),平衡向正向移動,反應的平衡常數增大
B. 第二階段,Ni(CO)4分解率較低
C. 第一階段,在30℃和50℃兩者之間選擇反應溫度,選50℃
D. 該反應達到平衡時,v生成[Ni(CO)4]=4v生成(CO)
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】第四周期包含18種元素,其中多種元素具有重要的用途,在現代工業中備受青睞。
(l)鐵位于元素周期表____區,Fe3+的價電子排布式為 ____。
(2)乙二胺(H2NCH2CH2NH2)是一種有機化合物,可用en代表,其能夠與Cu2+形成穩定環狀配離子,可表示為[Cu(en)2]2+,其中Cu2+的配位數為____。1 mol[Cu(en)2]C12中含有σ鍵的數目為____。
(3)氣態SeO3為單分子,該分子中Se原子的雜化軌道類型為 ___。用物質結構理論解釋H2SeO4比H2SeO3酸性強的原因:______________。
(4)如圖為Cu2O的晶胞結構,其中黑球表示____原子(填元素符號);Cu2O的密度為pg·cm-3則晶胞的邊長為 ___cm。(用NA表示阿伏加德羅常數的值)
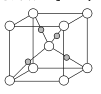
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】A、B、C、D、E、F、G 為短周期主族元素,其原子半徑與最外層電子數的關系如圖,下列說法正確的是
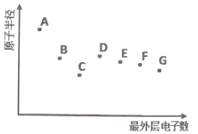
A.根據元素B 在元素周期表中的位置推測,其最高價氧化物對應的水化物可能具有兩性
B.元素D在自然界中主要以游離態存在,其單質可用作半導體材料
C.元素A的離子半徑大于元素G的離子半徑
D.元素F 的氣態氫化物比元素G的氣態氫化物更穩定
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】溶液X 中含有下表中離子若干種,且離子濃度均為相等(不考慮水的電離與離子水解)。向X 中加入足量稀鹽酸,有無色氣體生成, 經分析反應前后陰離子種類沒有變化,下列說法正確的是
陽離子 | Na+、Ca2+ 、Fe3+、Fe2+、Al3+、Mg2+ |
陰離子 | OH-、 |
A.溶液X 中可能有![]() 或
或![]() 中的一種或兩種都有
中的一種或兩種都有
B.溶液X 中是否有Na+不能確定,需通過焰色反應來確定
C.溶液X 中可能有2 種陽離子,3 種陰離子
D.原溶液一定沒有Al3+、Fe 3+,但Na+,、![]() 不確定
不確定
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】現有一包鋁粉和銅粉的混合物,用100mL 某濃度的稀硝酸溶解,生成的氣體全部是NO, 待粉末完全溶解后,逐滴加入3molL-1 的氨水,產生沉淀的物質的量與加入氨水的體積關系如圖。
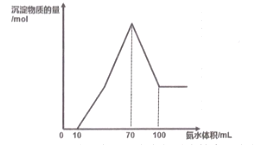
(1)寫出圖中滴加氨水10~100mL 的過程中銅元素參與反應的離子方程式_________。
(2)所用硝酸的物質的量濃度為______mol L-1;寫出簡要計算過程______。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】淀粉在一定條件下發生下列轉化關系:

已知:化合物H中含有一個甲基。請回答:
(1)寫出B的電子式___;化合物D中的官能團名稱___。
(2)E+H→G的化學方程式:___。
(3)下列說法不正確的是___。
A.化合物A和D能與銀氨溶液反應生成光亮的銀鏡
B.用新制的氫氧化銅不能區分化合物C、D、E
C.相同質量的A、E和H充分燃燒時消耗等量的氧氣
D.化合物F與G互為同分異構體
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】圖Ⅰ是NO2(g)+CO(g)CO2(g)+NO(g)應過程中能量變化的示意圖。一定條件下,在固定容積的密閉容器中該反應達到平衡狀態當改變其中一個條件X,Y隨X的變化關系曲線如圖Ⅱ所示。
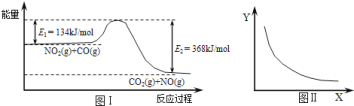
下列有關說法正確的是
A.一定條件下,向密閉容器中加入1 mol NO2(g)與1 mol CO(g)反應放出234kJ熱量
B.若X表示溫度,則Y表示的可能是CO2的物質的量濃度
C.若X表示CO的起始濃度,則Y表示的可能是NO2的轉化率
D.若X表示反應時間,則Y表示的可能是混合氣體的密度
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com