
【題目】常溫常壓下,一氧化二氯(Cl2O)為棕黃色氣體,沸點為3.8 ℃,42 ℃以上會分解生成Cl2和O2,Cl2O易溶于水并與水反應生成HClO。
(制備產品)
將氯氣和空氣(不參與反應)按體積比1∶3混合通入含水8%的碳酸鈉中制備Cl2O,并用水吸收Cl2O(不含Cl2)制備次氯酸溶液。

(1)各裝置的連接順序為___→___→___→________→____。___________
(2)裝置B中多孔球泡和攪拌棒的作用是_;裝置C的作用是__。
(3)制備Cl2O的化學方程式為___。
(4)反應過程中,裝置B需放在冷水中,其目的是___。
(5)此方法相對于用氯氣直接溶于水制備次氯酸溶液有兩個主要優點,分別是____。
(測定濃度)
(6)已知次氯酸可被FeSO4等物質還原。用下列實驗方案測定裝置E所得溶液中次氯酸的物質的量濃度:量取10 mL上述次氯酸溶液,并稀釋至100 mL,再從其中取出10.00 mL于錐形瓶中,并加入10.00 mL 0.80 mol·L-1的FeSO4溶液,充分反應后,用0.050 00 mol·L-1的酸性KMnO4溶液滴定至終點,消耗KMnO4溶液24.00 mL,則原次氯酸溶液的濃度為___。
【答案】ADBCE加快反應速率,使反應充分進行除去Cl2O中的Cl22Cl2+Na2CO3===Cl2O+2NaCl+CO2(或2Cl2+Na2CO3+H2O===Cl2O+2NaCl+2NaHCO3)防止反應放熱后溫度過高導致Cl2O分解制得的次氯酸溶液純度較高,濃度較大1.000mol·L-1
【解析】
A裝置用二氧化錳和濃鹽酸制備氯氣,由D裝置飽和食鹽水吸收氯氣中的氯化氫氣體,與空氣形成1:3的混合氣體通入B裝置,防止反應放熱后溫度過高導致Cl2O分解,裝置B需放在冷水中,在攪拌棒的作用下與含水8%的碳酸鈉充分反應制備Cl2O,反應為:2Cl2+Na2CO3═Cl2O+2NaCl+CO2,通入C裝置吸收除去Cl2O中的Cl2,并在E裝置中用水吸收Cl2O制備次氯酸溶液,據此分析作答。
(1)A裝置制備氯氣,D裝置吸收吸收氯氣中的氯化氫氣體,與空氣形成1:3的混合氣體通入B裝置,與含水8%的碳酸鈉充分反應制備Cl2O,C裝置吸收除去Cl2O中的Cl2,E裝置中用水吸收Cl2O制備次氯酸溶液;故答案為:A、D、B、C、E;(2)裝置B中多孔球泡和攪拌棒的作用是加快反應速率,使反應充分進行;裝置C裝置有足量的四氯化碳溶液,其作用是除去Cl2O中的Cl2;(3)氯氣和空氣(不參與反應)按體積比1:3混合通入含水8%的碳酸鈉中制備Cl2O,反應為:2Cl2+Na2CO3═Cl2O+2NaCl+CO2或2Cl2+Na2CO3+H2O═Cl2O+2NaCl+2NaCO3;(4)由題可知:Cl2O 42℃以上會分解生成Cl2和O2,故為防止反應放熱后溫度過高導致Cl2O分解,裝置B需放在冷水中;(5)此方法相對于用氯氣直接溶于水制備次氯酸溶液有兩個主要優點,分別是制得的次氯酸溶液純度較高,濃度較大;(6)根據反應H2O+ClO-+2Fe2+=Cl-+2Fe3++2OH-、MnO4-+5Fe2++8H+=Mn2++5Fe3++4H2O,則原次氯酸溶液的濃度為![]() =1.000mol·L-1。
=1.000mol·L-1。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小學生10分鐘應用題系列答案
小學生10分鐘應用題系列答案科目:高中化學 來源: 題型:
【題目】某化學研究性學習小組對某無色水樣的成分進行檢驗,已知該水樣中只可能含有K+、Mg2+、Fe3+、Cu2+、Al3+、Ag+、Ca2+、CO![]() 、SO
、SO![]() 、Cl﹣中的若干種離子.該小組同學取100mL水樣進行實驗,向水樣中先滴加硝酸鋇溶液,再滴加1mol/L的硝酸,實驗過程中沉淀質量的變化情況如下圖所示:(提示:Al3+與CO
、Cl﹣中的若干種離子.該小組同學取100mL水樣進行實驗,向水樣中先滴加硝酸鋇溶液,再滴加1mol/L的硝酸,實驗過程中沉淀質量的變化情況如下圖所示:(提示:Al3+與CO![]() 不共存)
不共存)

(1)水樣中一定含有的陰離子是_____,其物質的量濃度之比為_____.
(2)寫出BC段所表示反應的離子方程式:_____.
(3)由B到C點變化過程中消耗硝酸的體積為_____.
(4)試根據實驗結果推測K+是否存在?_____(填“是”或“否”);若存在,K+的物質的量濃度c(K+)的范圍是_____.(若K+不存在,則不必回答該問).
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】一定溫度下,向一個容積為3L的真空密閉容器中通入1molN2和3molH2,2min后,測得容器內的壓強是開始時的0.8倍,則這段時間內V(H2)為( )
A.0.2mol/(L·min)B.0.6mol/(L·min)
C.0.1mol/(L·min)D.0.3mol/(L·min)
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下表是元素周期表的一部分,針對表中的①~⑩中元素,用元素符號或化學式填空回答以下問題:
IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 | |
二 | ① | ② | ||||||
三 | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ||
四 | ⑨ | ⑩ |
(1)化學性質最不活潑的元素原子的原子結構示意圖為________;
(2)比較元素①、②的簡單氫化物的穩定性______________________(用化學式表示);
(3)元素的最高價氧化物對應的水化物中酸性最強的是________,堿性最強的是_______,呈兩性的氫氧化物是_______________,(填寫化學式) 元素③的最高價氧化物對應水化物中含有的化學鍵類型為________________;
(4)在③~⑦元素中,簡單離子半徑最小的是_________;
(5) Na2O2的電子式為___________;CO2的電子式為_________;
(6)在⑦與⑩的單質中,氧化性較強的是_______________,用化學反應方程式證明:_____________________________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列物質之間的相互關系錯誤的是( )
A. O2和O3互為同素異形體
B. 12C和14C互為同位素
C. CH3CH2OH和CH3OCH3互為同分異構體
D. CH3COOCH3和HCOOCH2CH3為同一種物質
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】某有機物X的合成路線如下圖所示。請回答下列問題:
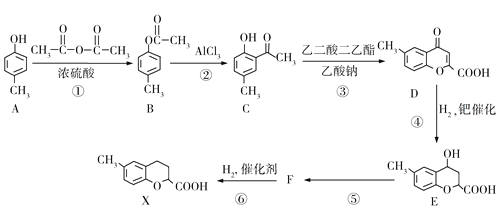
(1)A的名稱是________________,X的分子式為_____________。
(2)B的核磁共振氫譜中所有峰的面積之比是________________。
(3)有機物D中含氧官能團的名稱是________________,④的反應類型為________________。
(4)反應①的化學方程式為________________________________。
(5)有機物F的結構簡式為________________________________。
(6)滿足下列條件的C的同分異構體有_____種,任寫出其中一種的結構簡式_________。
①苯環上只有三個取代基;
②能與三氯化鐵溶液反應顯色;
③可以發生銀鏡反應。
查看答案和解析>>
科目:高中化學 來源: 題型:
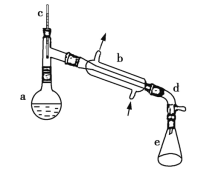
【題目】醇脫水是合成烯烴的常用方法,實驗室合成環己烯的反應和實驗裝置如圖所示。
![]()
![]()
![]() +H2O
+H2O
可能用到的有關數據如下:
相對分子質量 | 密度/(g·cm3) | 沸點/℃ | 溶解性 | |
環己醇 | 100 | 0.961 8 | 161 | 微溶于水 |
環己烯 | 82 | 0.810 2 | 83 | 難溶于水 |
合成反應:
在a中加入20 g環己醇和2小片碎瓷片,冷卻攪動下慢慢加入1 mL 濃硫酸。b中通入冷卻水后,開始緩慢加熱a,控制餾出物的溫度不超過90 ℃。
分離提純:
反應粗產物倒入分液漏斗中,分別用少量5%碳酸鈉溶液和水洗滌,分離后加入無水氯化鈣顆粒,靜置一段時間后棄去氯化鈣。最終通過蒸餾得到純凈環己烯10 g。
回答下列問題:
(1)裝置b的名稱是___________________。
(2)加入碎瓷片的作用是___________________;如果加熱一段時間后發現忘記加瓷片,應該采取的正確操作是___________________ (填正確答案標號)。
A.立即補加 B.冷卻后補加 C.不需補加 D.重新配料
(3)分液漏斗在使用前須清洗干凈并___________________;在本實驗分離過程中,產物應該從分液漏斗的___________________ (填“上口倒出”或“下口放出”)。
(4)分離提純過程中加入無水氯化鈣的目的是___________________。
(5)在環己烯粗產物蒸餾過程中,不可能用到的儀器有____________ (填正確答案標號)。
A.圓底燒瓶 B.溫度計 C.吸濾瓶 D.球形冷凝管 E.接收器
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】![]() 是重要的核工業原料。下列有關
是重要的核工業原料。下列有關![]() 、
、![]() 說法正確的是
說法正確的是
A. ![]() 原子核中含有92個中子 B.
原子核中含有92個中子 B. ![]() 原子核外有143個電子
原子核外有143個電子
C. ![]() 與
與![]() 互為同位素 D.
互為同位素 D. ![]() 與
與![]() 互為同素異形體
互為同素異形體
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】原子序數大于4的主族元素Xm+、Yn-的離子核外電子層結構相同,則關于X、Y兩元素的敘述正確的是
A. X的原子序數小于Y的原子序數 B. X、Y的核電荷數之差是(m-n)
C. X和Y處于同一周期 D. Y元素與X元素的族序數之差是8-(m+n)
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com