
【題目】研究高效催化劑是解決汽車尾氣中的 NO 和 CO 對大氣污染的重要途徑。
(1)已知:C(s)+O2(g)=CO2(g) △H1=-393.5 kJ/mol
C(s)+![]() O2(g)= CO(g) △H2= -110.5 kJ/mol
O2(g)= CO(g) △H2= -110.5 kJ/mol
N2(g)+ O2(g)=2NO(g) △H3= +180.0 kJ/mol
則汽車尾氣的催化轉化反應 2NO(g)+ 2CO(g)=N2(g)+ 2CO2(g)的△H =_______kJ/mol。
(2)400℃時,在分別裝有催化劑 A 和 B 的兩個容積為 2 L 的剛性密閉容器中,各充入物質的量均為nmol的NO和CO發生上述反應。通過測定容器內總壓強隨時間變化來探究催化劑對反應速率的影響,數據如下表:
時間/min | 0 | 10 | 20 | 30 | ∞ |
A容器內壓強/kPa | 75.0 | 70.0 | 65.0 | 60.0 | 60.0 |
B容器內壓強/kPa | 75.0 | 71.0 | 68.0 | 66.0 | 60.0 |
①由上表可以判斷催化劑 __________(填“A”或“B”) 的效果更好。
②容器中CO 的平衡轉化率為 __________。400℃時,用壓強表示的平衡常數Kp__________(kPa)-1 (保留兩位小數)。
③汽車尾氣排氣管中使用催化劑可以提高污染物轉化率,其原因是 __________。
(3)為研究氣缸中NO的生成, 在體積可變的恒壓密閉容器中,高溫下充入物質的量均為 1mol 的氮氣和氧氣,發生反應 N2(g)+ O2(g)2NO(g)。
①下列說法能表明該反應已經達到平衡狀態的是_________(填序號)。
A.2v正(O2)= v逆(NO) B.混合氣體的平均相對分子質量不變
C.c(N2):c(O2)=l D.容器內溫度不變
②為減小平衡混合氣中 NO 的體積分數, 可采取的措施是 ___________。
(4)對于氣缸中N的生成,化學家提出了如下反應歷程:
第一步 O22O 慢反應
第二步 O+N2NO+N 較快平衡
第三步 N+O2NO+O 快速平衡
下列說法錯誤的是_______(填標號)。
A.第一步反應不從N2分解開始,是因為N2比O2穩定
B.N、O 原子均為該反應的催化劑
C.三步反應中第一步反應活化能最大
D.三步反應的速率都隨溫度升高而增大
【答案】-794.5 A 80% 4.27 排氣管是敝口容器,管中進行的反應為非平衡態,該非平衡條件下,反應速率越快,相同時間內污染物轉化率就越高 AD 降低溫度 B
【解析】
(1)已知:①C(s)+O2(g)=CO2(g) △H1=-393.5 kJ/mol
②C(s)+![]() O2(g)= CO(g) △H2= -110.5 kJ/mol
O2(g)= CO(g) △H2= -110.5 kJ/mol
③N2(g)+ O2(g)=2NO(g) △H3= +180.0 kJ/mol
根據蓋斯定律,2×①-(2×②+③)得2NO(g)+ 2CO(g)=N2(g)+ 2CO2( g) △H=-393.5 kJ/mol×2-(-110.5 kJ/mol)×2 -180.0 kJ/mol=-794.5 kJ/mol,故答案為:-794.5;
(2)①根據表中數據分析A容器中反應先達到平衡,則催化劑A的效果更好,故答案為:A;
②設平衡時反應的CO的物質的量為x,則
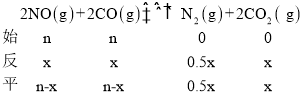
則![]() ,解得x=
,解得x=![]() ,CO的平衡轉化率為
,CO的平衡轉化率為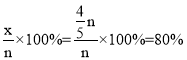 ;平衡時NO、CO、N2、CO2的物質的量分別為
;平衡時NO、CO、N2、CO2的物質的量分別為![]() 、
、![]() 、
、![]() 、
、![]() ,則各物質的分壓分別為
,則各物質的分壓分別為![]() 、
、![]() 、
、![]() 、
、![]() ,
,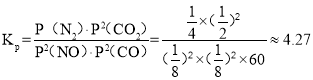 (kPa)-1,故答案為:80%;4.27;
(kPa)-1,故答案為:80%;4.27;
③汽車尾氣排氣管中使用催化劑可以提高污染物轉化率,其原因是排氣管是敝口容器,管中進行的反應為非平衡態,該非平衡條件下,反應速率越快,相同時間內污染物轉化率就越高,故答案為:排氣管是敝口容器,管中進行的反應為非平衡態,該非平衡條件下,反應速率越快,相同時間內污染物轉化率就越高;
(3)①A. 2v正(O2)= v逆(NO)=2v逆(O2),正反應速率等于逆反應速率,則說明反應達到平衡狀態,故A選;
B. 混合氣體的平均相對分子質量始終保持不變,所以B不選;
C. c(N2):c(O2)=l不能說明反應物、生成物的濃度保持不變,故C不選;
D 該反應伴隨著能量不變,該容器內溫度不變,說明轉化率不變,能說明反應達到平衡狀態,故D
②該反應為吸熱反應,降低溫度平衡逆反應方向移動,NO的體積分數降低,故答案為:降低溫度;
(4)A. 根據題給反應機理分析,N2比O2穩定,所以第一步反應不從N2分解開始,故A正確;
B. 根據反應歷程分析,O 原子為該反應的催化劑,故B錯誤;
C. 三步反應中第一步反應速率最慢,說明活化能最大,故C正確;
D. 溫度升高,增大活化分子百分數,所以三步反應的速率都隨溫度升高而增大,故D正確;故答案為:B。


科目:高中化學 來源: 題型:
【題目】二甲醚(CH3OCH3)是一種氣體麻醉劑,可由“可燃冰”為原料合成。回答下列問題:
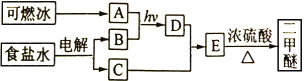
(1)B為黃綠色氣體,其化學名稱為____________。
(2)由A和B生成D的化學方程式為__________________。
(3)E的結構簡式為____________。
(4)由E生成二甲醚的反應類型為______________________。
(5)二甲醚的同分異構體的結構簡式為_____________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】化合物如圖的分子式均為C7H8。下列說法正確的是
![]()
A. W、M、N均能與溴水發生加成反應B. W、M、N的一氯代物數目相等
C. W、M、N分子中的碳原子均共面D. W、M、N均能使酸性KMnO4溶液褪色
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】取1mL 0.1mol·L-1AgNO3溶液進行如下實驗(實驗中所用試劑濃度均為0.1mol·L![]() ):
):
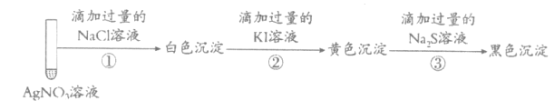
下列說法不正確的是
A.實驗①白色沉淀是難溶的AgCl
B.由實驗②說明AgI比AgCl更難溶
C.若按①③②順序實驗,看不到黑色沉淀
D.若按②①③順序實驗,看不到白色沉淀
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】以含鋰電解鋁廢渣(主要含 AlF3、 NaF、LiF、CaO ) 和濃硫酸為原料,制備電池級碳酸鋰,同時得副產品冰晶石,其工藝流程如下:

已知LiOH易溶于水,Li2CO3微溶于水。回答下列問題:
(1)電解鋁廢渣與濃硫酸反應產生的氣體化學式為 ___________。濾渣2的主要成分是(寫化學式)_________。
(2)堿解反應中, 同時得到氣體和沉淀反應的離子方程式為_____________。
(3)一般地說 K>105 時,該反應進行得就基本完全了。苛化反應中存在如下平衡:Li2CO3(s)+Ca2+(aq)2Li+(aq)+ CaCO3(s)通過計算說明該反應是否進行完全________(已知Ksp(Li2CO3) = 8.64×10-4、Ksp(CaCO3) = 2.5×10-9)。
(4)碳化反應后的溶液得到Li2CO3的具體實驗操作有:加熱濃縮、______、______、干燥。
(5)上述流程得到副產品冰晶石的化學方程式為__________。
(6)Li2CO3是制備金屬鋰的重要原料, 一種制備金屬鋰的新方法獲得國家發明專利,其裝置如圖所示:

工作時電極 C 應連接電源的______極,陽極的電極反應式為__________ 。該方法設計的 A 區能避免熔融碳酸鋰對設備的腐蝕和因________逸出對環境的污染。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】25℃,向20.00mL 0.100 mol·L![]() HX中滴加0.100 mol·L
HX中滴加0.100 mol·L![]() NaOH過程中,pH變化如下圖所示。
NaOH過程中,pH變化如下圖所示。
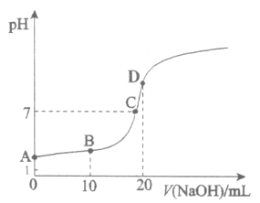
(1)寫出HX的電離方程式:__________。
(2)下列有關B點溶液的說法正確的是__________(填字母序號)。
a. 溶質為:HX、NaX
b. 微粒濃度滿足:c(Na+)+c(H+)=c(X-)+c(OH-)
c. 微粒濃度滿足:c(Na+)=c(HX)+c(X-)
d. 微粒濃度滿足:c(X-)>c(Na+)>c(H+)>c(OH-)
(3)A、C兩點水的電離程度:A__________C(填“>”、“<”或“=”)。
(4)C點對應離子濃度由大到小的順序為__________。
(5)用離子方程式解釋D點溶液pH>7的原因:_______。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】四甲基氫氧化銨[(CH3)4NOH]是強堿,常溫下甲胺(CH3NH2·H2O)的電離常數為Kb,且pKb=-lgKb=3.38。常溫下,在體積均為20mL、濃度均為0.1mol·L-1的四甲基氫氧化銨溶液和甲胺溶液,分別滴加濃度為0.1mol·L-1的鹽酸,溶液的導電率與鹽酸體積的關系如圖所示。
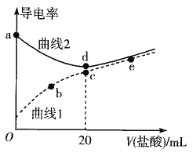
下列說法正確的是
A. 曲線1代表四甲基氫氧化銨溶液
B. 在b、c、e三點中,水的電離程度最大的點是e
C. b點溶液中存在c(H+)=c(OH-)+c(CH3NH2·H2O)
D. 常溫下,CH3NH3Cl水解常數的數量級為10-11
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】某化學科研小組研究在其他條件不變時,改變某一條件對化學平衡的影響,得到如圖所示變化規律(p表示壓強,T表示溫度,n表示物質的量):
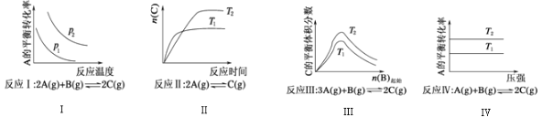
根據以上規律判斷,下列結論正確的是( )
A.反應Ⅰ:△H>0,p2>p1
B.反應Ⅲ:△H>0,T2>T1或△H<0,T2<T1
C.反應Ⅱ:△H>0,T1>T2
D.反應Ⅳ:△H<0,T2>T1
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】一種釕(Ru)基配合物光敏染料敏化太陽能電池的工作原理及電池中發生的主要反應如圖所示。下列說法錯誤的是

A. 電池工作時,光能轉變為電能,X為電池的負極
B. 鍍鉑導電玻璃上發生氧化反應生成I-
C. 電解質溶液中發生反應:2Ru3++3I-![]() 2Ru2++I3-
2Ru2++I3-
D. 電池工作時,電解質溶液中I-和I3-的濃度基本不變
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com