
【題目】取氯化鈣和氯化鈉的混合物10g,加入40g水使其完全溶解,再加入50g碳酸鈉溶液恰好完全反應,過濾,得95g濾液(不考慮實驗過程中質量損失),計算:
(1)所加碳酸鈉溶液的溶質質量分數;
(2)反應后所得濾液中溶質的質量分數(計算結果精確到0.1%).
【答案】(1)10.6%;(2)10.8%
【解析】
根據質量守恒定律可知,過程中質量的減少是因為生成了碳酸鈣,所以可以求算碳酸鈣的質量,根據碳酸鈣和對應的化學方程式求算碳酸鈉和生成氯化鈉的質量,進而求算對應的質量分數.
(1)根據質量守恒定律可得,生成的碳酸鈣的質量為10g+40g+50g﹣95g=5g
設碳酸鈉的質量為x,樣品中氯化鈣的質量為y,生成的氯化鈉的質量為z.
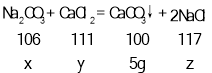
![]()
x=5.3g
y=5.55g
z=5.85g
碳酸鈉溶液中碳酸鈉的質量分數為![]() ×100%=10.6%
×100%=10.6%
(2)反應后所得溶液中氯化鈉的質量分數為![]() ×100%≈10.8%
×100%≈10.8%
答:(1)所加碳酸鈉溶液的溶質質量分數為10.6%;
(2)反應后所得濾液中溶質的質量分數約為10.8%.


 優等生題庫系列答案
優等生題庫系列答案科目:初中化學 來源: 題型:
【題目】如圖是初中化學常見物質的相互轉化關系示意圖.其中A是一種金屬氧化物.
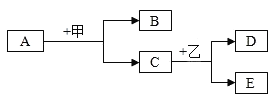
請回答下列問題:
(1)若甲是稀硫酸,D為藍色沉淀,則D為_____,A為_____.寫出A跟甲反應的化學方程式_____.
(2)若乙是稀硫酸,A為紅色固體,寫出C跟乙反應的化學方程式_____.若B能使澄清石灰水變渾濁,寫出B與石灰水反應的化學方程式_____.
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】有實驗室有一包白色粉末,可能含有![]() 和
和![]() 中的一種或幾種,為了確定其成分,某化學興趣小組進行了如下探究。
中的一種或幾種,為了確定其成分,某化學興趣小組進行了如下探究。
(查閱資料)![]() 固體不溶于水,也不溶于稀鹽酸。
固體不溶于水,也不溶于稀鹽酸。
(實驗探究)
(1)甲同學設計了如下的實驗方案。
實驗步驟 | 實驗現象 | 實驗結論 |
a取少量該粉末于試管中,加入足量水充分溶解 | 有白色沉淀 | 有原粉末中一定含有 |
b將步驟a試管中物質過濾,向濾液中滴加酚酞溶液 | 溶液變紅 | 原粉末一定含有_______ |
(2)乙同學認為甲同學步驟a的結論不一定正確,其理由是_______,他補充了如下實驗,取白色沉淀于試管中,加入足量稀鹽酸,觀察到有氣泡產生且_______,從而得出結論:步驟a中得到的白色沉淀全部是![]() ;
;
(3)丙同學取甲同學步驟b中已變紅的溶液,向其中逐滴滴入稀硫酸,發現有白色沉淀生成且溶液褪色.根據有白色沉淀生成的現象確定原粉末中一定有________,一定沒有________;溶液褪色的原因用化學方程式表示為_______。
(總結歸納)通過以上探究,原白色粉末中無法確定的成分是_______(填化學式)
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】現有稀鹽酸、稀硫酸、氫氧化鈉溶液、硫酸銅溶液和氯化鋇溶液五種溶液,為了鑒別和探究五種溶液,進行了下列相關實驗,請回答
(1)根據溶液顏色即可確定硫酸銅溶液.取少量四種無色溶液分別放入四支試管中,再分別滴加硫酸銅溶液,出現白色沉淀的是氯化鋇溶液;出現_____(填現象)的是_____(填溶液名稱).
(2)另取少量剩余的兩種溶液分別放入兩支試管中,再分別滴加氯化鋇溶液,其中一支試管內產生白色沉淀,該反應可用化學方程式表示為_____,至此,五瓶溶液已全部鑒別出來.
(3)氫氧化鈉溶液露置在空氣中易變質.下列是分析已變質氫氧化鈉溶液的相關實驗,其中合理的是_____(填字母).
A 證明變質:取樣,滴加足量稀鹽酸,觀察是否有氣泡產生
B 除去雜質:取樣,滴加氫氧化鈣溶液至恰好完全反應,過濾
C 確定成分:取樣,滴加足量氯化鋇溶液,過濾,向濾液中滴加酚酞溶液,觀察顏色變化(氯化鋇溶液呈中性)
(4)當部分變質的氫氧化鈉固體中,氫氧化鈉和碳酸鈉所含鈉元素的質量相同時,該固體中氫氧化鈉的質量分數為_____(計算結果精確到0.1%).
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】我區某校化學社團﹣﹣“拉瓦錫實驗室”的同學們在化學實驗室進行了一系列的實驗探究活動.
(1)甲組同學的實驗是除去粗鹽中難溶性雜質,實驗步驟主要有四步,如圖1.
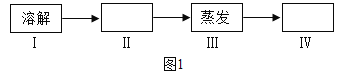
①步驟Ⅲ,給蒸發皿加熱時_____(填“需要”或“不需要”)墊石棉網,當出現_____時,停止加熱;
②步驟Ⅳ是_____.
(2)乙組同學進行的實驗是“從NaCl和Na2CO3的混合物中提純NaCl”.同學們經過討論認為利用兩物質化學性質的差異,可采用如下化學方法來提純.
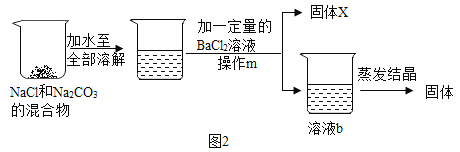
①如圖2中X的化學式為_____.由于BaCl2溶液的用量不易控制,會使溶液b的溶質有多種情況,導致蒸發后得到的固體可能不純.同學們對方案中溶液b的溶質成分進行了猜想.猜想一:NaCl、BaCl2 猜想二:NaCl 猜想三_____;
②經討論,大家認為只用一種試劑就能判斷出溶液b中溶質的成分,這種試劑是_____(寫名稱)
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】下列實驗操作,能達到實驗目的的是
選項 | 實驗目的 | 實驗操作 |
A | 驗證NaCl溶液中混有鹽酸 | 取少量溶液,滴加無色酚酞溶液 |
B | 除去NaOH中混有的碳酸鈉 | 滴加足量鹽酸、蒸發 |
C | 比較Zn、Cu、Ag的金屬活動性 | 將Zn和Ag分別放入CuSO4溶液中 |
D | 除去粗鹽中的難溶性雜質 | 將粗鹽研碎、溶解、蒸發 |
A.AB.BC.CD.D
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】有一種含CaCO3與CaO的混合物,測得其中鈣元素質量分數為50%.取該混合物16g,經高溫煅燒后,將剩余固體投入足量水中,固體全部溶解生成Ca(OH)2,則生成的Ca(OH)2質量為( )
A.3.7gB.7.4gC.14.8gD.22.2g
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】興趣小組對“一氧化碳還原氧化銅”的實驗進行拓展研究。
(查閱資料)
Ⅰ.制取 CO 的方法:加熱碳酸鎂和鋅粉的混合物,反應原理為:MgCO3+Zn==MgO+ZnO+CO↑Ⅱ.處理尾氣的方法:用氯化亞銅的氨水溶液吸收一氧化碳,溶液中會出現紅色固體。
(設計方案)根據上述資料設計如下實驗裝置(固定裝置略,裝置氣密性良好):
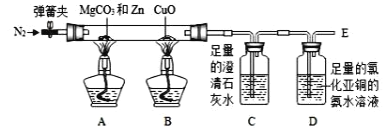
(實驗步驟)
第一步:打開彈簧夾,通入一會兒氮氣;
第二步:關閉彈簧夾,點燃兩個酒精燈;
第三步:一段時間后,熄滅兩個酒精燈;
第四步:……
(實驗分析)
(1)實驗過程中,觀察到 B 處的實驗現象是________;
(2)C 處發生反應的化學方程式是____________;
(3)D 處發生反應的化學方程式為:2CuCl+2CO+2X═Cu2Cl2(CO)2·2H2O↓,其中 X 的化學式為____________
(4)第四步操作是:打開彈簧夾,再通入氮氣至____________。
(5)若 A 處有 mg MgCO3 參加反應,實驗結束后 C 處生成 ng CaCO3,此時 D 裝置的溶液中有紅色固體析出,則 m 與 n 數量上的關系為____________。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com