
(6分)在高效復習課堂中,同學們利用“硫酸、硝酸鋇、氫氧化鈉、碳酸鉀” 四種物質的溶液對 “復分解反應發生的條件”進行再探究。
【知識回放】
 通過判斷上述四種溶液兩兩之間能否發生反應,我能寫出其中符合下列條件的兩個化學方程式:
通過判斷上述四種溶液兩兩之間能否發生反應,我能寫出其中符合下列條件的兩個化學方程式:
⑴一個中和反應 ;
⑵一個有沉淀生成的反應 。
【挖掘實質】
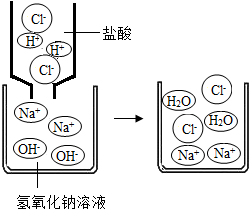
⑴圖38-1是HCl和NaOH在水中解離出離子的示意圖,小麗發現HCl在水中會解離出H+和Cl-,NaOH在水中會解離出Na+和OH-,以此類推硝酸鋇在水中會解離出的離子是 (填離子符號)。
⑵圖38-2是稀鹽酸和氫氧化鈉溶液發生化學反應的微觀過程示意圖,該化學反應的實質可以表示為
H+ + OH- = H2O
我也能用同樣的方式表示上述四種溶液兩兩之間發生反應時有氣體生成的反應的實質 。
【實踐運用】
⑴通過上述探究發現,在溶液中H+和OH-不能大量共存,我還發現在溶液中
(填離子符號,下同)也不能大量共存。
⑵利用上述四種物質的溶液完成實驗后,將所得物質混合并過濾,得到一種無色溶液。經測定,該溶液顯酸性。則在該溶液中一定含有的離子是 。
39. 【題文】(4分)家庭食用面堿(主要成分為Na2CO3)中往往混有少量NaCl。李童同學為測定食用面堿中碳酸鈉的含量,設計并進行了以下實驗:
①稱取面堿樣品3.4g于燒杯中,加入20mL水,攪拌至樣品全部溶解;
②向其中加入足量的CaCl2溶液,至不再生成沉淀為止;
③過濾并將所得沉淀干燥后,稱得質量為3.0g(不考慮操作中的質量損失)。
請計算:食用面堿中Na2CO3的質量分數是 (精確到0.1%)
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小學生10分鐘應用題系列答案
小學生10分鐘應用題系列答案科目:初中化學 來源: 題型:閱讀理解

| 溶液中可能含有的離子 | 設計實驗驗證(實驗步驟、現象及對應的結論) |
可能性一:Ba2+ 可能性二:SO42- 可能性三:Ba2+或SO42- 可能性一:Ba2+ 可能性二:SO42- 可能性三:Ba2+或SO42- | ①取上述溶液少量于試管中,加入少量硫酸鈉溶液.若出現白色沉淀,則說明上述溶液中含有Ba2+;若沒有出現白色沉淀,則說明上述溶液中不含有Ba2+., ②取上述溶液少量于試管中,加入少量硝酸鋇溶液.若出現白色沉淀,則說明上述溶液中含有SO42-;若沒有出現白色沉淀,則說明上述溶液中不含有SO42-. ③取上述溶液少量于試管中,加入少量硫酸鈉溶液.若出現白色沉淀,則說明上述溶液中含有Ba2+,不含有SO42-. ①取上述溶液少量于試管中,加入少量硫酸鈉溶液.若出現白色沉淀,則說明上述溶液中含有Ba2+;若沒有出現白色沉淀,則說明上述溶液中不含有Ba2+., ②取上述溶液少量于試管中,加入少量硝酸鋇溶液.若出現白色沉淀,則說明上述溶液中含有SO42-;若沒有出現白色沉淀,則說明上述溶液中不含有SO42-. ③取上述溶液少量于試管中,加入少量硫酸鈉溶液.若出現白色沉淀,則說明上述溶液中含有Ba2+,不含有SO42-. |
查看答案和解析>>
科目:初中化學 來源: 題型:閱讀理解
 36、在高效復習課堂中,同學們利用“硫酸、硝酸鋇、氫氧化鈉、碳酸鉀”四種物質的溶液對“復分解反應發生的條件”進行再探究.
36、在高效復習課堂中,同學們利用“硫酸、硝酸鋇、氫氧化鈉、碳酸鉀”四種物質的溶液對“復分解反應發生的條件”進行再探究.| 溶液中可能含有的離子 | 設計實驗驗證 | ||
| 實驗步驟 | 現象 | 結論 | |
查看答案和解析>>
科目:初中化學 來源: 題型:閱讀理解

| 溶液中可能含有的離子 | 設計實驗驗證(實驗步驟、現象及對應的結論) |
可能含SO42- 可能含SO42- |
取上述溶液少量于試管中,加入少量硝酸鋇溶液.若出現白色沉淀,則說明含有SO42-;若沒有出現白色沉淀,則說明上述溶液中不含有SO42-. 取上述溶液少量于試管中,加入少量硝酸鋇溶液.若出現白色沉淀,則說明含有SO42-;若沒有出現白色沉淀,則說明上述溶液中不含有SO42-. |
查看答案和解析>>
科目:初中化學 來源: 題型:閱讀理解
| 時間/h | 1 | 1.5 | 4 | 8 | 12 | 24 | 48 | 60 | |
| 吸水質量/g | 硫酸甲 | 1.6 | 2.2 | 5.2 | 10.3 | 14.0 | 20.9 | 29.2 | 32.1 |
| 硫酸乙 | 1.2 | 1.5 | 3.5 | 5.9 | 8.1 | 12.9 | 19.5 | 21.0 | |
| 溶液中可能含有的離子 | 設計實驗驗證(實驗步驟、現象及對應的結論) |
SO42- SO42- |
取少量濾液,加入硝酸鋇溶液,若有白色沉淀產生,說明溶液中含有SO42-;若無白色沉淀產生,說明溶液中不含有SO42-. 取少量濾液,加入硝酸鋇溶液,若有白色沉淀產生,說明溶液中含有SO42-;若無白色沉淀產生,說明溶液中不含有SO42-. |
查看答案和解析>>
科目:初中化學 來源: 題型:
 在高效復習課堂中,同學們利用“硝酸、氯化鋇、氫氧化鉀、硫酸鎂”四種物質的溶液對“復分解反應發生的條件”進行再探究.
在高效復習課堂中,同學們利用“硝酸、氯化鋇、氫氧化鉀、硫酸鎂”四種物質的溶液對“復分解反應發生的條件”進行再探究.查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com