
題目列表(包括答案和解析)
某同學為了測定Cu-Zn合金中銅的質量分數,該同學取合金粉末20.0g,向其中逐滴加入稀硫酸,當加入187.4g稀硫酸時恰好完全反應,不再產生氣泡,經測定反應后溶液的質量為200.0g。求
(1)該合金中銅的質量分數。 (2)反應后溶液中溶質的質量分數。
某課外活動小組為了測定銅鐵合金中鐵的質量分數,現取銅鐵合金樣品20.0g,將80.0g稀硫酸平均分成4份,分4次逐漸加入到樣品中,每次充分反應后測得剩余固體質量見下表
| 次數 | 1 | 2 | 3 | 4 |
| 加入稀硫酸的質量/g | 20.0 | 20.0 | 20.0 | 20.0 |
| 剩余固體質量/g | 17.2 | 14.4 | 13.0 | 13.0 |
試求:
①20.0g銅鐵合金中,銅的質量為 g。
②銅鐵合金中,鐵元素的質量分數為 。
③20g稀硫酸溶液中溶質質量。
(12分)鐵及其化合物在生活生產中有重要的應用。請回答下列問題:
(1)鐵制品在空氣中易銹蝕,其實質是鐵與空氣中的氧氣、 等接觸后發生化學反應的過程。
(2)在盛有氧氣的集氣瓶中點燃細鐵絲發生劇烈燃燒的化學方程式是 。為防止集氣瓶破裂,常采取的措施是 。
(3)把鐵粉和銅粉的混合物放入硝酸銀溶液中,充分反應后,過濾,為確定濾渣和濾液的成分,甲同學向濾渣中滴加稀鹽酸,無氣泡產生; 乙同學向濾液中滴加稀鹽酸,產生白色沉淀。根據兩同學實驗的現象,分析下列結論不正確的是 (填寫字母序號)。
A.濾渣中只含銀 B.濾渣中一定含有銀,可能含有銅
C.濾液中一定有Ag+ 、Fe2+ 和Cu2+ D.濾液中只含Ag+ 和Fe2+,不含Cu2+
【探究】廢舊金屬的回收利用。
廢鐵屑的主要成份是鐵,同時還有少量鐵銹(Fe2O3),生產動物飼料添加劑硫酸亞鐵的工藝之一如下圖所示:
(4)在反應器中發生反應的化學方程式有:
Fe + H2SO4 =FeSO4 +H2↑、 、 Fe2(SO4)3 + Fe = 3FeSO4。
(5)濾液M中肯定含有的溶質的化學式是 ;
(6)在化學反應中,凡是有元素化合價變化的反應屬于氧化還原反應。下列反應類型肯定屬于氧化還原反應的是 (填字母編號);
A.化合反應 B.置換反應 C.分解反應 D.復分解反應
(7)取表面含有氧化鎂的鎂條(無其它雜質)2.5g,加入到足量的20.0g的稀硫酸中,充分反應后,所得溶液的質量為22.3g。求:該鎂條中單質鎂的質量分數。
金屬材料在生產、生活中有著廣泛的應用。
 ⑴下列生活用品,主要利用金屬具有良好導熱性的是:___ ____。
⑴下列生活用品,主要利用金屬具有良好導熱性的是:___ ____。
A.鑄鐵炊具 B.金屬細絲 C.銅制電纜 D.鐵錘
⑵工業生產中,切割鐵板時用硫酸銅溶液在鐵板上畫線可留下紅色的印跡。有關反應的化學方程式為____ _ _。
⑶若要比較鐵、錳、銅的金屬活動性強弱,可選擇的藥品除了鐵、銅單質外,還需要 。
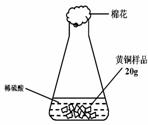
⑷研究性學習小組為了測定黃銅(銅、鋅合金)的組成,用電子天平分別稱得錐形瓶與棉花的質量為44.1g,稱取黃銅
樣品20.0g。在錐形瓶中加入該樣品和足量稀硫酸后瓶口塞上棉花,如圖1所示。將電子天平稱量的數據繪成圖2。
請認真分析數據,回答下列問題:
(Ⅰ)四個同學從多角度處理數據,下列數據處理的圖像中正確的是 。
(Ⅱ)試計算:
①樣品中銅的質量分數;②恰好反應時所得溶液中溶質的質量分數。


湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com