
題目列表(包括答案和解析)
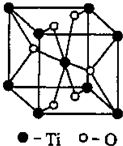
(12分) (物質(zhì)結(jié)構(gòu)與性質(zhì))新型節(jié)能材料高溫超導(dǎo)體的最先突破是在1987年從新的釔鋇銅氧材料的研究開始的。在制備釔鋇銅氧高溫超導(dǎo)體的同時,偶然得到了副產(chǎn)品——紫色的硅酸銅鋇。湊巧的是,后者正是發(fā)現(xiàn)于中漢代器物上的被稱為“漢紫”的顏料,還發(fā)現(xiàn)于秦俑彩繪。 釔鋇銅氧的晶胞結(jié)構(gòu)如圖。研究發(fā)現(xiàn),此高溫超導(dǎo)體中的銅元素有兩種價態(tài),+2價和+3價。
釔鋇銅氧的晶胞結(jié)構(gòu)如圖。研究發(fā)現(xiàn),此高溫超導(dǎo)體中的銅元素有兩種價態(tài),+2價和+3價。
(1)給出銅在周期表中的位置(周期和族)
(2)寫出基態(tài)Cu原子的核外電子排布:
(3)根據(jù)圖示晶胞結(jié)構(gòu),推算晶體中Y,Cu,Ba和O原子個數(shù)比,確定其化學(xué)式為:
(4)①某+1價銅的配離子為[Cu(CN)4]3-,與其配體互為等電子體的一種微粒是
(寫化學(xué)式)。
②許多+1價銅的化合物的溶液能吸收CO和烯烴(如C2H4、CH3-CH=CH2……),CH3-CH=CH2分子中C原子的雜化方式是 、 。
(5)在硫酸銅溶液中逐滴加入氨水至過量,觀察到先出現(xiàn)藍(lán)色沉淀,最終沉淀溶解得到深藍(lán)色的溶液。寫出藍(lán)色沉淀溶解的離子方程式 。
 [化學(xué)-物質(zhì)結(jié)構(gòu)與性質(zhì)]
[化學(xué)-物質(zhì)結(jié)構(gòu)與性質(zhì)] 鍵和1個大
鍵和1個大 鍵,C2H2是非極性分子
鍵,C2H2是非極性分子 

(1)陰影部分元素N在元素周期表中的位置為第________周期第________族。根據(jù)元素周期律,請你預(yù)測,H3AsO4、H3PO4的酸性強弱:H3AsO4________H3PO4(填“>”、“<”或“=”)。
(2)根據(jù)NaH的存在,有人提議可把氫元素放在第ⅦA族,那么根據(jù)其最高正價與最低負(fù)價的絕對值相等,又可把氫元素放在周期表中的第________族。
(3)元素甲是第三周期金屬元素中原子半徑最小的元素,該元素的離子與過量氨水反應(yīng)的離子方程式為:____________________________。
(4)周期表中有10多種人體所需的微量元素,其中有一種被譽為“生命元素”的主族元素R,對延長人類壽命起著重要作用.已知R元素的原子有4個電子層,其最高價氧化物的分子式為RO3,則R元素的名稱為________。
A.硫 B.砷 C.硒 D.硅
(5)羰基硫(COS)分子結(jié)構(gòu)與二氧化碳分子結(jié)構(gòu)相似,所有原子的最外層都滿足8電子結(jié)構(gòu),用電子式表示羰基硫分子的形成過程:_______________________________________。
| |||||||||||||||||||||||||||||||||
(一)選擇題
1.C2.C3.A4.B5.C6.B7.D8.A、B9.D10.AB11.B、C12.C13.D14.C15.C16.C17.D18.B19.A、D20.A21.B22.D23.B24.C25.D26.C27.B28.D29.A、D30.B
(二)非選擇題
1.有關(guān)反應(yīng)為
Fe+4HNO3Fe(NO3)3+NO+2H2O……(1)
Fe(NO3)3Fe2O3+3NO2+O2……(2)
3NO2+O2+H2O3HNO3……(3)
NO+O2+H2OHNO3……(4)
由逆向推,反應(yīng)(4)中n(NO)=這正好是反應(yīng)(1)中消耗的n(Fe)。故耗鐵的質(zhì)量m(Fe)=0.04mol×56g/mol=2.24gA中溶質(zhì)為(3)、(4)反應(yīng)中生成的HNO3,根據(jù)氮原子守恒規(guī)則,正好是反應(yīng)(1)中消耗的HNO3,所以A中HNO3質(zhì)量:m(HNO3)=0.04mol×4×63g/mol=8.82g答(略)
2.NH3?H2O+SO2=NH4++HSO3―或2NH3?H2O+SO2=2HN4++SO+H2O
2NO2+2OH―=NO3―+NO2―+H2O
CaCO3+2H+=Ca2++H2O+CO2?
3.解析題目給予的條件較多,海水中有D物質(zhì)存在,且A、B元素均為常見的元素,可推知D可能為MgCl2。并由此推出A單質(zhì)是Ba,B單質(zhì)是Mg,X為Cl2或HCl,E為BaCl2。
答案:(1)Cl2或HCl
(2)MgCl2+Ba(OH2)BaCl2+Mg(OH)↓(3)Ba2++SOBaSO4↓
4.P4、X:P2O5Y:HPOZ:H3PO4
5.(1)S~CaSO4?2H2O
1mol172g
x
x=76780g=76.78kg
(2)若溶液中溶質(zhì)全為Na2SO3,則Na+=2mol?L-1×0.2L=0.4mol,Na2SO3質(zhì)量為0.2mol×126g/mol=25.2g<33.4g;
若溶質(zhì)是NaHSO3,則質(zhì)量是:
0.4mol×104g/mol=41.6g>33.4g
所以,33.4g溶質(zhì)是Na2SO3和NaHSO3的混合物。
設(shè)Na2SO3的物質(zhì)的量為x,NaHSO3為y
解得:x=0.1mol,y=0.2mol
6.(1)6HCl+KClO3KCl+3Cl2+3H2O(2)0.5mol電子(3)73.3
7.①以防止試管C內(nèi)Na2O2和外界相通時發(fā)生吸潮現(xiàn)象②濃H2SO4Na2O2與干燥的CO2不反應(yīng)③帶火星的小木條在試管B的液面上劇烈燃燒,同時黃色粉末變成白色粉末④2Na2O2+2C18O2+2H=2Na2C18O3+2H2O+O2?
8.(1)從周期表位置上下關(guān)系看,金屬性Mg>Li,從周期表位置左右關(guān)系看,金屬性Li>Mg,所以處在以上圖對角關(guān)系的兩個元素,化學(xué)性質(zhì)往往相似。
(2)兩性H2BeO2+2OH―BeO+2H2O,Be(OH)2+2H+Be2++2H2O(3)原子
9.(1)球碳分子C60?(2)星際中存在的應(yīng)是球碳分子C60,火山口發(fā)現(xiàn)的應(yīng)是金剛石。
10.(1)含Ba2+、Ca2+離子中的一種或兩種,因BaSO4難溶,CaSO4微溶。(2)Fe(OH)3(3)2AlO―2+CO2+3H2O2Al(OH)3↓+CO或AlO―2+CO2+2H2OAl(OH)3↓+HCO―3
11.(1)D,3H2O2+Cr2(SO4)3+10KOH2K2CrO4+3K2SO4+8H2O(2)C(3)A
12.(1)Cu+H2SO4(濃)CuSO4+SO2↑+H2O
(2)4FeS2+11O22Fe2O3+8SO2
(3)H2S+H2SO4(濃)S↓+SO2↑+H2O
(4)Na2SO3+H2SO4Na2SO4+SO2↑+H2O
13.“不另加固體或液體物質(zhì)”說明可以通入氣體試劑。依題意通NH3可使溶液中的Al3+沉淀;通CO2氣可使溶液中的AlO―2沉淀;也可用Al3+和AlO―2在溶液中相混合產(chǎn)生沉淀的方法。
(1)設(shè)往A溶液中至少通入xmolNH3,則
Al3++3NH3+3H2OAl(OH)3?+3NH+4
11
axx=3amol
(2)設(shè)往B溶液中至少通入ymolCO2,則
2AlO―2+CO2+3H2O2Al(OH)3+CO
21
byy=0.5bmol
(3)將A溶液與B溶液混合,則
Al3++3AlO―2+6H2O4Al(OH)3?
13
ab
討論:①若b=3a,則混合后兩溶液中的Al元素正好全部轉(zhuǎn)化為沉淀;
②若b<3a,則只有AlO―2完全轉(zhuǎn)化。
Al3++3AlO―2+6H2O4Al(OH)2?
13
b
則剩余Al3+(a-)mol,還需要通入NH3為3(a-)=(3a-b)mol。
③若b>3a,則只有Al3+完全轉(zhuǎn)化。
Al3++3AO―2+6H2O4Al(OH)3
13
a3a
則剩余AlO―2(b-3a)mol,還需通入CO2氣體為mol。
14.(1)A、C、D(2)Cu++NO―2+2H+Cu2++NO↑+H2O
(3)3NONO2+N2O
(4)生成的NO2又發(fā)生如下反應(yīng):2NO2N2O4,而使壓力略小于原壓力的
15.(1)稀,a、c(2)a、c(3)b,Fe(OH)3,Cu(OH)2
16.解析(1)從圖中可以看出,在由硅氧四面體形成的環(huán)上,每個硅原子保留了兩個沒有被共用的氧原子,另外還有兩個氧原子分別在相鄰的左右兩個硅氧四面體共用,因此在每個硅氧四面體內(nèi)占有的氧原子數(shù)為:
即,如果硅原子的數(shù)目為n,則氧原子的數(shù)目為3n.構(gòu)成硅氧四面體內(nèi)的硅原子呈+4價,氧原子呈-2價,據(jù)此可計算出酸根的化合價,從而寫出通式(2)將n=6代入通式,可知綠柱石的酸根為(Si6O18)12-,因此兩種金屬的化合價之和應(yīng)為+12。設(shè)綠柱石化學(xué)式為BexAlySi6O18,元素Be為+2價,元素Al為+3價,由此可得2x+3y=12,經(jīng)討論解得x=3,y=2是合理答案,這樣可確定綠柱石的化學(xué)式為Be3Al2Si6O18,最后可寫出氧化物形式:3BeO?Al2O3?6SiO2.
17.(1)孔雀石CuCO3?Cu(OH)2石青2CuCO3?Cu(OH)2
(2)化學(xué)組成:CuCO3?Cu(OH)2與2CuCO3?Cu(OH)2混合物
(3)36g
(4)A=124
18.(1)(略)(2)先通NH3,因其溶解度遠(yuǎn)大于CO2.在通CO2時發(fā)生NH3+CO2+H2O=NH4HCO3,使[HCO―3]大增,而NaHCO3溶解度不是很大,故析出。若反之由于CO2溶解度小,再通NH3時,不能使[HCO―3]大增,故不析出。若同時通氣則會浪費CO2.
19.解析Fe3+對Zn、Fe、Cu均顯氧化性,故有Fe3+就無金屬殘留,溶液中離子為Zn2+、Fe2+、Cu2+、Fe3+。溶液顯藍(lán)色,有Cu2+,則Fe、Zn不能存在,故②中Cu可能剩余,溶液中離子為Cu2+、Fe2+、Zn2+。③有Fe則無Cu2+、Fe3+,F(xiàn)e質(zhì)量不變說明Fe3+恰好和Zn反應(yīng)掉(Fe3+先與還原能力強的Zn反應(yīng)),否則存在如有Zn存在則Zn+Fe2+Fe,會使Fe質(zhì)量增加,所以固體是Cu、Fe混合物。因Zn+2Fe3+Zn2++2Fe2+,故反應(yīng)后Cu∶Fe∶Fe2+∶Zn2+∶Cl―=1∶1∶2∶1∶6。④還有Zn剩余,則溶液里無Fe3+、Fe2+、Cu2+只有Zn2+。Cu、Fe均未消耗,相反Fe質(zhì)量還要增加。
20.(1)FeS、FeS2(2)(3)略
21.E:C;G:O;D:Fe;A:Kx=3;y=1;z=3K3Fe(C2O4)3
22.①②④③⑥(2)K2CO3溶液(3)不能,KOH溶液,AgNO3溶液,小于
23.C2Cl?5F,C2H2F4
24.(1)1,0<x<w(2)2,x≥w(3)
25.(1)甲:x表示Cl2的物質(zhì)的量
乙:x表示原有Cl2的體積
丙:x表示被氧化的NH3的物質(zhì)的量
丁:x表示原混合氣中的Cl2的體積分?jǐn)?shù)
(2)0.34g
26.(1)a=,b==1.306
(2)m1(H2O)=20g?mol-1?n1(SO3)
m2(H2O)=13.8g?mol-1?n2(SO3)
(3)
(4)m總(H2O)=
27.(SinO3n+1)(2n+2)-
28.(1)BH―4+2H2O=BO―2+4H2↑(2)3BH―4+8Au3++24OH―=3BO―2+8Au+18H2O
29.(1)C+CO22CO(2)FeO和Fe,CO2(3)C和Fe,CO(4)1/2<n<1(5)n=2/3
30.(1)B+3HNO3H3BO3+3NO2
(2)
(3)B2H6
31.(1)Cu2O+Fe2(SO4)3+H2SO42CuSO4+2FeSO4+H2O
(2)10FeSO4+2KMnO4+8H2SO45Fe2(SO4)3+2MnSO4+K2SO4+8H2O
(3)Cu2O~Fe2(SO4)3~2FeSO4~KMnO4
mCu2o=
Cu2O%=×100%=72%
32.(1)①4Al+3O22Al2O3+Q
②2NH4ClO42O2↑+N2↑+Cl2↑+4H2O↑
(2)1mol高氯酸銨分解所產(chǎn)生的氣體有4mol.
33.加液氨后HClO與NH3反應(yīng)轉(zhuǎn)化為較穩(wěn)定的NH2Cl,可在水中存在較長時間,而且隨著HClO的開始消耗,上述平衡向左移動,產(chǎn)生HClO,又起殺菌作用。
34.(1)3Br2+6OH―BrO―3+5Br―+3H2O
(2)BrO―3+5Br―+6H+3Br2+3H2O
35.(1)Be+2OH―BeO+H2↑
(2)NaOH溶液,Be(OH)2+2OH―+2H2O
(3)共價化合物,∶Cl∶Be∶∶,Be2++2H2OBe(OH)2+2H+
國際學(xué)校優(yōu)選 - 練習(xí)冊列表 - 試題列表
湖北省互聯(lián)網(wǎng)違法和不良信息舉報平臺 | 網(wǎng)上有害信息舉報專區(qū) | 電信詐騙舉報專區(qū) | 涉歷史虛無主義有害信息舉報專區(qū) | 涉企侵權(quán)舉報專區(qū)
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com