
題目列表(包括答案和解析)
| A、科舉用氟能預防齲齒 | B、青少年經常用牙簽剔牙有損牙齒健康 | C、乳牙能被恒牙替換,所以保護牙齒應從換牙時開始 | D、飲食多樣化有利于牙齒健康 |
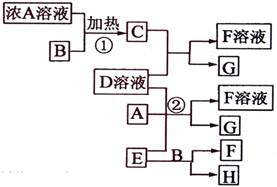
(9分)有關物質存在如圖所示的轉化關系(部分產物已省略)。通常C為氣體單質,G為紫黑色固體單質。實驗室中,常用固體E在B的催化下加熱制取氣體單質H。
![]()
![]()
![]()
請回答下列問題
(1)反應①的化學方程式為
(2)反應②的離子方程式為
(3)寫出另外一種實驗室制取H的化學方程式
(4)D溶液與Pb(NO3)2溶液混合可形成沉淀,此沉淀的Ksp=7.0×10―9。將等體積的D溶液與Pb(NO3)2溶液混合,若D的濃度為1×10―2mo1/L ,則生成沉淀所需Pb(NO3)2溶液的最小濃度為 。
(9分) Li-SOCl2電池可用于心臟起搏器。該電池的電極材料分別為鋰和碳,電解液是LiAlCl4―SOCl2。電池的總反應可表示為:4Li+2SOCl2 = 4LiCl +S +SO2。
![]() 請回答下列問題:
請回答下列問題:
![]() (1)電池的負極材料為 ,發生的電極反應為 ;
(1)電池的負極材料為 ,發生的電極反應為 ;
![]() (2)電池正極發生的電極反應為 ;
(2)電池正極發生的電極反應為 ;
(3)SOCl2易揮發,實驗室中常用NaOH溶液吸收SOCl2,有Na2SO3和NaCl生成。 如果把少量水滴到SOCl2中,實驗現象是 ,反應的化學方程式為 ;
![]() (4)組裝該電池必須在無水、無氧的條件下進行,原因是 。
(4)組裝該電池必須在無水、無氧的條件下進行,原因是 。
(9分)下圖表示從固體混合物中分離X的2種方案,請回答有關問題。
![]()


(1)選用方案I時,X應該具有的性質是 ,殘留物應該具有的性質是 ;
(2)選用方案Ⅱ從某金屬粉末(含有Au、Ag和Cu)中分離Au,加入的試劑是 ,有關反應的化學方程式為 ;(3)為提純某Fe2O3樣品(主要雜質有SiO2、A12O3),參照方案I和Ⅱ,請設計一種以框圖形式表示的實驗方案(注明物質和操作) 。
1.D 2.B 3.B 4.D 5.A 6.AD 7.D 8.AD 9.A 10.AC 11.AC
12.D 13.BC 14.D 15.C 16.D 17.A 18.B 19.A 20.A 21.C 22.D
23.(1)CuS、S (2)6∶1∶4
(3)

24.(1)D (2)> (3)B
25.解析:(1)
(2)因 中的
中的 ,
, 中的
中的 ,故依電子得失守恒有(x+1)×25.00×0.1000=5×30.00×0.0500,解之,x+2,即
,故依電子得失守恒有(x+1)×25.00×0.1000=5×30.00×0.0500,解之,x+2,即 被氧化成+2價氮的氧化物NO.又因V×C×2=30.00×0.0500×5,故
被氧化成+2價氮的氧化物NO.又因V×C×2=30.00×0.0500×5,故 .依題意知,
.依題意知,


 .所以
.所以 與
與 反應的方程式為
反應的方程式為

 w.w.w.k.s.5.u.c.o.m
w.w.w.k.s.5.u.c.o.m
26.解析:這是一道天平平衡問題的計算.兩個燒杯的質量相等.兩個燒杯里鹽酸溶液的質量相等.因此論證天平兩個燒杯內反應體系質量改變量相等是解決本題的關鍵.由題意可知:
 溶液增重
溶液增重
100 56
a
 溶液增重
溶液增重
84 40
x 40x/84
當0.3 mol HCl與 恰好完全反應時,消耗
恰好完全反應時,消耗 的質量為:
的質量為: 時;0.3 mol HCl與
時;0.3 mol HCl與 恰好完全反應,消耗
恰好完全反應,消耗 的質量為:0.3×84=
的質量為:0.3×84=
(1)a≤ 、
、 均過量,天平保持平衡的條件是:
均過量,天平保持平衡的條件是:
 x=
x=
(2)a> 不足,且對于
不足,且對于 恰好完全反應時,加入
恰好完全反應時,加入 的燒杯內反應體系的增重量為a-0.15×44,而加入
的燒杯內反應體系的增重量為a-0.15×44,而加入 的燒杯內反應體系的增重量為0.3×40.則天平保持平衡的條件是:
的燒杯內反應體系的增重量為0.3×40.則天平保持平衡的條件是:
a-0.15×44=0.3×40 a=18.6
因此,18.6≥a>15時,天平保持平衡的條件是:
 x=2,
x=2,
(3)當a>18.6時,天平保持平衡的條件是:a-0.15×44=x-0.3×44
x=a+6.6
因為燒杯中無固體剩余,說明a≤15. 、
、 的摩爾質量相當,當等質量的
的摩爾質量相當,當等質量的 、
、 與酸完全反應時,生成
與酸完全反應時,生成 質量相等.所以天平保持平衡時:x=a≤15
質量相等.所以天平保持平衡時:x=a≤15
27.解析:題中涉及化學反應如下: w.w.w.k.s.5.u.c.o.m
w.w.w.k.s.5.u.c.o.m
 ①
①
 ②
②
 ③
③
(1)當剩余固體為 ,排出氣體為
,排出氣體為 、
、 時,因為沒有NaOH生成,水未與
時,因為沒有NaOH生成,水未與 反應.將方程式①×2+②得:
反應.將方程式①×2+②得:

由方程式可知: .
.
(2)當剩余固體為 、NaOH,排出氣體為
、NaOH,排出氣體為 、
、 時,由于有NaOH生成,所以有水與
時,由于有NaOH生成,所以有水與 反應.假設反應后無
反應.假設反應后無 生成,將方程式①×2+②+③得:
生成,將方程式①×2+②+③得:

由方程式可知此時 .因為有水生成,所以
.因為有水生成,所以
(3)當 時,由2討論可知:剩余固體為
時,由2討論可知:剩余固體為 、NaOH、
、NaOH、 ;排出氣體為
;排出氣體為 .
.
(4)當排出的 和
和 為等物質的量時,依方程式討論有:
為等物質的量時,依方程式討論有:

2b b b

b b 
設反應的 的物質的量為x
的物質的量為x

x x 
依題意有:

所以,反應中消耗 的物質的量為:
的物質的量為: ,用去
,用去 的物質的量為:
的物質的量為:
 w.w.w.k.s.5.u.c.o.m
w.w.w.k.s.5.u.c.o.m
所以,
28.(1)0~50℃時, 不發生分解,固體物質質量不變
不發生分解,固體物質質量不變
(2)50℃~ 分解的結果,結晶水全部失去
分解的結果,結晶水全部失去

179 143

(3)100℃~ 穩定且不發生分解,故固體質量不變
穩定且不發生分解,故固體質量不變
(4)214℃~ 發生了分解
發生了分解

143 55+16x
0.80 0.40
x≈1 y=1.5,
故反應方程式為
(5)280℃~ 反應生成高價態氧化物
反應生成高價態氧化物
 方程式為
方程式為

29.解:假設反應后的混合物標況下仍為氣體且體積為 ,由
,由 ,得
,得
 ,可見反應前后物質的量不變,設烷烴為
,可見反應前后物質的量不變,設烷烴為 ,體積為x,則CO為
,體積為x,則CO為
由 體積減少
體積減少

 體積增加
體積增加
 nL (n+1)L
nL (n+1)L 
x

據題意得: nx=
nx=
討論:(1)n=l時,x=
(2)n=2時,
(3)n=3時,
(4)n=4時,
(5)n≥5時,常溫下烷烴不是氣態,所以,烷烴可能是 占50%或是:
占50%或是: 占33.3%或:
占33.3%或: 占25%
占25% w.w.w.k.s.5.u.c.o.m
w.w.w.k.s.5.u.c.o.m
30.(1)

2 mol 2 mol 2 mol 2 mol
溶液中剩余的水的質量為:
析出小蘇打的質量為:
(2) 和
和
當降溫至 的質量為:
的質量為:

析出 的質量為:
的質量為:
 共析出晶體的質量為:
共析出晶體的質量為: www.ks5u.com
www.ks5u.com
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com