
題目列表(包括答案和解析)
 2NH3,在一定條件下已達到平衡狀態(tài).
2NH3,在一定條件下已達到平衡狀態(tài). 2NH3(g)△H=-92.4KJ/mol
2NH3(g)△H=-92.4KJ/mol 2NH3(g)△H=-92.4KJ/mol
2NH3(g)△H=-92.4KJ/mol| 2-a |
| 2 |
| 2-a |
| 2 |
| 6-3a |
| 2 |
| 6-3a |
| 2 |
| A | B | C | D | E | |
| n(CO2) | 3 | l | 0 | 1 | l |
| n(H2) | 2 | l | 0 | 1 | 2 |
| n(CO) | 1 | 2 | 3 | 0.5 | 3 |
| n(H2O) | 5 | 2 | 3 | 2 | l |
| T/°C | T1 | 300 | T2 |
| K | 1.00×107 | 2.45×105 | 1.88×103 |
| 1 |
| 2 |
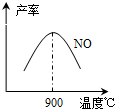 (3)NH3和O2在鉑系催化劑作用下從145℃就開始反應:4NH3(g)+5O2(g)?4NO(g)+6H2O(g)△H=-905kJ?mol-1,不同溫度下NO產(chǎn)率如右圖所示.溫度高于900℃時,NO產(chǎn)率下降的原因
(3)NH3和O2在鉑系催化劑作用下從145℃就開始反應:4NH3(g)+5O2(g)?4NO(g)+6H2O(g)△H=-905kJ?mol-1,不同溫度下NO產(chǎn)率如右圖所示.溫度高于900℃時,NO產(chǎn)率下降的原因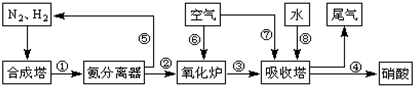
| T/℃ | T1 | 300 | T2 |
| K | 1.00×107 | 2.45×105 | 1.88×103 |
| n(NO) |
| n(CO) |
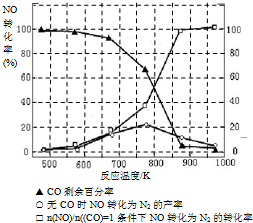
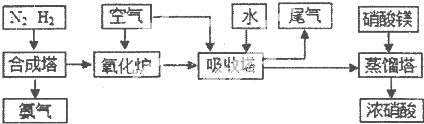
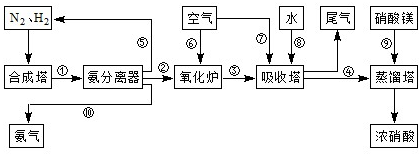
(16分)工業(yè)合成氨與制備硝酸一般可連續(xù)生產(chǎn),流程如下:
(1)工業(yè)生產(chǎn)時,制取氫氣的一個反應為:CO+H2O(g)CO2+H2。t℃時,往1L密閉容器中充入0.2molCO和0.3mol水蒸氣。反應建立平衡后,體系中c(H2)=0.12mol·L-1。該溫度下此反應的平衡常數(shù)K=_____(填計算結(jié)果)。
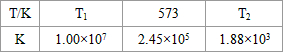
(2)合成塔中發(fā)生反應N2(g)+3H2(g)2NH3(g) △H<0。下表為不同溫度下該反應的平衡常數(shù)。由此可推知,表中T1____300℃(填“>”、“<”或“=”)。
| T/℃ | T1 | 300 | T2 |
| K | 1.00×107 | 2.45×105 | 1.88×103 |
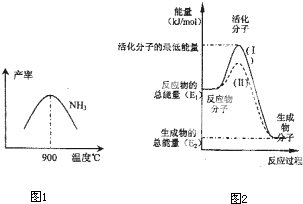
(3)N2和H2在鐵作催化劑作用下從145℃就開始反應,不同溫度下NH3產(chǎn)率如圖所示。溫度高于900℃時,NH3產(chǎn)率下降的原因 。
(4)在上述流程圖中,氧化爐中發(fā)生反應的化學方程式為
__________ _。
(5)硝酸廠的尾氣直接排放將污染空氣。目前科學家探索利用燃料氣體中的甲烷等將氮的氧化物還原為氮氣和水,反應機理為:
CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(g) △H= -574kJ·mol-1
CH4(g)+4NO(g)=2N2(g)+CO2(g)+2H2O(g) △H= -1160kJ·mol-1
則甲烷直接將NO2還原為N2的熱化學方程式為:________________________ 。
(6)氨氣在純氧中燃燒,生成一種單質(zhì)和水,試寫出該反應的化學方程式____________________,科學家利用此原理,設計成氨氣-氧氣燃料電池,則通入氨氣的電極是__________(填“正極”或“負極”);堿性條件下,該電極發(fā)生反應的電極反應式為_______________________。
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
17
18
D
D
A
B
D
D
C
D
B
B
B
C
C
A
C
C
B
A
19.(8分)( 1 ) B D ( 2 分)
(2)一定有 NO3-、Al3+、SO42-(2分); 一定無 Fe3+、Ba2+、HCO3-(2分)
(3) Al3+ + 3 NH3?H2O = Al(OH)3↓+3NH4+ (2分)
 20.(10分)(一)(1)2NH4Cl
+ Ca(OH)2 CaCl2+2NH3↑+2H2O (2分)
20.(10分)(一)(1)2NH4Cl
+ Ca(OH)2 CaCl2+2NH3↑+2H2O (2分)