Na
2O
2可用作漂白劑和呼吸面具中的供氧劑.
(1)某學習小組發現:在盛有Na
2O
2的試管中加入足量水,立即產生大量氣泡,當氣泡消失后,向其中滴入1~2滴酚酞試液,溶液變紅;將試管輕輕振蕩,紅色很快褪去;此時再向試管中加入少量MnO
2粉末,又有氣泡產生.
①使酚酞試液變紅是因為
,紅色褪去的可能原因是
.
②加MnO
2粉末后發生的反應
.
寫出Na
2O
2作供氧劑的反應方程式,并用雙線橋表示電子轉移的數目
.
(2)Na
2O
2有強氧化性,H
2具有還原性,有同學猜想Na
2O
2與H
2能反應.為了驗證此猜想,該小組同學進行如下實驗,實驗步驟和現象如下.
步驟1:按圖組裝儀器(圖中夾持儀器省略),檢查氣密性,裝入藥品;
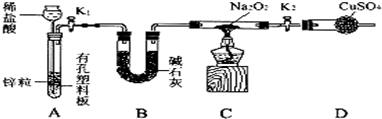
步驟2:打開K
1、K
2,產生的氫氣流經裝有Na
2O
2的硬質玻璃管,一段時間后,沒有任何現象;
步驟3:檢驗H
2的純度后,開始加熱,觀察到硬質玻璃管內Na
2O
2開始熔化,淡黃色的粉末變成了白色固體,干燥管內硫酸銅未變藍色;
步驟4:反應后撤去酒精燈,待硬質玻璃管冷卻后關閉K
1.
①盛裝稀鹽酸的儀器名稱
;B裝置的作用是
.
②必須檢驗氫氣純度的原因是
.
③設置裝置D的目的是
.
④你得到的結論是
(若能反應請用化學方程式表示).

