
題目列表(包括答案和解析)
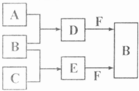 A、B、C是三種常見短周期元素的單質.常溫下D為無色液體,E是一種常見的溫室氣體.其轉化關系如圖(反應條件和部分產物略去).試回答:
A、B、C是三種常見短周期元素的單質.常溫下D為無色液體,E是一種常見的溫室氣體.其轉化關系如圖(反應條件和部分產物略去).試回答:







③n=1 ④n>1
例8下列各組離子在溶液中可以大量共存,且加入氨水后也不產生沉淀的是 ( )
A.Na+ Ba2+ Cl- SO42-
B.K+ AlO2- NO3-
C.H+ NH4+ Al3+ SO42- D.H+ Cl- CH3COO- NO3-
[思路]:離子共存問題,一直是高考的“熱點”。解決這類問題,只要考慮兩大方面即可:(1)能否發生復分解反應,(2)能否發生氧化還原反應。若兩類反應均不發生,則可共存。
[解析]:Al3+只能存在于酸性條件下,故C可共存,但加入氨水后可生成Al(OH)3沉淀,且不溶于溶液中銨鹽;AlO2-存在于堿性環境中,加入氨水后不會產生沉淀;A答案中Ba2+、SO42-不共存,而D中的H+ 和CH3COO-不能共存。故選B。
例9.下列離子方程式正確的是 ( )
A.稀硫酸與氫氧化鋇溶液反應
H++SO42-+Ba2++OH-=BaSO4↓+H2O
B.硫酸鋁溶液中滴入氨水
Al3++3OH-=Al(OH)3 ↓
C.碳酸氫鎂溶液中加入氫氧化鈉溶液
Mg2++2HCO3-+4OH-=Mg(OH)2↓+CO32-+2H2O
D.硝酸鋁溶液中滴加少量的氫氧化鈉溶液
Al3++3OH-=Al(OH)3 ↓
[思路與解析]:A式錯在若一種物質中有兩種或兩種以上的離子參加反應,必須維持在原物質中的微粒數比,在稀硫酸中1個SO42-離子對應兩個H+離子,在氫氧化鋇中1個Ba2+對應2個OH-離子,故該反應的離子方程式為:
2H++SO42-+Ba2++2OH-=BaSO4↓+2H2O
B項中氨水(NH3?H2O)為一元弱堿,是弱電解質,應該保留分子式,故該反應的離子方程式為:Al3++3 NH3?H2O=Al(OH)3↓+3NH4+
C項中的碳酸氫鎂屬易溶且易電離的物質,它與NaOH溶液反應,屬酸式鹽與堿的反應。變成的是正鹽MgCO3,而Mg2+和OH-結合生成的Mg(OH)2因其溶解度較MgCO3低的多,根據離子反應總是向著離子減少的方向進行的規律,Mg2+變成Mg(OH)2而不會生成MgCO3,該離子方程式是正確的。
D項在過量的硝酸鋁溶液中滴加少量的NaOH溶液,生成的Al(OH)3沉淀不會溶解,故該離子方程式是正確的。
故選C、D。
例10 今有鋁、稀硫酸和氫氧化鈉溶液為原料,在實驗室制備一定量的氫氧化鋁。可分別采用如下化學方程式所表示的兩種方法:
①2Al+3H2SO4=Al2(SO4)3+3H2↑
Al2(SO4)3+6NaOH=2Al(OH)3↓+3Na2SO4
②2Al+2NaOH+2H2O=2NaAlO2+3H2↑
2NaAlO2+2H2O+H2SO4=2Al(OH)3↓+Na2SO4
(1)上述那一種方法比較節約試劑?(提示:試從每生產2molAl(OH)3所耗費的試劑用量給予說明)
(2)原料相同,請設計一種更為節約試劑的方法(以方程式表示,并說明其可以最節約試劑的根據)。
思路與解析:(1)Al即可以跟稀硫酸,也可跟氫氧化鈉溶液反應放出氫氣。反應后如果再以H2SO4或NaOH溶液處理,實際上是調控pH,使之得到Al(OH)3,達到制備的目的。先用酸,后用堿,還是先用堿,后用酸,都是可行的,但是耗用的酸、堿用量卻不同。同樣是制備2molAl(OH)3,前法需2molAl、3molH2SO4、6molNaOH;后法只需2molAl、1molH2SO4、2molNaOH,顯然,后法較前法節約了酸、堿試劑。
(2)仔細觀察第一種方法,它第一步生成的是Al2(SO4)3,略有酸性,所以要用較多的NaOH。第二種方法生成的是NaAlO2,略有堿性,所以要用較多的硫酸。因此,設想是否能用略有酸性的Al2(SO4)3和略有堿性的NaAlO2自己中和呢?聯合兩法可設計出第三種方法。
2Al+3H2SO4=Al2(SO4)3+3H2↑
2Al+2NaOH+2H2O=2NaAlO2+3H2↑
Al2(SO4)3+6NaAlO2+12H2O=8Al(OH)3↓+3Na2SO4
相當于制備2molAl(OH)3需要的原料為2molAl、0.75molH2SO4、1.5molNaOH,確實節約了試劑。
例11:某復鹽的化學式AxB(ED4)y?z H2O,已知x、y、z均為正整數,且x+y+z=10,用該晶體完成下列實驗:①稱取晶體40.2g,加熱至質量不再改變,質量減少了10.8g,②將剩余固體溶于水,配成200mL溶液,取出20mL,向其中加入過量的Ba(OH)2溶液,ED4離子和B離子完全沉淀,經測定為5.24g,③將沉淀物加到足量的鹽酸中,固體質量又減少了0.580g。
試通過計算和推理回答A、B是何種元素及晶體的化學式。
[思路]:所謂復鹽,即含有兩種或兩種以上的金屬離子(含NH4+ )和一種酸根離子的鹽。題設復鹽的化學式為AxB(ED4)y?z H2O,顯然A、B為簡單金屬離子;ED4離子和B離子與過量的Ba(OH)2溶液反應得到兩種沉淀物,顯然是陰離子ED4離子與Ba2+ 結合得一沉淀,陽離子B離子與OH-結合得一沉淀,且可溶于鹽酸的必為B離子與OH-結合得到的金屬B的難溶氫氧化物,另一不溶于鹽酸的必為ED4離子與Ba2+ 結合得到的難溶性鋇鹽,而且從陰離子的形式使我們想起了SO42-,即初步確認難溶性鋇鹽為BaSO4。
[解析]:這類問題的解決,一般還要輔之于定量的計算,由題給實驗數據,在
結晶水的物質的量為:10.8g÷18g/mol=0.600mol
初步確認的SO42-的物質的量為:{(5.24g-0.580g)÷233g/mol}×200mL/20mL=0.200mol
這樣,該復鹽中y:z=0.200:0.600=1:3
這就找到了解決問題的突破口,因為有了y:z=1:3,加之題給x+y+z=10,就創造了利用數學手段,結合化學意義進行討論進而確認的機會。討論:
當y=1時,z=3,則x=6,依該結論,則該復鹽的化學式當初步確定為A6B(ED4)?3H2O,這顯然與化合價法則相矛盾。原假設不能成立。
當y=2時,z=6,則x=2,依該結論,則該復鹽的化學式當初步確定為A2B(ED4)2?6H2O,且可能成立的情況必然為A為+1價,則B必為+2價。依上述推論推得的40.2g中含結晶水0.600mol,則含A為0.200mol、B為0.100mol,可知生成金屬B的氫氧化物的化學式為B(OH)2,且其摩爾質量為:
(0.58g×200mL/20mL)/0.100mol=58.0g/mol
易得金屬B的相對原子質量為58.0-17.0×2=24.0,顯然B元素為Mg。40.2g復鹽中A元素的質量為:
金屬A的摩爾質量為:7.80g÷0.2mol=39.0g/mol,所以A元素為K元素。
這樣復鹽的化學式是K2Mg(SO4)2?6H2O。
例12.向已知含有Zn2+的溶液中滴加氨水,有白色沉淀Zn(OH)2生成,繼續滴加氨水使其過量,沉淀溶解,生成了[Zn(NH3)4](OH)2。此外Zn(OH)2即可溶于鹽酸,又可溶于NaOH溶液,生成ZnO22-,所以Zn(OH)2是一種兩性氫氧化物。
現有四種離子,每組有兩種金屬離子。請各選一種試劑,將它們兩者分開。可供選擇的試劑有:
A.硫酸 B.鹽酸 C.硝酸 D.氫氧化鈉溶液 E.氨水
根據上述內容填寫下表:
離子組
選用試劑代號
沉淀物化學式
保留在溶液中的離子
①Zn2+和Al3+
②Zn2+和Mg2+
③Zn2+和Ba2+
④Mg2+和Al3+
[思路]:本題給出的知識性信息是Zn(OH)2兩性和可生成溶于水的[Zn(NH3)4](OH)2。運用它們的化學性質,選擇適當的試劑加以分離。
[解析]:①Zn2+和Al3+的分離:由于Al(OH)3和Zn(OH)2均為兩性氫氧化物,不能用酸堿加以區分,但是Zn2+可與過量的氨水反應,生成Zn(NH3)42+,Al3+無此性質,可選用氨水(E)為試劑,生成沉淀Al(OH)3,留在溶液中的為Zn(NH3)42+。
②Zn2+和Mg2+的分離:因Zn(OH)2為兩性氫氧化物,Mg(OH)2無兩性且為難溶于水的沉淀,可選用NaOH(D)為試劑。沉淀為Mg(OH)2,留在溶液中的離子為:ZnO22-。
③Zn2+和Ba2+的分離:由于BaSO4難溶于水且不溶于酸,而ZnSO4則能溶于水,可選用H2SO4(A)為試劑。沉淀為BaSO4,保留在溶液中的離子為Zn2+。
④Mg2+和Al3+的分離:Al(OH)3有兩性,能溶于過量的NaOH溶液中,Mg(OH)2無兩性且為難溶于水的沉淀,可選用NaOH(D)為試劑。沉淀為Mg(OH)2,留在溶液中的離子為:AlO2-。
4.實戰演練
一、選擇題
1.(2001年春季高考題)將一定質量的Mg、Zn、Al混合物與足量稀H2SO4反應,生成H2
A
C
2.將某物質的量的鎂和鋁相混合,取等質量的該混合物四份,分別加到足量的下列溶液中,充分反應后,放出氫氣最多的是?
A.3 mol?L-1 HCl?
B.4 mol?L-1的HNO3?
C.8 mol?L-1 NaOH?
D.18 mol?L-1 H2SO4?
3.人的純凈的胃液是一種強酸性液體,pH在0.9~1.5左右,氫氧化鋁是一種治療胃液過多的胃藥的主要成分,目前這種胃藥已不常用,原因主要是?
A.長期攝入鋁元素不利于人體健康?
B.它不能中和胃液?
C.它不易溶于胃液?
D.它的療效太差?
4.下列氣體逐漸通入NaAlO2溶液中,開始時產生沉淀,繼續通入氣體時沉淀又溶解,該氣體是?
A.NO2 B.NO?
C.CO2 D.H2S?
5.在硝酸鋁和硝酸鎂的混合溶液中,逐滴加入稀氫氧化鈉溶液,直至過量。下列表示氫氧化鈉加入量(x)與溶液中沉淀物的量(y)的關系示意圖中正確的是?

6.在氯化鎂和硫酸鎂的混合液中,若Mg2+與Cl-的物質的量濃度之比為4∶3時,下列判斷正確的是?
A.溶液中Mg2+與SO 的物質的量濃度相等?
的物質的量濃度相等?
B.溶液中Mg2+與SO 物質的量濃度之比為5∶8?
物質的量濃度之比為5∶8?
C.溶液中Mg2+與SO 物質的量濃度之比為8∶5?
物質的量濃度之比為8∶5?
D.溶液中氯化鎂和硫酸鎂物質的量相等?
7.將AlCl3溶液和NaOH溶液等體積混合得到的沉淀物和溶液中所含鋁元素的質量相等,則原AlCl3溶液和NaOH溶液物質的量濃度之比可能是?
A.2∶3 B.1∶3?
C.1∶4 D.2∶7?
8.m g鈉、鋁混合物,放入n g水中,反應停止后,仍有不溶物a g,則溶液中溶質為
A.NaOH?
B.NaAlO2?
C.NaOH和NaAlO2?
D.無法確定?
9.將鋁粉放入燒堿溶液中,若反應過程中有1.5 mol電子發生轉移,則參加反應的水為?
A.9 g? B.18 g?
C.0.5 mol? D. mol?
mol?
10.將物質X逐漸加入Y溶液中,生成沉淀物質的量n2與所加X的物質的量n1的關系如圖所示。符合圖示情況的是?

A
B
C
D
X
NaOH
AlCl3
HCl
NaAlO2
Y
AlCl3
NaOH
NaAlO2
HCl
二、非選擇題(共50分)?
11.(12分)在50 mL b mol?L-1 AlCl3溶液中加入50 mL a mol?L-1 NaOH溶液。
(1)當a≤3b時,生成Al(OH)3沉淀的物質的量為 。?
(2)當a、b滿足 條件時,先有沉淀,后又有部分沉淀溶解,此時Al(OH)3的質量為 g。
12.(12分)今用鋁、稀硫酸和氫氧化鈉溶液為原料,在實驗室制備一定量的氫氧化鋁。可分別采用如下化學方程式所表示的兩種方法:?
①2Al+3H2SO4===Al2(SO4)3+3H2↑?
Al2(SO4)3+6NaOH===2Al(OH)3↓+3Na2SO4?
②2Al+2NaOH+2H2O===2NaAlO2+3H2↑?
2NaAlO2+H2SO4+2H2O===2Al(OH)3↓+Na2SO4?
(1)上述哪一種方法比較節約試劑?[提示:試從每生產2 mol Al(OH)3所耗費的試劑用量予以說明]?
(2)原料相同,請設計一種更為節約試劑的方法(以方程式表示,并說明其可以最節約試劑的根據)。?????????
13.(10分)鎂是一種很活潑的金屬,常用作脫硫劑、脫氧劑。在電子工業中利用鎂制取硅的反應為:?
2Mg+SiO2 2MgO+Si?
2MgO+Si?
同時有副反應發生:2Mg+Si Mg2Si?
Mg2Si?
Mg2Si遇鹽酸迅速反應生成SiH4(硅烷)。?
SiH4在常溫下是一種不穩定、易分解的氣體。?

(1)圖(甲)是進行Mg與SiO2反應的實驗裝置。?
Ⅰ.由于O2的存在對該實驗有較大影響,實驗中應通入X氣體作為保護氣。X氣體應選用①CO2、②N2、③H2中的 。
Ⅱ.實驗開始時,必須先通入X的氣體,再接通電源加熱反應物,其理由是 ;當反應引發后,切斷電源,反應能繼續進行,其原因是 。
Ⅲ.反應結束時,待冷卻至常溫后,關閉K,從分液漏斗處加入稀鹽酸,可觀察到導管口a處有閃亮的火星。據此現象可推知 在空氣中能自燃。?
(2)圖(乙)所示裝置進行的實驗如下:先關閉K,使A中反應進行;加熱玻璃管C,可觀察到C管中發出耀眼白光,產生白煙,管壁上附著有淡黃色物質。實驗完成后,將C管中固體全部加入鹽酸中,有臭雞蛋氣味的氣體生成。?
Ⅰ.C中的Mg應放在不銹鋼墊片上而不能直接接觸管壁,這是因為 。
Ⅱ.停止實驗時,先打開K,再停止滴加濃硫酸并熄滅酒精燈。橡膠氣膽B在實驗中的作用是 。
Ⅲ.C中全部反應產物有 、 、 。(填化學式)?
14.(8分)有鋁粉和四氧化三鐵組成的鋁熱劑,在隔絕空氣的條件下灼燒,使之充分反應。將所得混合物研細并分成兩等份,分別投入過量的燒堿溶液和鹽酸中。充分反應后,前者消耗m mol NaOH,放出氣體0.
(1)該鋁熱劑的質量分數。?
(2)m、n、V的值。
15.(8分)在標準狀況下進行甲、乙、丙三組實驗,三組各取30 mL同濃度的鹽酸溶液,加入同一種鎂鋁合金粉末,產生氣體,有關數據列表如下:?
實驗序號
甲
乙
丙
合金質量(mg)
255
385
459
生成氣體體積(mL)
280
336
336
(1)甲組實驗中,鹽酸 (填“過量”“適量”或“不足量”),理由是 。乙組實驗中,鹽酸 (填“過量”“適量”或“不足量”),理由是 。要算出鹽酸的物質的量濃度,題中可作計算依據的數據是 ,求得的鹽酸的物質的量濃度為 。
(2)求合金中Mg、Al的物質的量之比,題中可作計算依據的數據是 ,求得的Mg、Al的物質的量之比為 。
(3)在丙組實驗之后,向容器中加入1 mol?L-1的氫氧化鈉溶液,能使合金中的鋁恰好溶解,不形成含鋁的沉淀,并使Mg2+剛好沉淀完全,再過濾出不溶固體,求濾液中各溶質的物質的量和所加入氫氧化鈉溶液的體積(寫計算過程)。
附參考答案
一、1.C?
2.解析:鎂、鋁不能與HNO3、濃H2SO4反應產生H2;Mg不與NaOH反應,Al能;Mg\,Al都能與鹽酸反應產生H2。?
答案:A?
3.A 4.A 5.C 6.C 7.AD 8.B 9.AC 10.C?
二、11.(1) a mol (2)3b<a<4b (15.6b-
a mol (2)3b<a<4b (15.6b-
12.(1)方法②比方法①更節約試劑。?
(2)2Al+3H2SO4===Al2(SO4)3+3H2↑?
2Al+2NaOH+2H2O===2NaAlO2+3H2↑?
Al2(SO4)3+6NaAlO2+12H2O===8Al(OH)3↓+3Na2SO4?
相當于制備2molAl(OH)3所用原料為2mol Al、 mol H2SO4、1.5 mol NaOH,確實節約了試劑。
mol H2SO4、1.5 mol NaOH,確實節約了試劑。
13.(1)Ⅰ.③ Ⅱ.防止加熱條件下H2與空氣混合爆炸 Mg與SiO2的反應是放熱反應 Ⅲ.SiH4?
(2)Ⅰ.同在加熱條件下,Mg能與玻璃中的SiO2反應 Ⅱ.防止C管降溫時因氣體壓強減小,而引起D中溶液倒流 Ⅲ.MgO S MgS?
14.(1)Al:27.95% Fe3O4:72.05%?
(2)m=0.05 mol n=0.24 mol V=
15.(1)過量
因為乙組所用合金量比甲組多,產生H2也多,說明甲組中HCl未反應完 不足量 因為甲組255 g合金生成H2 280 mL,每克合金生成H2: mL。若乙組中合金耗盡,應生成H2:
mL。若乙組中合金耗盡,應生成H2: ×385=423 mL,實際只生成336 mL,所以鹽酸不足量
鹽酸30 mL、氣體336 mL 1 mol?L-1?
×385=423 mL,實際只生成336 mL,所以鹽酸不足量
鹽酸30 mL、氣體336 mL 1 mol?L-1?
(2)合金255 mg,氣體280 mL 1∶1?
(3)濾液中溶質為NaCl,NaAlO2?
設丙組中Mg、Al的物質的量均為x?
則24x+27x=0.459 x=0.009 mol?
根據Cl元素守恒:?
n(NaCl)=n(HCl)=1×0.03=0.03 mol?
根據Al元素守恒:n(NaAlO2)=n(Al)=0.009 mol?
由Na元素守恒:n(NaOH)=n(NaCl)+n(NaAlO2)=0.03+0.009
=0.039 mol
V(NaOH)= =0.039 L=39 mL
=0.039 L=39 mL
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com