
題目列表(包括答案和解析)
在0.5 L某濃度的NaCl溶液中含有0.5 mol Na+,下列對該溶液的說法中,不正確的是( )
A.該溶液的物質的量濃度為1 mol·L-1
B.該溶液中含有58.5 g NaCl
C.配制1000 mL該溶液需用58.5 g NaCl
D.量取100 mL該溶液倒入燒杯中,燒杯中Na+的物質的量為0.1 mol
在0.5 L某濃度的NaCl溶液中含有0.5 mol Na+,下列對該溶液的說法中,不正確的是
A.該溶液的物質的量濃度為1 mol·L-1
B.該溶液中含有58.5 g NaCl
C.配制100 mL該溶液需用5.85 g NaCl
D.量取100 mL該溶液倒入燒杯中,燒杯中Na+的物質的量為0.1 mol
聯堿法(候氏制堿法)和氨堿法的生產流程簡要表示如下圖: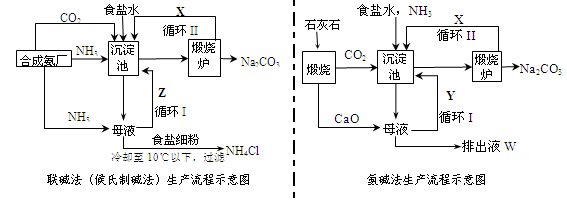
(1)兩種方法的沉淀池中均發生的反應化學方程式為_____________________________。
(2)若沉淀池含800.00 mol NH3的水溶液質量為54.00 kg,向該溶液通入二氧化碳至反應完全,過濾,得到濾液31.20kg,則NH4HCO3的產率為______________%。
(3)在氨堿法生產過程中氨要循環使用,但不需要補充,在母液中加生石灰前先要加熱的原因是 ___ 。
(4)根據聯堿法中從濾液中提取氯化銨晶體的過程推測,所得結論正確是_______(選填編號)。
a.常溫時氯化銨的溶解度比氯化鈉小
b.通入氨氣能增大NH4+的濃度,使氯化銨更多析出
c.加入食鹽細粉能提高Na+的濃度, 使NaHCO3結晶析出
d.通入氨氣能使NaHCO3轉化為Na2CO3,提高析出的NH4Cl純度
(5)聯堿法相比于氨堿法,氯化鈉利用率從70%提高到90%以上,主要是設計了循環Ⅰ,聯堿法的另一項優點是__________________________________________________。
(6)從沉淀池析出的晶體含有NaCl雜質,某同學在測定其NaHCO3的含量時,稱取5.000g試樣,配制成100mL溶液,用標準鹽酸溶液滴定(用甲基橙做指示劑),測定數據記錄如下:
| 滴定次數 | 待測液(mL) | 0.6000mol/L鹽酸溶液的體積(mL) | |
| 初讀數 | 終讀數 | ||
| 第一次 | 20.00 | 1.00 | 21.00 |
| 第二次 | 20.00 | 如右圖Ⅰ | 如右圖Ⅱ |
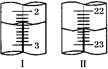 顯示消耗的鹽酸溶液體積為 。
顯示消耗的鹽酸溶液體積為 。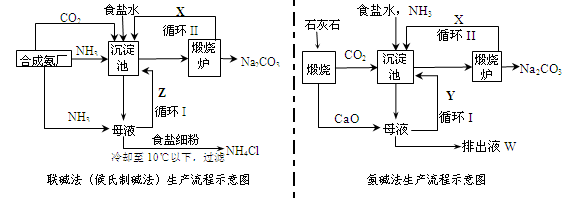
| 滴定次數 | 待測液(mL) | 0.6000mol/L鹽酸溶液的體積(mL) | |
| 初讀數 | 終讀數 | ||
| 第一次 | 20.00 | 1.00 | 21.00 |
| 第二次 | 20.00 | 如右圖Ⅰ | 如右圖Ⅱ |
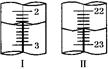 顯示消耗的鹽酸溶液體積為 。
顯示消耗的鹽酸溶液體積為 。湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com