
科目: 來源: 題型:
【題目】甲醛(HCHO)俗稱蟻醛,是一種重要的化工原料。可通過以下方法將甲醇轉化為甲醛。
脫氫法:CH3OH(g)=HCHO(g)+H2(g) ΔH1=+92.09 kJ·mol-1
氧化法:CH3OH(g)+![]() O2(g)=HCHO(g)+H2O(g)ΔH2
O2(g)=HCHO(g)+H2O(g)ΔH2
回答下列問題:
(1)已知:2H2(g)+O2(g)=2H2O(g)ΔH3=-483.64 kJ·mol-1,則ΔH2=_________________。
(2)與脫氫法相比,氧化法在熱力學上趨勢較大,其原因為________________________________________。
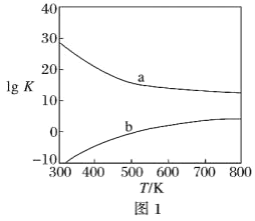
(3)圖1為甲醇制備甲醛反應的lg K(K為平衡常數)隨溫度(T)的變化曲線。曲線_____(填“a”或“b”)對應脫氫法,判斷依據是_____________________________________。
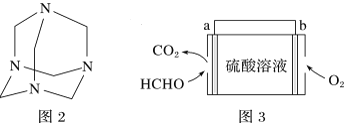
(4)將甲醛水溶液與氨水混合蒸發可制得烏洛托品(結構簡式如圖2),該物質在醫藥等工業中有廣泛用途。若原料完全反應生成烏洛托品,則甲醛與氨的物質的量之比為___________。
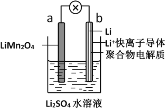
(5)室內甲醛超標會危害人體健康,通過傳感器可以監測空氣中甲醛的含量。一種燃料電池型甲醛氣體傳感器的原理如圖3所示,則a極的電極反應式為_________________________________________________,當電路中轉移4×10-4 mol電子時,傳感器內參加反應的HCHO為________________mg。
查看答案和解析>>
科目: 來源: 題型:
【題目】新能源汽車所用蓄電池分為鉛酸蓄電池、二次鋰電池、空氣電池等類型。請回答下列問題:
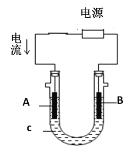
(1)2019年諾貝爾化學獎授予了為鋰離子電池發展做出貢獻的約翰·班寧斯特·古迪納夫等三位科學家。如圖所示為水溶液鋰離子電池體系。放電時,電池的負極是_______(填a或b),溶液中Li+從______遷移(填“a向b”或“b向a”)。
(2)鉛酸蓄電池是最常見的二次電池,電壓穩定,安全可靠,價格低廉,應用廣泛。電池總反應為Pb(s)+PbO2(s)+2H2SO4(aq) ![]() 2PbSO4(s)+2H2O(l)
2PbSO4(s)+2H2O(l)
①放電時,正極的電極反應式是________________________,電解質溶液中硫酸的濃度_____(填“增大”、“減小”或“不變”),當外電路通過0.5 mol e-時,理論上負極板的質量增加_______g。
②用該蓄電池作電源,進行粗銅(含Ag、Pt、Au等雜質)的電解精煉。如下圖所示,電解液c選用________溶液,A電極的材料是_______,B電極反應式是_________。
③用該蓄電池作電源,A、B為石墨電極,c為氯化鈉溶液,進行電解。如上圖所示,則A電極產生的氣體是________,B電極附近溶液的pH_____(填“增大”、“減小”或“不變”)。
查看答案和解析>>
科目: 來源: 題型:
【題目】下列圖示與對應敘述相符的是
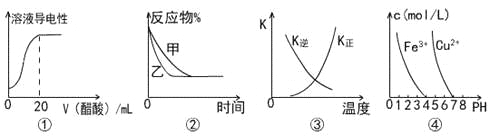
A.圖①表示向20 mL 0.1 mol/L氨水中逐滴加入0.1 mol/L醋酸,溶液導電性隨加入酸體積的變化
B.圖②表示壓強對可逆反應A(g)+2B(g)![]() 3C(g)+D(s)的影響,乙的壓強比甲的壓強大
3C(g)+D(s)的影響,乙的壓強比甲的壓強大
C.圖③中曲線表示反應3A(g) + B(g)![]() 2C(g)△H<0,正、逆反應的平衡常數K隨溫度的變化
2C(g)△H<0,正、逆反應的平衡常數K隨溫度的變化
D.據圖④,若要除去CuSO4溶液中的Fe3+,可加入NaOH溶液至pH在4左右
查看答案和解析>>
科目: 來源: 題型:
【題目】用煤油作溶劑,二(2-乙基己基)磷酸酯作流動載體,H2SO4 作內相酸處理含銅廢水。 在其他條件相同時,Cu2+萃取率[萃取率= ×100% ]與初始 Cu2+濃度關系如圖 1 所示;在其他條件相同時,處理前初始 Cu2+濃度為 200 mg·L-1,Cu2+萃取率與廢水 pH 的關系如圖 2 所示。下列說法錯誤的是
×100% ]與初始 Cu2+濃度關系如圖 1 所示;在其他條件相同時,處理前初始 Cu2+濃度為 200 mg·L-1,Cu2+萃取率與廢水 pH 的關系如圖 2 所示。下列說法錯誤的是
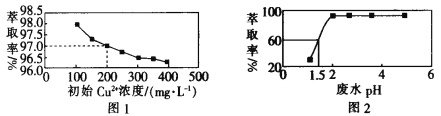
A.根據圖 1 可知,廢水中初始 Cu2+濃度越大,Cu2+的萃取效果越好
B.根據圖 2 可知,廢水初始 pH>2 時,去除 Cu2+的效果較好
C.根據圖 1 可知,Cu2+初始濃度為 200 mg·L-1 時,Cu2+的萃取率為 97.0%
D.根據圖 2 可知,若取 800 mL 初始 Cu2+濃度為 200 mg·L-1 的廢水,在 pH=1.5 時處理廢水,則處理后的廢水中剩余 Cu2+的物質的量為 1.5×10-3mol(假設體積不變)
查看答案和解析>>
科目: 來源: 題型:
【題目】如圖所示,甲池的總反應式為:N2H4+O2=N2+H2O,下列關于該電池工作時的說法正確的是( )

A. 該裝置工作時,Ag電極上有氣體生成
B. 甲池中負極反應為N2H4-4e-=N2+4H+
C. 甲池和乙池中的溶液的pH均減小
D. 當甲池中消耗0.1molN2H4時,乙池中理論上最多產生6.4g固體
查看答案和解析>>
科目: 來源: 題型:
【題目】在2 L的密閉容器中充入2 molX(g)和1 mol Y(g),發生反應2X(g) +Y(g) ![]() 3Z(g) △H,反應過程中持續升高溫度,測得混合體系中X的體積分數與溫度的關系如圖所示,下列推斷正確的是
3Z(g) △H,反應過程中持續升高溫度,測得混合體系中X的體積分數與溫度的關系如圖所示,下列推斷正確的是

A.升高溫度.平衡常數增大
B.W點Y的正反應速率等于M點Y的正反應速率
C.Q點時,Y的轉化率最大
D.平衡時充入3molZ,達到新平衡時Z的體積分數比原平衡時大
查看答案和解析>>
科目: 來源: 題型:
【題目】25℃時,向0.10mol·L-1的H2C2O4(二元弱酸)溶液中滴加NaOH溶液,溶液中部分微粒的物質的量濃度隨pH的變化曲線如圖所示。下列說法不正確的是

A. 25℃時H2C2O4的一級電離常數為Ka1=104.3
B. pH=2.7的溶液中:c(H2C2O4)=c(C2O42-)
C. pH=7的溶液中:c(Na+)>2c(C2O42-)
D. 滴加NaOH溶液的過程中始終存在:c(OH-)+2c(C2O42-)+c(HC2O4-)=c(Na+)+c(H+)
查看答案和解析>>
科目: 來源: 題型:
【題目】碘循環工藝不僅能吸收SO2降低環境污染,同時又能制得氫氣,具體流程如下:
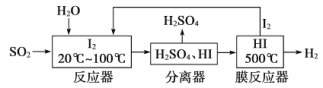
下列說法正確的是
A.分離器中的物質分離操作為過濾
B.反應器中,控制溫度為20-100℃,溫度過低速率慢,過高水氣化且增大碘的流失,反應速率也慢
C.該工藝中I2和HI的相互轉化體現了“碘循環”
D.碘循環工藝的總反應為2SO2+4H2O+I2=H2+2H2SO4+2HI
查看答案和解析>>
科目: 來源: 題型:
【題目】化學與社會生活密切相關,下列說法正確的是( )
A.軍艦船底鑲嵌鋅塊作正極,以防船體被腐蝕
B.汽車尾氣中NO和CO可以緩慢反應生成N2和CO2,減小壓強,反應速率減慢
C.金屬冶煉過程是金屬離子得電子變成金屬單質的氧化過程
D.PM2.5顆粒![]() 微粒直徑約為2.5×106m)分散在空氣中形成氣溶膠
微粒直徑約為2.5×106m)分散在空氣中形成氣溶膠
查看答案和解析>>
科目: 來源: 題型:
【題目】按要求回答下列問題。
(1)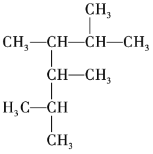 的名稱為______。
的名稱為______。
(2) 的名稱為______。
的名稱為______。
(3)3-甲基-2-戊烯的結構簡式為______。
(4)1,3,5-三甲基苯的結構簡式為______。
(5)某烷烴的相對分子質量為72,其一氯代物只有一種,該烷烴的結構簡式為______。
(6)2,3-二甲基-2-丁烯的鍵線式為______。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com