
科目: 來源: 題型:
【題目】利用pH傳感器探究NaOH溶液與硫酸、硫酸銅混合溶液發生反應的離子反應順序,繪得三份曲線圖如圖。已知實驗使用的NaOH溶液濃度和滴速相同;硫酸溶液和硫酸銅溶液濃度相同;混合溶液中兩溶質的濃度也相同。
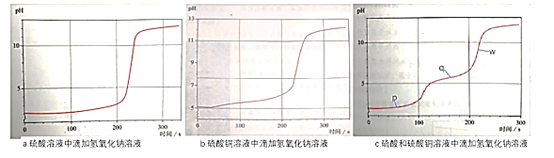
以下解讀錯誤的是
A.三個時點的c(Cu2+):p>q>w
B.w點:c(Na+)>c(SO42-)>c(Cu2+)>c(H+)
C.混合溶液中滴加NaOH溶液,硫酸先于硫酸銅發生反應
D.q點時溶液離子濃度:c(SO42-)+c(OH-)=c(Cu2+)+c(H+)+c(Na+)
查看答案和解析>>
科目: 來源: 題型:
【題目】元素X、Y、Z、W均為短周期元素,且原子序數依次增大。已知Y原子最外層電子數占核外電子總數的3/4,W-、Z+、X+的離子半徑逐漸減小,化合物XW常溫下為氣體,Z是本周期中除稀有氣體元素外,原子半徑最大的元素。據此回答下列問題:
(1)W在元素周期表中的位置___________________,實驗室制取W單質的離子方程式是____________________________________________________________;
(2)A、B均由上述四種元素中的三種組成的強電解質,A是一種強堿,B是某種家用消毒液的有效成分,則A、B的化學式分別為___________、____________;
(3)C是由Y和Z兩種元素組成的一種化合物,其中Y和Z的原子個數比為1∶1,則C的電子式是____________;
查看答案和解析>>
科目: 來源: 題型:
【題目】A、B、W、D、E為短周期元素,且原子序數依次增大,質子數之和為39,B、W同周期,A、D同主族,A、W能形成兩種液態化合物A2W和A2W2,E元素的周期序數與主族序數相等.
(1)W2-離子的結構示意圖為______________,E元素在周期表中的位置為____________,寫出E的最高價氧化物與D的最高價氧化物的水化物反應的離子方程式____________________。
(2)經測定A2W2為二元弱酸,A2W2的電子式為___________,常用硫酸處理BaO2來制備A2W2,寫出該反應的化學方程式__________________________。
(3)向含有Fe2+和淀粉KI的酸性溶液中滴入A2W2,觀察到溶液呈藍色并有紅褐色沉淀成.當消耗2mol I﹣時,共轉移3mol電子,該反應的離子方程式是_____________________。
(4)元素D的單質在一定條件下,能與A單質化合生成一種化合物DA,熔點為800℃,能與水反應放氫氣,寫出該反應方程式______________________,若將1molDA和1molE單質混合加入足量的水,充分反應后生成氣體的體積是_________L(標準狀況下)。
查看答案和解析>>
科目: 來源: 題型:
【題目】某抗癌藥物的結構簡式如圖所示,其中W、X、Y、Z是原子序數依次增大的短周期主族元素,W、Y同主族,Y、Z的最外層電子數之和是X的最外層電子數的2倍。下列敘述正確的是
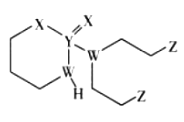
A.元素的非金屬性:W>Z>X
B.Y的最高價氧化物的水化物是強酸
C.W的最簡單氫化物與Z的單質混合后可產生白煙
D.Y、Z形成的化合物中,每個原子均滿足8電子結構
查看答案和解析>>
科目: 來源: 題型:
【題目】某可充電鈉離子電池放電時工作原理如圖所示,下列說法錯誤的是
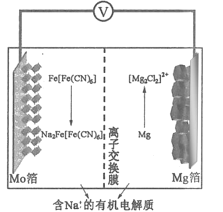
A.放電時電勢較低的電極反應式為:Fe[Fe(CN)6]+2Na++2e-=Na2Fe[(CN)6]
B.外電路中通過0.2 mol電子的電量時,負極質量變化為2.4 g
C.充電時,Mo箔接電源的正極
D.放電時,Na+從右室移向左室
查看答案和解析>>
科目: 來源: 題型:
【題目】生物固氮與模擬生物固氮都是重大基礎性研究課題。大連理工大學曲景平教授團隊設計合成了一類新型鄰苯二硫酚橋聯雙核鐵配合物,建立了雙鐵分子仿生化學固氮新的功能分子模型。如圖是所發論文插圖。以下說法錯誤的是
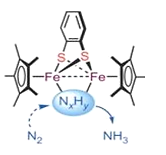
A.催化劑不能改變反應的焓變
B.催化劑不能改變反應的活化能
C.圖中反應中間體NXHY數值X<3
D.圖示催化劑分子中包含配位鍵
查看答案和解析>>
科目: 來源: 題型:
【題目】3.2 g某元素A 的單質與氫氣化合生成3.4 g氣態氫化物H2A,已知A 的原子核中質子數和中子數相等,則:
(1) A的原子序數為______;
(2) 元素A位于元素周期表中位置:____ _____;
(3) 氣態氫化物的化學式是_____,并書寫氣態氫化物的電子式_______。
查看答案和解析>>
科目: 來源: 題型:
【題目】回答下問題:
(1)C、N、O三種元素的第一電離能由大到小的順序是__________________。
(2)C、Si、N的電負性由大到小的順序是__________________。
(3)氟化氫水溶液中存在的氫鍵有_________種。
(4)金屬鎳及其化合物在合金材料以及催化劑等方面應用廣泛,Ni的基態原子有________種能量不同的電子。很多不飽和有機物在Ni催化下可以H2發生加成反應。如①CH2=CH2、②HC≡CH、③![]() 、④HCHO,其中碳原子采取sp2雜化的分子有__________(填物質編號),HCHO分子的立體構型為______________。
、④HCHO,其中碳原子采取sp2雜化的分子有__________(填物質編號),HCHO分子的立體構型為______________。
查看答案和解析>>
科目: 來源: 題型:
【題目】下表是元素周期表短周期的一部分:

請按要求用化學用語回答下列問題:
(1)元素④、⑥、⑨的離子半徑由大到小的順序為________________;
(2)元素②、③、④的簡單氫化物的沸點由低到高的順序: _____________________;
(3)用電子式表示元素④與元素⑥形成的化合物的形成過程____________;
(4)比元素⑦的原子序數多17的元素在周期表的位置為________________;
(5)寫出由①④⑤三種元素組成的一種離子化合物的電子式_______________,若將其溶于水,破壞了其中的__________(填“離子鍵”、“共價鍵”或“離子鍵和共價鍵”);
(6)元素①和元素④形成的化合物及元素①和元素⑧形成的化合物均為18電子分子,請寫出這兩種化合物按物質的量之比4:1反應的離子方程式________。
查看答案和解析>>
科目: 來源: 題型:
【題目】已知:A、B、C、D、E、F六種元素核電荷數依次增大,屬周期表中前四周期的元素。其中A原子核外有三個未成對電子;化合物B2E的晶體為離子晶體,E原子核外的M層中只有兩對成對電子;C元素是地殼中含量最高的金屬元素;D單質的熔點在同周期元素形成的單質中最高;F能形成紅色(或磚紅色)的F2O和黑色的FO兩種氧化物。
回答下列問題:
(1)F的原子的M層電子排布式為 。
(2)B、C、D的第一電離能由小到大的順序為 。(用元素符號表示)
(3)A的簡單氫化物分子極易溶于水,其主要原因是 。
(4)E的最高價氧化物分子的空間構型是 ,其中心原子的雜化方式為 。
(5)F的高價離子與A的簡單氫化物形成的配離子,不考慮空間構型,配離子的結構可用示意圖表示為 。

(6)A、F形成某種化合物的晶胞結構如圖所示,則其化學式為 ;(黑色球表示F原子),已知緊鄰的白球與黑球之間的距離為a cm,該晶胞的密度為 g/cm3。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com