
科目: 來源: 題型:
【題目】將V1mL 1.0 mol·L-1鹽酸溶液和V2mL未知濃度的氫氧化鈉溶液混合均勻后測量并記錄溶液溫度,實驗結果如圖所示(實驗中始終保持V1+V2=50 mL)。
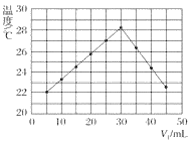
下列敘述正確的是( )
A.做該實驗時環境溫度為20 ℃
B.該實驗表明化學能可能轉化為熱能
C.氫氧化鈉溶液的濃度約為1.0 mol·L-1
D.該實驗表明有水生成的反應都是放熱反應
查看答案和解析>>
科目: 來源: 題型:
【題目】如圖所示,其中甲池的總反應式為2CH3OH+3O2+4KOH===2K2CO3+6H2O,下列說法正確的是
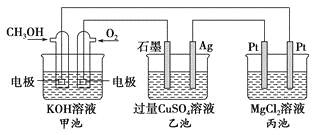
A. 甲池是電能轉化為化學能的裝置,乙、丙池是化學能轉化電能的裝置
B. 甲池通入CH3OH的電極反應式為CH3OH-6e-+2H2O===CO32-+8H+
C. 反應一段時間后,向乙池中加入一定量Cu(OH)2固體能使CuSO4溶液恢復到原濃度
D. 甲池中消耗280 mL(標準狀況下)O2,此時丙池中理論上最多產生1.45 g固體
查看答案和解析>>
科目: 來源: 題型:
【題目】在一定溫度下,向一個容積可變的容器中,通入3 mol SO2和2 mol O2及固體催化劑,使之發生反應:2SO2(g)+O2(g) ![]() 2SO3(g) ΔH=—196.6 kJ·mol-1,一段時間后達到平衡,平衡時容器內氣體總的物質的量為起始時的90%.下列說法正確的是 ( )
2SO3(g) ΔH=—196.6 kJ·mol-1,一段時間后達到平衡,平衡時容器內氣體總的物質的量為起始時的90%.下列說法正確的是 ( )
A.達到平衡時SO2的轉化率約為33.3%
B.達到平衡時反應放出的熱量為294.9 kJ
C.平衡時SO3的物質的量為2mol
D.達平衡時用O2表示的反應速率為0.25 mol·L-1·min-1
查看答案和解析>>
科目: 來源: 題型:
【題目】在密閉容器中的一定量混合氣體發生反應:xA(g) +yB(g)![]() z C(g),平衡時測得A的濃度為0.50 mol/L,保持溫度不變,將容器的容積擴大到原來的兩倍。再達平衡時,測得A的濃度為0.30 mol/L。下列有關判斷正確的是( )
z C(g),平衡時測得A的濃度為0.50 mol/L,保持溫度不變,將容器的容積擴大到原來的兩倍。再達平衡時,測得A的濃度為0.30 mol/L。下列有關判斷正確的是( )
A.x+y < zB.平衡向正反應方向移動
C.C的體積分數下降D.B的轉化率升高
查看答案和解析>>
科目: 來源: 題型:
【題目】通過加入適量乙酸鈉,設計成微生物電池可以將廢水中的氯苯轉化為苯而除去,其原理如圖所示。下列敘述正確的是
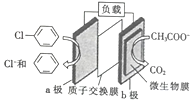
A. b極為正極,發生還原反應
B. 一段時間后b極區電解液的pH減小
C. H+由a極穿過質子交換膜到達b極
D. a極的電極反應式為![]() -e-=Cl-+
-e-=Cl-+![]()
查看答案和解析>>
科目: 來源: 題型:
【題目】在一恒容密閉容器中發生某化學反應2A(g)![]() B(g)+C(g),在三種不同條件下進行,其中實驗Ⅰ、Ⅱ都在800℃,實驗Ⅲ在850℃,B、C的初始濃度都為0,反應物A的濃度(mol·L-1)隨時間(min)的變化如圖的示:試回答下列問題:
B(g)+C(g),在三種不同條件下進行,其中實驗Ⅰ、Ⅱ都在800℃,實驗Ⅲ在850℃,B、C的初始濃度都為0,反應物A的濃度(mol·L-1)隨時間(min)的變化如圖的示:試回答下列問題:
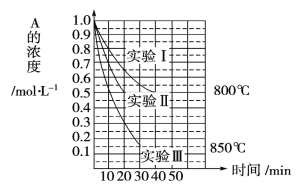
(1)在800℃時該反應的化學平衡常數K=_____。
(2)在實驗Ⅰ中,反應在20min至40min內A的化學反應速率為_________。
(3)實驗Ⅱ和實驗Ⅰ相比,可能隱含的反應條件是_____。
(4)根據實驗Ⅲ和實驗Ⅰ的比較,可推測該反應降低溫度,平衡向_____(填“正”或“逆”)反應方向移動,該正反應是__________(填“放熱”或“吸熱”)反應。
(5)與實驗Ⅰ相比,若實驗Ⅰ中的A的初始濃度改為0.8mol·L-1,其他條件不變,則達到平衡時所需用的時間_____實驗Ⅰ(填“等于”、“大于”或“小于”)。
查看答案和解析>>
科目: 來源: 題型:
【題目】如圖所示,甲池的總反應式為:N2H4+O2=N2+H2O,下列關于該電池工作時的說法正確的是( )

A. 該裝置工作時,Ag電極上有氣體生成
B. 甲池中負極反應為N2H4-4e-=N2+4H+
C. 甲池和乙池中的溶液的pH均減小
D. 當甲池中消耗0.1molN2H4時,乙池中理論上最多產生6.4g固體
查看答案和解析>>
科目: 來源: 題型:
【題目】CO2 與 H2 合成(CH3)2O(二甲醚)是煤化工中的重要反應,有關信息如下:2CO2(g)+6H2(g) ![]() (CH3)2O(g)+3H2O(g) ΔH<0 恒容下,該反應達平衡后,改變橫坐標表示的反應條件,下列示意圖正確的是( ) (K 表示該反應的平衡常數)
(CH3)2O(g)+3H2O(g) ΔH<0 恒容下,該反應達平衡后,改變橫坐標表示的反應條件,下列示意圖正確的是( ) (K 表示該反應的平衡常數)
A.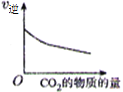 B.
B.
C.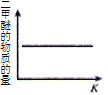 D.
D.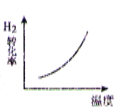
查看答案和解析>>
科目: 來源: 題型:
【題目】已知短周期元素的離子:aA2+、bB+、cC3-、dD-都具有相同的電子層結構,則下列敘述正確的是( )
A. 原子半徑:A>B>D>CB. 原子序數:d>c>b>a
C. 離子半徑:C>D>B>AD. 單質的還原性:A>B>D>C
查看答案和解析>>
科目: 來源: 題型:
【題目】一種可充電鋰-空氣電池如圖所示。當電池放電時,O2與Li+在多孔碳材料電極處生成Li2O2-x(x=0或1)。下列說法正確的是

A. 放電時,多孔碳材料電極為負極
B. 放電時,外電路電子由多孔碳材料電極流向鋰電極
C. 充電時,電解質溶液中Li+向多孔碳材料區遷移
D. 充電時,電池總反應為Li2O2-x=2Li+(1-![]() )O2
)O2
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com