
科目: 來源: 題型:
【題目】某溫度下,在2L密閉容器中投入一定量的A、B發生反應:3A(g) + bB (g) ![]() cC(g) ΔH=-Q kJ·mol-1(Q>0)。12s 時達到平衡,生成C的物質的量為0.8mol,反應過程如右圖所示。下列說法正確的是
cC(g) ΔH=-Q kJ·mol-1(Q>0)。12s 時達到平衡,生成C的物質的量為0.8mol,反應過程如右圖所示。下列說法正確的是

A.前12s內,A的平均反應速率為0.025mol·L-1·s-1
B.12s后,A的消耗速率等于B的生成速率
C.化學計量數之比b :c=1 :2
D.12s內,A和B反應放出的熱量為0.2Q kJ
查看答案和解析>>
科目: 來源: 題型:
【題目】某同學在實驗室探究NaHCO3的性質:常溫下,配制0.10 mol/ L NaHCO3溶液,測其pH為8.4;取少量該溶液滴加CaCl2溶液至pH=7,滴加過程中產生白色沉淀,但無氣體放出。下列說法不正確的是( )
A. NaHCO3溶液呈堿性的原因是HCO3-的水解程度大于電離程度
B. 反應的過程中產生的白色沉淀為CaCO3
C. 反應后的溶液中存在:c(Na+)+2c(Ca2+)=c(HCO3-)+2c(CO32-)+c(Cl-)
D. 加入CaCl2促進了HCO3-的水解
查看答案和解析>>
科目: 來源: 題型:
【題目】(1)肼(N2H4)又稱聯氨,在常溫下是一種可燃性的液體,可用作火箭燃料。已知在101 kPa時,1 g N2H4在氧氣中完全燃燒生成氮氣和H2O(l),放出19.5 kJ熱量(25 ℃時),表示N2H4燃燒的熱化學方程式是____________________________ 。
(2)在火箭推進器中裝有強還原劑肼(N2H4)和強氧化劑(H2O2),當它們混合時,即產生大量的N2和水蒸氣,并放出大量熱。已知0.4 mol液態肼和足量液態H2O2反應,生成氮氣和液態水,放出327.05 kJ的熱量。寫出該反應的熱化學方程式:__________________________________。
(3)已知拆開1 mol H—H鍵、1 mol N—H鍵、1 mol N≡N鍵分別需要的能量是436 kJ、391 kJ、946 kJ,則N2與H2反應生成NH3的熱化學方程式為_________________________________________________。
(4)下圖是一定量丙烷完全燃燒生成CO2 和1mol H2O (l)過程中的能量變化圖。

寫出表示丙烷燃燒熱的熱化學方程式:__________________________________。
查看答案和解析>>
科目: 來源: 題型:
【題目】金屬鋁分別和O2、O3發生反應生成Al2O3,反應過程和能量關系如圖所示(圖中的ΔH表示生成1mol生成物的數據)。下列有關說法中不正確的是( )

A.Al(s)與O3(g)反應生成Al2O3(s)的熱化學方程式為2Al(s)+O3(g)=Al2O3(s);ΔH= -1559.5kJ·mol-1
B.等質量的O2比O3的能量低
C.1mol O2完全轉化為O3,需吸收142kJ的熱量
D.給3O2(g)![]() 2O3(g)的平衡體系加熱,有利于O3的生成
2O3(g)的平衡體系加熱,有利于O3的生成
查看答案和解析>>
科目: 來源: 題型:
【題目】如圖所示,電流表指針發生偏轉,同時A極質量減少,B極上有氣泡產生,C為電解質溶液,

下列說法錯誤的是
A. B極為原電池的正極
B. A、B、C可能分別為Zn、Cu、稀鹽酸
C. C中陽離子向A極移動
D. A極發生氧化反應
查看答案和解析>>
科目: 來源: 題型:
【題目】下列表述中正確的是( )

A. 根據圖甲可知合成甲醇的熱化學方程式為CO(g)+2H2(g)=CH3OH(g) △H1=(b-a)kJ·mol-1
B. 圖乙表示2mol H2(g)所具有的能量比2mol氣態水所具有的能量多483.6kJ
C. 1mol NaOH分別和1mol CH3COOH、1mol HNO3反應,后者比前者△H小
D. 汽油燃燒時將全部的化學能轉化為熱能
查看答案和解析>>
科目: 來源: 題型:
【題目】銅鋅原電池工作時,下列敘述不正確的是
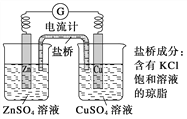
A. 負極反應為Zn-2e-===Zn2+
B. 電池反應為Zn+Cu2+===Zn2++Cu
C. 在外電路中,電子從銅電極流向鋅電極
D. 鹽橋中的K+移向CuSO4溶液
查看答案和解析>>
科目: 來源: 題型:
【題目】三硫化磷(P4S3)是黃綠色針狀晶體,易燃、有毒,分子結構之一如下圖所示,已知其燃燒熱ΔH=-3677 kJ/mol(P被氧化為P4O10),下列有關P4S3的說法不正確的是()

A. 分子中每個原子最外層均達到8電子穩定結構
B. P4S3中硫元素為-2價,磷元素為+3價
C. 一個P4S3分子中含有三個非極性共價鍵
D. 熱化學方程式為:P4S3(s)+8O2(g)=P4O10(s)+3SO2(g) ΔH=-3677 kJ/mol
查看答案和解析>>
科目: 來源: 題型:
【題目】甲醇是一種可再生能源,具有開發和應用的廣闊前景,工業上一般可采用如下反應來合成甲醇:![]()
![]()
(1)下表所列數據是該反應在不同溫度下的化學平衡常數![]()
溫度 | 250℃ | 300℃ | 350℃ |
K |
|
|
|
①該反應的平衡常數表達式![]() ______________,
______________,![]() __________
__________![]() 填“
填“![]() ”、“
”、“![]() ”或“
”或“![]() ”
”![]() 。
。
②某溫度下,將![]() 和
和![]() 充入2L的密閉容器中,充分反應10min后,達到平衡時測得
充入2L的密閉容器中,充分反應10min后,達到平衡時測得![]() ,則CO的轉化率為____________,此時的溫度為_________。
,則CO的轉化率為____________,此時的溫度為_________。
(2)向![]() 的
的![]() 溶液中加入
溶液中加入![]() 的鹽酸,生成沉淀。已知該溫度下AgCl的
的鹽酸,生成沉淀。已知該溫度下AgCl的![]() ,忽略溶液的體積變化,請計算:
,忽略溶液的體積變化,請計算:
①完全沉淀后,溶液中![]() ________。
________。
②完全沉淀后,溶液的![]() ________。
________。
查看答案和解析>>
科目: 來源: 題型:
【題目】某溫度下,向10 mL ![]() 溶液中滴加
溶液中滴加![]() 的
的![]() 溶液,滴加過程中,溶液中
溶液,滴加過程中,溶液中![]() 與
與![]() 溶液體積(V)的關系如圖所示,下列說法正確的是( )已知:
溶液體積(V)的關系如圖所示,下列說法正確的是( )已知: ![]() 。
。

A. 該溫度下 ![]()
B. X、Y、Z三點中,Y點水的電離程度最小
C. ![]() 溶液中:
溶液中:![]()
D. 向100 mL ![]() 濃度均為
濃度均為![]() 的混合溶液中逐滴加入
的混合溶液中逐滴加入![]() 的
的![]() 溶液,
溶液,![]() 先沉淀
先沉淀
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com