
科目: 來源: 題型:
【題目】工業上常用高濃度的K2CO3溶液吸收CO2,得溶液X,再利用電解法使K2CO3溶液再生,其裝置示意圖如下:
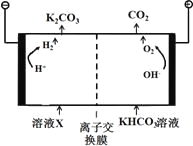
(1)在陽極區發生的反應包括_____________和H ++ HCO3-=H2O + CO2↑。
(2)簡述CO32-在陰極區再生的原理_______________
查看答案和解析>>
科目: 來源: 題型:
【題目】常溫下,向20 mL 0.1mol/L醋酸溶液中滴加0.1 mol/L的氫氧化鈉溶液,測定結果如下圖所示。下列解釋不正確的是

A. 0.1mol/L醋酸溶液pH約為3,說明醋酸是弱電解質
B. m大于20
C. a點表示的溶液中,c(CH3COO— )>c(Na+)
D. b點表示的溶液中,溶質為醋酸鈉和氫氧化鈉
查看答案和解析>>
科目: 來源: 題型:
【題目】常溫下,0.1mol·L-1的H2A溶液中各種微粒濃度的對數值(lgc)與pH的關系如圖所示。
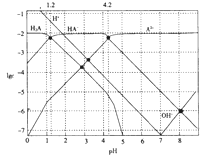
下列說法不正確的是
A. H2A是二元弱酸
B. HA-![]() H++A2-的電離平衡常數Ka=10-12
H++A2-的電離平衡常數Ka=10-12
C. 0.1mol·L-1的H2A溶液中:c(H+)=c(HA-)+2c(A2-)+c(OH-)
D. pH=4.2 時:c(HA-)=c(A2-)>c(H+)>c(H2A)>c(OH-)
查看答案和解析>>
科目: 來源: 題型:
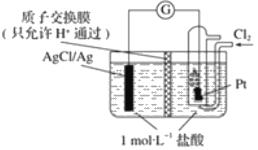
【題目】某原電池裝置如圖所示,電池總反應為 2Ag+Cl2═2AgCl。
(1)寫出該電池工作時的兩極反應:負極:___;正極:___。
(2)當電路中轉移amole﹣時,交換膜左側溶液中約減少___mol離子;交換膜右側溶液c(HCl)___(填“>”“<”或“=”)1molL-1(忽略溶液體積變化)。
查看答案和解析>>
科目: 來源: 題型:
【題目】按要求回答下列問題:
(1)在25℃、101Kpa下,1gCH3OH(l)燃燒生成CO2(g)和H2O(l)時放熱22.68kJ。則CH3OH燃燒的熱化學方程式為__________________。
(2)若以(1)中反應原理設計成甲醇燃料電池,電解質溶液為20%~30%的 KOH溶液,則該燃料電池的負極電極反應式為___________________。
(3)惰性電極電解400mL2mol/LCuSO4溶液,一段時間陰極增重1.28g (該極無氣體放出),電解后溶液體積不變,則溶液的pH 為_____,陽極可收集標況下氣體____mL。寫出電解的離子方程式:_____
(4)某溫度下,反應2NH3(g)![]() N2(g)+3H2(g)于恒容密閉容器中達到平衡狀態。(填“正向”、“逆向”或“不”)。若某時刻向該容器內通入一定量氨氣,則化學平衡________移動。若某時刻容器內所有物質的濃度均增加為原來的2倍,則化學平衡________移動。
N2(g)+3H2(g)于恒容密閉容器中達到平衡狀態。(填“正向”、“逆向”或“不”)。若某時刻向該容器內通入一定量氨氣,則化學平衡________移動。若某時刻容器內所有物質的濃度均增加為原來的2倍,則化學平衡________移動。
查看答案和解析>>
科目: 來源: 題型:
【題目】水溶液中的行為是中學化學的重要內容,按要求回答下列問題.
(1)在醋酸水溶液中存在平衡CH3COOH![]() CH3COO-+H+若分別改變下列條件:①加水稀釋②加熱③加少量固體醋酸鈉,其中能使醋酸電離程度增大的是_______,能使溶液pH增大的是_______(填序號)。
CH3COO-+H+若分別改變下列條件:①加水稀釋②加熱③加少量固體醋酸鈉,其中能使醋酸電離程度增大的是_______,能使溶液pH增大的是_______(填序號)。
(2)常溫下,0.1mol·L-1NaHCO3溶液的pH大于8,則溶液中Na+、HCO3-、CO32-、OH-四種微粒的濃度由大到小的順序為:________________________________。
(3)AlCl3溶液加熱蒸干并灼燒最終得到物質是________(填化學式),將NaHCO3與Al2(SO4)3溶液混合后可做泡沫滅火劑,其原理是_______(用離子方程式表示)。
(4)已知下列物質在20℃下的Ksp如下:
化學式 | AgCl | AgBr | AgI |
顏色 | 白色 | 淺黃色 | 黃色 |
Ksp | 2.0×10-10 | 5.4×10-13 | 8.3×10-17 |
①當向含相同濃度Cl-、Br-、I-的溶液中滴加AgNO3溶液時,_______先沉淀(填離子符號),
②向BaCl2溶液中加入AgNO3和KBr,當兩種淀共存時,  =__________。
=__________。
查看答案和解析>>
科目: 來源: 題型:
【題目】氫氧化鈰[Ce(OH)4]是一種重要的稀土氫氧化物。平板電視顯示屏生產過程中會產生大量的廢玻璃粉末(含SiO2、Fe2O3、CeO2),某課題組以此粉末為原料回收鈰,設計實驗流程如下:
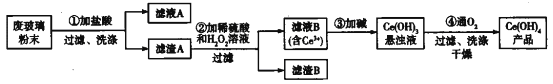
下列說法錯誤的是
A. 濾渣A中主要含有SiO2、CeO2
B. 過濾操作中用到的玻璃儀器有燒杯、漏斗、玻璃棒
C. 過程②中發生反應的離子方程式為CeO2+H2O2+3H+=Ce3++2H2O+O2↑
D. 過程④中消耗 11.2L O2(已折合成標準狀況),轉移電子數為2×6.02×1023
查看答案和解析>>
科目: 來源: 題型:
【題目】一定條件下,在水溶液中1 mol Cl-、ClOx- (x=1,2,3,4)的能量(kJ)相對大小如圖所示。下列有關說法正確的是 ( )
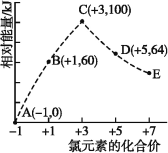
A.這些離子中結合H+能力最強的是A
B.A、B、C、D、E五種微粒中C最穩定
C.C→B+D的反應,反應物的總鍵能小于生成物的總鍵能
D.B→A+D反應的熱化學方程式為3ClO-(aq)=ClO3- (aq)+2Cl-(aq) ΔH=+116 kJ·mol-1
查看答案和解析>>
科目: 來源: 題型:
【題目】常溫下,現有![]() 的
的![]() 溶液,
溶液,![]() 已知含氮
已知含氮![]() 或含碳
或含碳![]() 各微粒的分布分數
各微粒的分布分數![]() 平衡時某種微粒的濃度占各種微粒濃度之和的分數
平衡時某種微粒的濃度占各種微粒濃度之和的分數![]() 與pH的關系如圖所示.下列說法正確的是
與pH的關系如圖所示.下列說法正確的是![]()
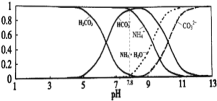
A.當溶液的![]() 時,溶液中存在下列關系:
時,溶液中存在下列關系:![]()
B.![]() 溶液中存在下列守恒關系:
溶液中存在下列守恒關系:![]()
C.往該溶液中逐滴滴加氫氧化鈉時![]() 和
和![]() 濃度逐漸減小
濃度逐漸減小
D.通過分析可知常溫下![]()
查看答案和解析>>
科目: 來源: 題型:
【題目】K2Cr2O7溶液中存在平衡:Cr2O72-(橙色)+H2O2CrO42-(黃色)+2H+。用K2Cr2O7溶液進行下列實驗:
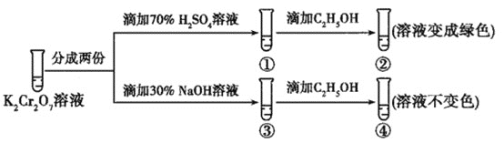
結合實驗,下列說法不正確的是( )
A.①中溶液橙色加深,③中溶液變黃
B.②中Cr2O72-被C2H5OH還原
C.對比②和④可知K2Cr2O7酸性溶液氧化性強
D.若向④中加入70%H2SO4溶液至過量,溶液變為橙色
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com