
科目: 來源: 題型:選擇題
 臭氧是理想的煙氣脫硝劑,其脫硝反應為:2NO2(g)+O3(g)?N2O5(g)+O2(g)△H.不同溫度下,在三個容器中發生上述反應,相關信息如下表及圖所示,下列說法正確的是( )
臭氧是理想的煙氣脫硝劑,其脫硝反應為:2NO2(g)+O3(g)?N2O5(g)+O2(g)△H.不同溫度下,在三個容器中發生上述反應,相關信息如下表及圖所示,下列說法正確的是( )| 容器 | 甲 | 乙 | 丙 |
| 容積/L | 1 | 1 | 2 |
| 反應物起始量 | 2mol NO2,1mol O3 | 2mol NO2,1mol O3 | 2mol NO2,1mol O3 |
| 溫度 | T1 | T2 | T2 |
| A. | 0~10min內甲容器中反應的平均速率:v(NO2)=0.02mol•L-1•min-1 | |
| B. | T1<T2,△H>0 | |
| C. | 平衡時N2O5濃度:c乙(N2O5)>c丙(N2O5) | |
| D. | T1℃時,若起始時間向容器甲中充入2molNO2、1molO3、2molN2O5和2mol O2,則脫硝反應達到平衡前,v(正)<c(逆) |
查看答案和解析>>
科目: 來源: 題型:解答題
 苯乙烯(
苯乙烯(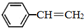 )是生產各種塑料的重要單體,可通過乙苯催化脫氫制得:
)是生產各種塑料的重要單體,可通過乙苯催化脫氫制得: CH2CH3(g)$\stackrel{催化劑}{?}$
CH2CH3(g)$\stackrel{催化劑}{?}$ =CH2(g)+H2(g)△=-Q1kJ.mol-1
=CH2(g)+H2(g)△=-Q1kJ.mol-1 .
.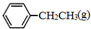 、
、 、H2(g)的燃燒熱(△H)分別為-Q1 kJ•mol-1、-Q2kJ•mol-1、-Q3 kJ•mol-1,寫出Q與Q1、Q2、Q3的關系式Q2+Q3-Q1.
、H2(g)的燃燒熱(△H)分別為-Q1 kJ•mol-1、-Q2kJ•mol-1、-Q3 kJ•mol-1,寫出Q與Q1、Q2、Q3的關系式Q2+Q3-Q1.查看答案和解析>>
科目: 來源: 題型:解答題

查看答案和解析>>
科目: 來源: 題型:解答題
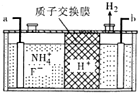 氮、磷及其化合物在生產、生活中有重要的用途.回答下列問題:
氮、磷及其化合物在生產、生活中有重要的用途.回答下列問題:查看答案和解析>>
科目: 來源: 題型:解答題
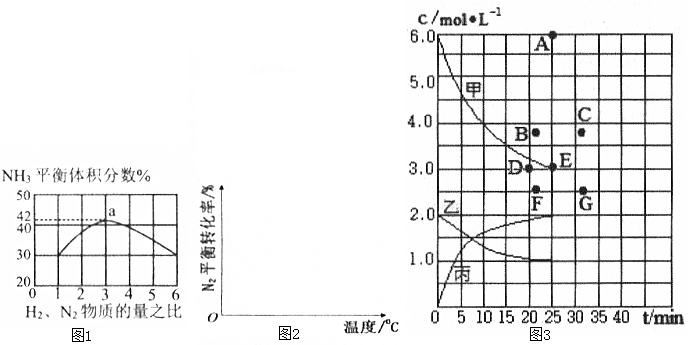

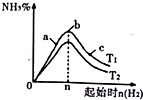
| t/min | 0 | 5 | 10 | 15 | 20 | 25 | 30 |
| N(H2)/mol | 6.00 | 4.50 | 3.60 | 3.30 | 3.03 | 3.00 | 3.00 |
| N(NH3)/mol | 0 | 1.00 | 1.60 | 1.80 | 1.98 | 2.00 | 2.00 |
查看答案和解析>>
科目: 來源: 題型:多選題
| A. | 常溫下,向含有AgCl固體的飽和溶液,加少量水稀釋,c(Ag+)和Ksp(AgCl)均保持不變 | |
| B. | pH=5的CH3COOH與CH3COONa的混合溶液中:c(Na+)>c(CH3COO-) | |
| C. | 將0.2mol/LCH3COOH溶液和0.1mol/LNaOH溶液等體積混合,則反應后的混合溶液中:2c(OH-)+c(CH3COO-)=2c(H+)+c(CH3COOH) | |
| D. | 將水加熱煮沸,能促進水的電離,Kw增大,pH增大,溶液呈堿性 |
查看答案和解析>>
科目: 來源: 題型:選擇題
 一定溫度下,在三個容積均為2.0L的恒容密閉容器中發生反應:
一定溫度下,在三個容積均為2.0L的恒容密閉容器中發生反應:| 容器 | 溫度/℃ | 起始物質的量/mol | |
| NO(g) | CO(g) | ||
| 甲 | T1 | 0.20 | 0.20 |
| 乙 | T1 | 0.30 | 0.30 |
| 丙 | T2 | 0.20 | 0.20 |
| A. | 該反應的正反應為吸熱反應 | |
| B. | 達到平衡時,乙中CO2的體積分數比甲中的小 | |
| C. | T1℃時,若起始時向甲中充入0.40molNO、0.40molCO、0.40molN2和0.40molCO2,則反應達到新平衡前v(正)<v(逆) | |
| D. | T2℃時,若起始時向丙中充入0.06molN2和0.12molCO2,則達平衡時N2的轉化率大于40% |
查看答案和解析>>
科目: 來源: 題型:解答題
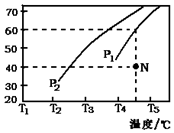
| CO濃度(mol•L-1) | H2濃度(mol•L-1) | 逆反應速率(mol•L-1•min-1) |
| 0.1 | c1 | 9.6 |
| c2 | c1 | 19.2 |
| c2 | 0.3 | 64.8 |
查看答案和解析>>
科目: 來源: 題型:解答題
查看答案和解析>>
科目: 來源: 題型:解答題

查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com