
科目: 來源: 題型:選擇題
| A. | PH=10的Mg(OH)2濁液C(Mg2+)=10-8 mol•L-1 (已知Mg(OH)2KSP=1×10-16) | |
| B. | 已知AgClKSP=1.8×10-10;Ag2CrO4KSP=1.2×10-12則AgCl的溶解度一定比Ag2CrO4大 | |
| C. | 在飽和AgCl溶液中加入NaI固體不會發生變化 | |
| D. | Fe3+在酸性溶液中一定不會生成Fe(OH)3沉淀 |
查看答案和解析>>
科目: 來源: 題型:解答題
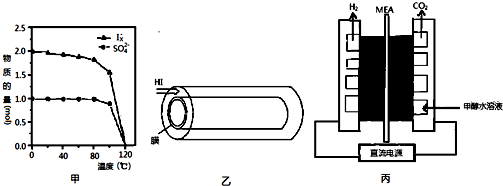
查看答案和解析>>
科目: 來源: 題型:選擇題
| 0min | 5min | 10min | |
| CO | 0.01 | 0.0056 | |
| H2O | 0.01 | 0.0156 | |
| CO2 | 0 | 0.0044 | |
| H2 | 0 | 0.0044 |
| A. | 0~5min 時用H2O(g)表示的平均反應速率為1.2×10-3 mol/( L.min) | |
| B. | 5min~10min 改變的條件是再加入了0.1mol H2O(g) | |
| C. | 200℃時,若向容器中充入0.01mol CO(g)、0.01mol H2O(g)、0.01molCO2(g)、0.01molH2(g),達平衡時,CO(g)為1.2×10-3mol/L | |
| D. | 300℃時,若向容器中充入0.01mol CO(g)、0.01mol H2O(g)、0.02molCO2(g)、0.02molH2(g),則開始反應時ν(正)<ν(逆) |
查看答案和解析>>
科目: 來源: 題型:解答題
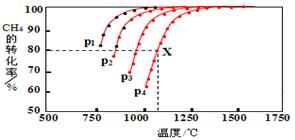 能源、環境與生產生活和社會發展密切相關.
能源、環境與生產生活和社會發展密切相關.| 容 器 | 甲 | 乙 |
| 反應物投入量 | 1molCO 2(g)和3molH2(g) | 1molCH3OH(g)和1molH2O(g) |
| 平衡時c(CH3OH) | c1 | c2 |
| 平衡時能量變化 | 放出29.4kJ | 吸收akJ |
查看答案和解析>>
科目: 來源: 題型:解答題
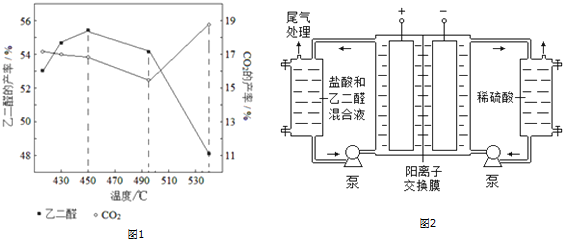
查看答案和解析>>
科目: 來源: 題型:選擇題
| A. | AgCl、Ag2C2O4、AgI三者的飽和溶液中c(Ag+)大小順序:Ag2C2O4>AgCl>AgI | |
| B. | 將0.02 mol•L-1AgNO3溶液和0.02 mol•L-1 Na2SO4溶液等體積混合,有沉淀生成 | |
| C. | 向5mL飽和AgCl溶液中滴加0.5mL 0.1 mol•L-1KI溶液,無沉淀生成 | |
| D. | 向濃度均為0.1mol•L-1NaCl和KI混合溶液中滴加AgNO3溶液,先有白色沉淀生成 |
查看答案和解析>>
科目: 來源: 題型:選擇題
| t/min | 平衡時的熱量變化 | |||||||
| 0 | 20 | 40 | 60 | 80 | 120 | |||
| 第一組 | X(HI) | 0 | 0.60 | 0.73 | 0.773 | 0.780 | 0.784 | 放出Q1kJ |
| 第二組 | X(HI) | 1 | 0.91 | 0.85 | 0.815 | 0.795 | 0.784 | 吸收Q2kJ |
| A. | Q1+Q2=11a(a>0) | |
| B. | k正=K•k逆(K為已知反應的平衡常數,下同) | |
| C. | K=$\frac{0.21{6}^{2}}{0.10{8}^{2}}$ | |
| D. | 相同溫度下,在第二組平衡后的混合氣體中再加入2molHI,重新達到平衡后,HI的轉化率為21.6% |
查看答案和解析>>
科目: 來源: 題型:解答題
 (1)同一物質存在氣態的熵值最大,液態的熵值次之,固態的熵值最小.若同溫同壓下,一個反應生成物氣體的體積等于反應物氣體的體積就可粗略認為該反應的熵變為0.某化學興趣小組,專門研究了氧族元素及其某些化學物的部分性質.所查資料如下:
(1)同一物質存在氣態的熵值最大,液態的熵值次之,固態的熵值最小.若同溫同壓下,一個反應生成物氣體的體積等于反應物氣體的體積就可粗略認為該反應的熵變為0.某化學興趣小組,專門研究了氧族元素及其某些化學物的部分性質.所查資料如下:查看答案和解析>>
科目: 來源: 題型:選擇題
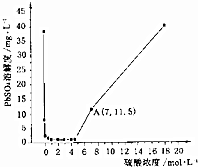 已知25℃時KSP(PbSO4)=1.6×10-8、KSP(BaSO4)=1.1×10-10,該溫度下PbSO4在不同濃度的硫酸中的溶解度如圖所示.下列有關說法不正確的是( )
已知25℃時KSP(PbSO4)=1.6×10-8、KSP(BaSO4)=1.1×10-10,該溫度下PbSO4在不同濃度的硫酸中的溶解度如圖所示.下列有關說法不正確的是( )| A. | 圖中A點c(SO42-)=7mol•L-1 | |
| B. | 過濾的PbSO4沉淀,用稀硫酸洗滌,可以減少沉淀損耗 | |
| C. | 硫酸濃度大于5mol•L-1時,PbSO4溶解度增大的原因是轉化成Pb(HSO4)2 | |
| D. | 將Pb(NO3)2、Ba(NO3)2混合溶液滴入稀硫酸中,能生成PbSO4和BaSO4兩種沉淀 |
查看答案和解析>>
科目: 來源: 題型:解答題
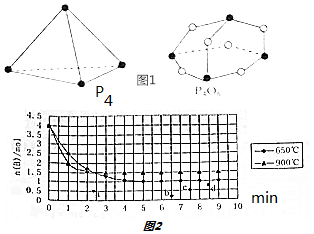
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com