
科目: 來源: 題型:解答題
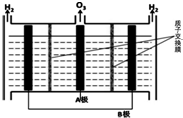 NO能引起光化學煙霧,破壞臭氧層.處理NO有多種方法,根據題意回答下列問題:
NO能引起光化學煙霧,破壞臭氧層.處理NO有多種方法,根據題意回答下列問題:| 時間(s) | 0 | 1 | 2 | 3 | 4 | … |
| c(NO)/mol•L-1 | 1.00×10-3 | 4.00×10-4 | 1.70×10-4 | 1.00×10-4 | 1.00×10-4 | … |
查看答案和解析>>
科目: 來源: 題型:解答題
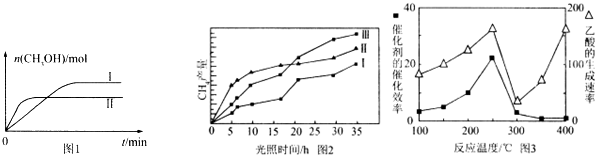 CO2(g)+3H2(g)?CH3OH(g)+H2O(g),測得CH3OH的物質的量隨時間的變化見圖1.
CO2(g)+3H2(g)?CH3OH(g)+H2O(g),測得CH3OH的物質的量隨時間的變化見圖1.| 容 器 | 甲 | 乙 |
| 反應物投入量 | 1mol CO2、3mol H2 | a mol CO2、b mol H2、 c mol CH3OH(g)、c mol H2O(g) |
查看答案和解析>>
科目: 來源: 題型:解答題
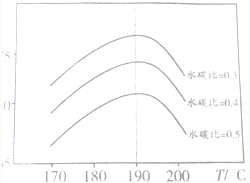 CO2和CH4均為溫室氣體,研究它們具有重要的意義.
CO2和CH4均為溫室氣體,研究它們具有重要的意義.| 時間/min | 0 | 10 | 20 | 30 | 40 | 50 | 65 | 80 | 100 |
| 總壓強p/100kPa | 9.53 | 7.85 | 6.37 | 5.78 | 5.24 | 4.93 | 4.67 | 4.45 | 4.45 |
查看答案和解析>>
科目: 來源: 題型:解答題
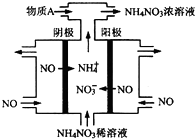 氮可形成多種氧化物,如NO、NO2、N2O4等.
氮可形成多種氧化物,如NO、NO2、N2O4等.| 時間/s | 0 | 20 | 40 | 60 | 80 |
| n(NO2)/mol | 0.40 | n1 | 0.26 | n3 | n4 |
| n(N2O4)/mol | 0.00 | 0.05 | n2 | 0.08 | 0.08 |
查看答案和解析>>
科目: 來源: 題型:解答題
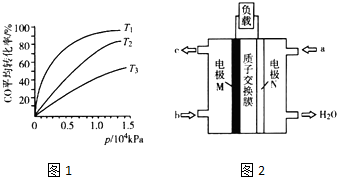
| 容器換號 | 溫度(℃) | 起始物質的量(mol) | 平衡物質的量(mol) | |
| CH3OH(g) | CH3OCH2(g) | H2O(g) | ||
| Ⅰ | 387 | 0.20 | 0.080 | 0.080 |
| Ⅱ | 207 | 0.20 | 0.090 | 0.090 |
查看答案和解析>>
科目: 來源: 題型:解答題
| 化學反應 | 反應熱 | 平衡常數(850℃) |
| ①CO (g)+2H2 (g)═CH3 OH(g) | △H1=-90.8kj/mol | k1=160(mol/L)-2 |
| ②CO2 (g)+H2 (g)═CO (g)+H2 O(g) | △H2=-41.2kj/mol | K2 |
| ③3H2 (g)+CO2 (g)═H2 O(g)+CH3 OH(g)△H 3 | △H3 | K3=160(mol/L)-2 |
| 物質 | H2 | CO2 | CH3OH | H2O |
| 濃度(mol/L) | 0.2 | 0.2 | 0.4 | 0.4 |
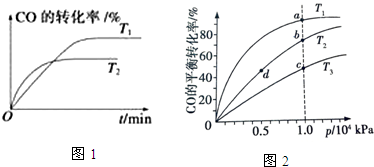
查看答案和解析>>
科目: 來源: 題型:選擇題
| A. | 0.2mol•L-1 | B. | 0.15mol•L-1 | C. | 0.04mol•L-1 | D. | 0.4mol•L-1 |
查看答案和解析>>
科目: 來源: 題型:選擇題
| A. | 10.7 | B. | 8.5 | C. | 32 | D. | 64 |
查看答案和解析>>
科目: 來源: 題型:解答題
 A、B、C、D、E、F、G、H為八種相鄰的短周期元素,其單質的沸點如圖所示.
A、B、C、D、E、F、G、H為八種相鄰的短周期元素,其單質的沸點如圖所示.查看答案和解析>>
科目: 來源: 題型:選擇題
| A. | Fe2(SO4)3和 Ba(OH)2溶液反應的離子方程式:Fe3++SO42-+Ba2++3OH-═Fe(OH)3↓+BaSO4↓ | |
| B. | 碳酸鋇加入稀硫酸:BaCO3+2H+═Ba2++H2O+CO2↑ | |
| C. | 向碳酸氫鈣溶液中加入過量氫氧化鈉:Ca2++2HCO3-+2OH-═CaCO3↓+2H2O+CO32- | |
| D. | 等物質的量的MgCl2、Ba(OH)2和 HC1溶液混合:Mg2++2OH-═Mg(OH)2↓ |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com