
科目: 來源: 題型:解答題
| 序號 | A溶液 | B溶液 |
| ① | 2mL 0.2mol/L H2C2O4溶液 | 4mL 0.01mol/L KMnO4溶液 |
| ② | 2mL 0.1mol/L H2C2O4溶液 | 4mL 0.01mol/L KMnO4溶液 |
| ③ | 2mL 0.2mol/L H2C2O4溶液 | 4mL 0.01mol/L KMnO4溶液和少量MnSO4 |
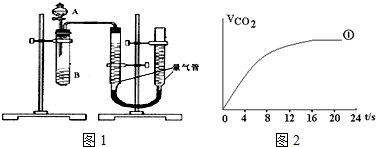
| 實驗編號 | 1 | 2 | 3 | 4 |
| 水/mL | 10 | 5 | 0 | X |
| 0.5mol/L H2C2O4/mL | 5 | 10 | 10 | 5 |
| 0.2mol/L KMnO4/mL | 5 | 5 | 10 | 10 |
| 時間/s | 40 | 20 | 10 | --- |
| 時間/s | 0 | 5 | 10 | 15 | 20 | 25 | 30 |
| 溫度/℃ | 25 | 26 | 26 | 26 | 26.5 | 27 | 27 |
查看答案和解析>>
科目: 來源: 題型:選擇題
| A. | 7 種 | B. | 6 種 | C. | 5 種 | D. | 4 種 |
查看答案和解析>>
科目: 來源: 題型:解答題
| 序號 | 硫酸的體積/mL | 鋅的質量/g | 鋅的形狀 | 溫度/℃ | 完全溶于酸的時間/s | 生成硫酸鋅的質量/g |
| ① | 50.0 | 2.0 | 薄片 | 15 | 200 | m1 |
| ② | 50.0 | 2.0 | 薄片 | 25 | 100 | m2 |
| ③ | 50.0 | 2.0 | 顆粒 | 25 | 70 | m3 |
| ④ | 50.0 | 2.0 | 顆粒 | 35 | 35 | m4 |
| ⑤ | 50.0 | 2.0 | 粉末 | 25 | t1 | 5.0 |
| ⑥ | 50.0 | 4.0 | 粉末 | 25 | t2 | m5 |
| ⑦ | 50.0 | 6.0 | 粉末 | 25 | t3 | 14.9 |
| ⑧ | 50.0 | 8.0 | 粉末 | 25 | t4 | 19.3 |
| ⑨ | 50.0 | 10.0 | 粉末 | 25 | t5 | m6 |
| ⑩ | 50.0 | 12.0 | 粉末 | 25 | t6 | 19.3 |
查看答案和解析>>
科目: 來源: 題型:解答題
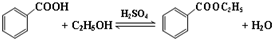
| 沸點(℃) | 密度(g•cm-3) | |
| 苯甲酸 | 249 | 1.2659 |
| 苯甲酸乙酯 | 212.6 | 1.05 |
| 乙醇 | 78.5 | 0.7893 |
| 環己烷 | 80.8 | 0.7785 |
| 乙醚 | 34.51 | 0.7318 |
| 環己烷、乙醇和水共沸物 | 62.1 |

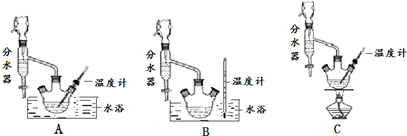
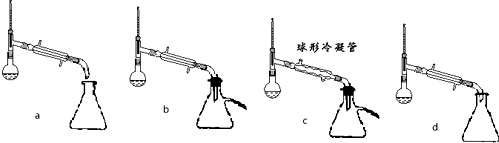
查看答案和解析>>
科目: 來源: 題型:解答題
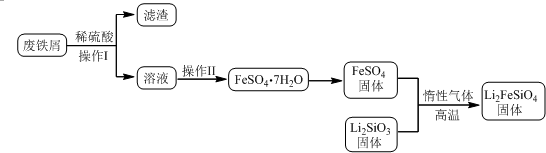
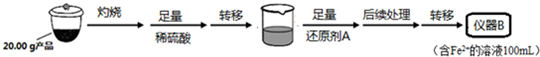
| 實驗序號 | 1 | 2 | 3 | 4 |
| 消耗KMnO4溶液體積 | 20.00mL | 19.98mL | 21.38mL | 20.02mL |
查看答案和解析>>
科目: 來源: 題型:解答題
| 序號 | 反應溫度/℃ | c(H2O2)/mol•L-1 | V(H2O2)/mL | m(MnO2)/g | t/min |
| 1 | 20 | 2 | 10 | 0 | t1 |
| 2 | 20 | 2 | 10 | 0.1 | t2 |
| 3 | 20 | 4 | 10 | 0.1 | t3 |
| 4 | 40 | 2 | 10 | 0.1 | t4 |
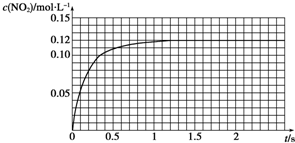
查看答案和解析>>
科目: 來源: 題型:解答題
 溴苯是一種化工原料,實驗室合成溴苯的裝置示意圖及有關數據如下:
溴苯是一種化工原料,實驗室合成溴苯的裝置示意圖及有關數據如下:| 苯 | 溴 | 溴苯 | |
| 密度/g•cm-3 | 0.88 | 3.10 | 1.50 |
| 沸點/℃ | 80 | 59 | 156 |
| 水中溶解度 | 微溶 | 微溶 | 微溶 |
 +Br2$\stackrel{Fe}{→}$
+Br2$\stackrel{Fe}{→}$ +HBr.
+HBr.查看答案和解析>>
科目: 來源: 題型:解答題


查看答案和解析>>
科目: 來源: 題型:選擇題
| A. | D的濃度減小了 | B. | A的轉化率減小了 | ||
| C. | 物質B的質量分數增加了 | D. | a+b>c+d |
查看答案和解析>>
科目: 來源: 題型:選擇題
| A. | 相同條件下,平衡時若充入稀有氣體,SO2的轉化率增大 | |
| B. | 0~6 min的平衡反應速率:v(O2)=0.105 mol/(L•min) | |
| C. | 保持其他條件不變,僅降低溫度,正反應速率減小程度比逆反應速率減小程度大 | |
| D. | 反應開始時,向容器中通入的SO2的物質的量是1.4 mol |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com