
科目: 來源:2015-2016學年江蘇省揚州市高二選修下學期期末調研化學試卷(解析版) 題型:填空題
科學研究與工業生產中常常用到溶液中的反應。
(1)25℃時,0.05 mol·L-1Ba(OH)2溶液的pH= ,將該Ba(OH)2溶液與pH=2的HCl溶液混合,若所得混合溶液pH=7,則Ba(OH)2溶液與HCl溶液的體積比為 。
(2)CO2可轉化成有機物實現碳循環:CO2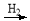 CH3OH
CH3OH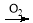 HCOOH……
HCOOH……
25 ℃時,幾種酸的電離平衡常數如下:
化學式 | HCOOH | H2CO3 | HClO |
電離平衡常數 | 1.7×10-4 | K1=4.3×10-7 K2=5.6×10-11 | 3.0×10-8 |
回答下列問題:
①用離子方程式表示HCOONa溶液呈堿性的原因 。
②物質的量濃度均為0.1 mol·L-1的下列四種物質:
a.Na2CO3 b.NaClO c.HCOONa d.NaHCO3 ,pH由大到小的順序是 (填編號)。
(3)常溫下,將0.2 mol·L-1的HCOOH和0.1 mol·L-1的NaOH溶液等體積混合,所得溶液的pH<7,說明所得混合溶液中HCOOH的電離程度 HCOONa的水解程度(填“大于”“等于”或“小于”)。
(4)含有Cr2O72-的廢水毒性較大,某工廠廢水中含5.00×10-3 mol·L-1的Cr2O72-。為使廢水能達標排放,做如下處理:Cr2O72-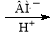 Cr3+、Fe3+
Cr3+、Fe3+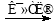 Cr(OH)3、Fe(OH)3。若處理后的廢水中殘留的c(Fe3+)=2×10-13 mol·L-1,則殘留的Cr3+的濃度為 mol·L-1 (已知:Ksp[Fe(OH)3]=4.0×10-38,Ksp[Cr(OH)3]=6.0×10-31)。
Cr(OH)3、Fe(OH)3。若處理后的廢水中殘留的c(Fe3+)=2×10-13 mol·L-1,則殘留的Cr3+的濃度為 mol·L-1 (已知:Ksp[Fe(OH)3]=4.0×10-38,Ksp[Cr(OH)3]=6.0×10-31)。
查看答案和解析>>
科目: 來源:2015-2016學年江蘇省揚州市高二選修下學期期末調研化學試卷(解析版) 題型:填空題
廢棄物的綜合利用既有利于節約資源,又有利于保護環境。實驗室利用廢棄舊電池的銅帽(Zn、Cu總含量約為99%)回收銅并制備ZnO的部分實驗過程如下:

(1)①寫出銅帽溶解過程中發生反應的化學方程式 。
②銅帽溶解后需將溶液中過量H2O2除去。除去H2O2的簡便方法是 。
(2)為確定加入鋅灰(主要成分為Zn、ZnO,雜質為鐵及其氧化物)含量,實驗中需測定除去H2O2后溶液中Cu2+的含量。實驗操作為:準確量取一定體積的含有Cu2+的溶液于帶塞錐形瓶中,加適量水稀釋,調節pH=3~4,加入過量KI,用Na2S2O3標準溶液滴定至終點。上述過程中的離子方程式如下:
2Cu2++4I-=2CuI(白色)↓+I2 I2+2 =2I-+
=2I-+
①滴定選用的指示劑為 ,滴定終點觀察到的現象為 。
②若滴定前溶液中H2O2沒有除盡,所測得的Cu2+的含量將會 (填“偏高”、“偏低”、“不變”)。
(3)已知pH>11時Zn(OH)2能溶于NaOH溶液生成[Zn(OH)4]2-。下表列出了幾種離子生成氫氧化物沉淀的pH(開始沉淀的pH按金屬離子濃度為1.0 mol·L-1計算)
Fe3+ | Fe2+ | Zn2+ | |
開始沉淀的pH | 1.1 | 5.8 | 5.9 |
完全沉淀的pH | 3.2 | 8.8 | 8.9 |
實驗中可選用的試劑:30% H2O2、1.0 mol·L-1HNO3、1.0 mol·L-1 NaOH。
由回收銅后的濾液制備ZnO的實驗步驟依次為:
① ;
② ;
③ 過濾;
④ ;
⑤ 過濾、洗滌、干燥
⑥ 900℃煅燒。
查看答案和解析>>
科目: 來源:2015-2016學年江蘇省揚州市高二選修下學期期末調研化學試卷(解析版) 題型:填空題
NH3是一種重要的化工原料,也是造成水體富營養化及氮氧化物污染的重要因素之一。
(1)N2和H2以物質的量之比為1∶3在不同溫度和壓強下發生反應:N2+3H2 2NH3,測得平衡體系中NH3的物質的量分數如圖1。
2NH3,測得平衡體系中NH3的物質的量分數如圖1。

①為提高原料氣的轉化率,工業上采取的合理措施有 (填字母)。
a. 采用常溫條件
b. 使用適當的催化劑
c. 將原料氣加壓
d. 將氨液化并不斷移出
②圖1中所示的平衡體系中NH3的物質的量分數為0.549和0.488時,該反應的平衡常數分別為K1、K2,則K1 K2。(填“>”“<”或“=”)
(2)氨氮是造成水體富營養化的重要因素之一,用次氯酸鈉水解生成的次氯酸將水中的氨氮(用NH3表示)轉化為氮氣除去,涉及的相關反應如下:
反應①:NH3+HClO===NH2Cl+H2O
反應②:NH2Cl+HClO===NHCl2+H2O
反應③:2NHCl2+H2O===N2+HClO+3HCl
已知在水溶液中NH2Cl較穩定,NHCl2不穩定易轉化為氮氣。在其他條件一定的情況下,改變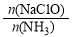 (即NaClO溶液的投入量),溶液中次氯酸鈉對氨氮去除率及余氯量 (溶液中+1價氯元素的含量)的影響如圖2所示。
(即NaClO溶液的投入量),溶液中次氯酸鈉對氨氮去除率及余氯量 (溶液中+1價氯元素的含量)的影響如圖2所示。
①反應中氨氮去除效果最佳的n(NaClO)/n(NH3)值約為 。
②a點之前氨氮去除率較低的原因為 。
(3)電解硝酸工業的尾氣NO可制備NH4NO3,其工作原理如圖3。
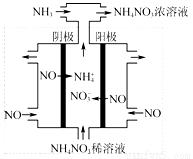
①電解過程(虛線內)發生反應的離子方程式為 。
②將電解生成的HNO3全部轉化為NH4NO3,則通入的NH3與實際參加反應的NO的物質的量之比至少為 。
查看答案和解析>>
科目: 來源:2015-2016學年江蘇省揚州市高二選修下學期期末調研化學試卷(解析版) 題型:填空題
數十年來,化學工作者對碳的氧化物做了廣泛深入的研究并取得了一些重要成果。在高溫高壓下CO具有極高的化學活性,能與多種單質或化合物反應。
(1)工業上常采用水蒸氣噴到灼熱的炭層上實現煤的氣化(制得CO、H2),該反應的化學方程式是 。
(2)上述煤氣化過程中需向炭層交替噴入空氣和水蒸氣,噴入空氣的目的是 ;反應生成的氣體在加熱、催化劑作用條件下可合成液體燃料甲醇,該反應的化學方程式為 。
(3)一定條件下,CO與H2可合成甲烷,反應方程式為:CO(g)+3H2(g) CH4(g)+H2O (g)該條件下,該反應能夠自發進行的原因是 。
CH4(g)+H2O (g)該條件下,該反應能夠自發進行的原因是 。
(4)CO—空氣燃料電池中使用的電解質是攙雜了Y2O3的ZrO2晶體,它在高溫下能傳導O2-。該電池正極的電極反應式為 。
(5)工業上可通過甲醇羰基化法制取甲酸甲酯,反應方程式為:
CH3OH(g)+CO(g) HCOOCH3(g) ΔH =-29.1 kJ·mol-1
HCOOCH3(g) ΔH =-29.1 kJ·mol-1
科研人員對該反應進行了研究,部分研究結果如下:

①根據反應體系的壓強對甲醇轉化率的影響并綜合考慮生產成本因素,工業制取甲酸甲酯應選擇的壓強為 。
a.3.5×106Pa b.4.0×106Pa c.5.0×106Pa
②實際工業生產中采用的溫度是 ,其理由是 。
查看答案和解析>>
科目: 來源:2015-2016學年江蘇省揚州市高二選修下學期期末調研化學試卷(解析版) 題型:填空題
將過量的氨水加到硫酸銅溶液中,溶液最終變成深藍色,繼續加入乙醇,析出晶體Cu(NH3)4SO4·H2O。
(1)Cu2+基態核外電子排布式為 ;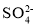 的空間構型為 。(用文字描述)
的空間構型為 。(用文字描述)
(2)乙醇分子中氧原子軌道雜化類型為 。與NH3互為等電子體的一種陽離子為 (填化學式)。
(3)1mol[Cu(NH3)4]2+中σ鍵的數目為 。
(4)某含有結晶水的銅的氯化物的晶胞結構如圖所示,該化合物的化學式是 。
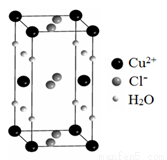
查看答案和解析>>
科目: 來源:2015-2016學年江西省高二下學期期末考試化學試卷(解析版) 題型:選擇題
人們一向把碳的氧化物、碳酸鹽看作無機物的原因是( )
A.都是碳的簡單化合物
B.不是從生命體中取得
C.不是共價化合物
D.不具備有機物典型的性質和特點
查看答案和解析>>
科目: 來源:2015-2016學年江西省高二下學期期末考試化學試卷(解析版) 題型:選擇題
有機物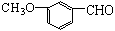 ,有多種同分異構體,其中屬于酯且含有苯環結構的共有( )
,有多種同分異構體,其中屬于酯且含有苯環結構的共有( )
A.3種 B.4種 C.5種 D.6種
查看答案和解析>>
科目: 來源:2015-2016學年江西省高二下學期期末考試化學試卷(解析版) 題型:選擇題
現有四組混合物:①乙酸乙酯和乙酸鈉溶液 ②乙醇和甘油 ③溴化鈉和單質溴的水溶液 ④碘和四氯化碳的混合物,分離以上各混合物的正確方法依次是( )
A. 分液、萃取、蒸餾、萃取 B. 萃取、蒸餾、分液、萃取
C. 分液、蒸餾、萃取、蒸餾 D. 蒸餾、萃取、分液、萃取
查看答案和解析>>
科目: 來源:2015-2016學年江西省高二下學期期末考試化學試卷(解析版) 題型:選擇題
能與NaOH溶液,新制Cu(OH)2懸濁液、純堿溶液、溴水、苯酚鈉、甲醇都起反應的是( )
A.CH3COOH B.CH2=CHCOOH C.鹽酸 D.乙酸甲酯
查看答案和解析>>
科目: 來源:2015-2016學年江西省高二下學期期末考試化學試卷(解析版) 題型:選擇題
①殘留在試管內壁上的碘,用酒精洗滌
②盛放過苯酚的試劑瓶中殘留的苯酚,用酒精洗滌
③做銀鏡反應后殘留的銀,用稀氨水洗滌
④沾附在試管內壁上的油脂,用熱堿液洗滌
A. ①②④ B. ②③④ C. ①③④ D. ①②③④
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com