
【題目】已知下列熱化學方程式:
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
回答下列問題:
(1).上述反應中屬于放熱反應的是________。
(2).H2的燃燒熱![]() ________________;C的燃燒熱
________________;C的燃燒熱![]() ________________。
________________。
(3).燃燒![]() 生成液態水,放出的熱量為________。
生成液態水,放出的熱量為________。
(4).寫出CO燃燒的熱化學方程式:________________________________。
【答案】![]()
![]()
![]()
![]()
![]()
![]()
【解析】
(1).焓變小于零為放熱反應;
(2).根據燃燒熱的定義確定燃燒熱的數值;
(3).物質的物質的量與焓變成正比,將質量換算成物質的量,進行計算;
(4).根據蓋斯定律可知,![]() 可得CO燃燒的熱化學方程式;
可得CO燃燒的熱化學方程式;
![]() 的反應屬于放熱反應;
的反應屬于放熱反應;![]() 的反應屬于吸熱反應,根據給出的熱化學方程式可知:
的反應屬于吸熱反應,根據給出的熱化學方程式可知:![]() 三個反應的
三個反應的![]() 都屬于放熱反應,
都屬于放熱反應,
故答案為:![]() ;
;
![]() 根據燃燒熱的定義知:
根據燃燒熱的定義知:![]() 燃燒時生成液態水更穩定,所以
燃燒時生成液態水更穩定,所以![]()
![]()
![]() 就是氫氣的燃燒熱化學方程式,其燃燒熱
就是氫氣的燃燒熱化學方程式,其燃燒熱![]()
![]() ;碳燃燒時生成
;碳燃燒時生成![]() 更穩定,所以
更穩定,所以![]()
![]() 就是碳的燃燒熱化學方程式,其燃燒熱
就是碳的燃燒熱化學方程式,其燃燒熱![]() ,
,
故答案為:![]() ;
;![]() ;
;
![]() 由熱化學方程式
由熱化學方程式![]() 可知:
可知:![]()
![]() ,
,![]() 燃燒生成氣態水放出的熱量為
燃燒生成氣態水放出的熱量為![]() ,則
,則![]() 燃燒生成氣態水放出的熱量為
燃燒生成氣態水放出的熱量為![]() ,
,
故答案為:1429kJ;
![]() 根據蓋斯定律可知,
根據蓋斯定律可知,![]() 可得
可得![]()
![]()
![]()
![]() ,
,
故答案為:![]()
![]() 。
。


科目:高中化學 來源: 題型:
【題目】下列表示戊烷燃燒熱的熱化學方程式正確的是( )
A. C5H12(l)+8O2(g)![]() 5CO2(g) +6H2O(l) ΔH=-3 540 kJ·mol-1
5CO2(g) +6H2O(l) ΔH=-3 540 kJ·mol-1
B. C5H12(l)+8O2(g)![]() 5CO2(g)+6H2O(g) ΔH=-3 540 kJ·mol-1
5CO2(g)+6H2O(g) ΔH=-3 540 kJ·mol-1
C. C5H12(l)+8O2(g)![]() 5CO2(g)+6H2O(g) ΔH=+3 540 kJ·mol-1
5CO2(g)+6H2O(g) ΔH=+3 540 kJ·mol-1
D. C5H12(l)+8O2(g)![]() 5CO2(g)+6H2O(l) ΔH=+3 540 kJ·mol-1
5CO2(g)+6H2O(l) ΔH=+3 540 kJ·mol-1
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】氟化鉻可用作毛織品防蛀劑、鹵化催化劑、大理石硬化及著色劑。以鉻云母礦石(含4.5%Cr2O3,還含Fe2O3、FeO、MgO、SiO2)為原料制備氟化鉻的工藝流程如下。
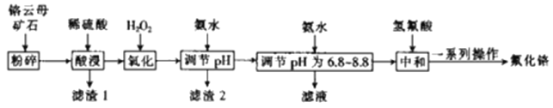
下表列出了相關金屬離子生成氫氧化物沉淀的pH:
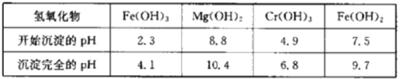
請回答下列問題:
(1)Fe2O3、MgO、FeO、SiO2中屬于堿性氧化物的有___種。
(2)將鉻云母礦石粉碎的目的是___。
(3)濾渣1主要成分的用途是___。(寫一種)
(4)Cr2O3與稀硫酸反應的化學方程式為___。
(5)第一次滴加氨水調節pH范圍為___。
(6)第二次滴加氨水調節pH為6.8~8.8的目的是___,Cr(OH)3與Al(OH)3一樣具有兩性,若第二次滴加的氨水改為NaOH溶液,生成的Cr(OH)3會部分溶解,寫出Cr(OH)3溶解的離子方程式:___。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】石油產品中含有H2S及COS、CH3SH等多種有機硫,石油化工催生出多種脫硫技術。請回答下列問題:
(1)已知熱化學方程式:①2H2S(g)+SO2(g)=3S(s)+2H2O(l) △H=-362kJ·mol-1
②2H2S(g)+3O2(g)=2SO2(g)+2H2O(l) △H2=-1172 kJ·mol-1
則H2S氣體和氧氣反應生成固態硫和液態水的熱化學方程式為___。
(2)可以用K2CO3溶液吸收H2S,其原理為K2CO3+H2S=KHS+KHCO3,該反應的平衡常數為___。(已知H2CO3 的Ka1=4.2×10-7,Ka2=5.6×10-11;H2S的Ka1=5.6×10-8,Ka2=1.2×10-15)
(3)在強酸溶液中用H2O2 可將COS氧化為硫酸,這一原理可用于COS的脫硫。該反應的化學方程式為___。
(4)COS的水解反應為COS(g)+H2O(g)![]() CO2(g)+H2S(g) △H<0。某溫度時,用活性α-Al2O3作催化劑,在恒容密閉容器中COS(g)的平衡轉化率隨不同投料比[n(H2O)/n(COS)]的轉化關系如圖1所示。其它條件相同時,改變反應溫度,測得一定時間內COS的水解轉化率如圖2所示:
CO2(g)+H2S(g) △H<0。某溫度時,用活性α-Al2O3作催化劑,在恒容密閉容器中COS(g)的平衡轉化率隨不同投料比[n(H2O)/n(COS)]的轉化關系如圖1所示。其它條件相同時,改變反應溫度,測得一定時間內COS的水解轉化率如圖2所示:

①該反應的最佳條件為:投料比[n(H2O)/n(COS)]=___,溫度___。
②P點對應的平衡常數為___。(保留小數點后2位)
③當溫度升高到一定值后,發現一定時間內COS(g)的水解轉化率降低;猜測可能的原因是___。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列有關AgCl沉淀的溶解平衡的說法中正確的是( )
A.AgCl沉淀生成和沉淀溶解不斷進行,但速率相等
B.AgCl難溶于水,溶液中沒有Ag+和Cl-
C.升高溫度,AgCl沉淀的溶解度減小
D.在有AgCl沉淀生成的溶液中加入NaCl固體,AgCl沉淀溶解的量不變
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】25℃時,用濃度為0.100 0 mol·L-1的氫氧化鈉溶液分別滴定20.00 mL濃度均為0.100 0 mol·L-1的二種酸HX、HY(忽略體積變化),實驗數據如下表,下列判斷不正確的是 ( )
數據編號 | 滴入NaOH(aq)的體積/mL | 溶液的pH | |
HX | HY | ||
① | 0 | 3 | 1 |
② | a | 7 | x |
③ | 20.00 | >7 | y |
A. 在相同溫度下,同濃度的兩種酸溶液的導電能力:HX<HY
B. 由表中數據可估算出Ka(HX)≈10-5
C. HY和HX混合,c(H+)=c(X-)+c(Y-)+c(OH-)
D. 上述②反應后的HY溶液中:c(Na+)>c(Y-)>c(OH-)>c(H+)
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】在室溫時,向![]() 溶液中滴加
溶液中滴加![]() 溶液,得到溶液pH與NaOH溶液體積的關系曲線如圖所示
溶液,得到溶液pH與NaOH溶液體積的關系曲線如圖所示![]() 無氣體溢出
無氣體溢出![]() ,以下說法不正確的是
,以下說法不正確的是![]()
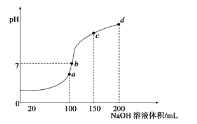
A.a點時水的電離程度最大
B.b點時溶液中的離子濃度關系有![]()
C.c點時溶液中的粒子濃度大小關系為![]()
D.d點時溶液中![]()
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列變化不能用勒夏特列原理解釋的是
A.工業生產硫酸的過程中使用過量的氧氣,以提高二氧化硫的轉化率
B.H2(g)+I2(g)![]() 2HI(g)的平衡體系中壓縮容器體積后顏色變深
2HI(g)的平衡體系中壓縮容器體積后顏色變深
C.Na2CrO4溶液中滴加稀硫酸,溶液顏色變深
D.實驗室用排飽和食鹽水的方法收集氯氣
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】B和Mg在材料科學領域有廣泛的應用和發展前景。
回答下列問題:
(1)下列B原子軌道表達式表示的狀態中,能量更高的是________![]() 填“A”或“B”
填“A”或“B”![]() 。
。
A. ![]() B.
B. ![]()
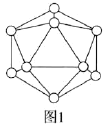
(2)晶體硼中的基本單元如圖1所示,其中含有12個B原子。![]() 該單元中含有
該單元中含有![]() 鍵的數目為________。
鍵的數目為________。
(3)![]() 是重要的還原劑。其中陰離子的立體構型為________,中心原子的雜化形式為________。
是重要的還原劑。其中陰離子的立體構型為________,中心原子的雜化形式為________。
(4)基態Mg原子的核外電子排布式為________;第三周期主族元素中,電負性小于Mg元素的有________![]() 填元素符號,下同
填元素符號,下同![]() ,原子第一電離能小于Mg原子的有________。
,原子第一電離能小于Mg原子的有________。
(5)![]() 和
和![]() 均可作為耐火材料,其原因是________。
均可作為耐火材料,其原因是________。
(6)![]() 常用于光學儀器,其長方體型晶胞結構如圖2所示:
常用于光學儀器,其長方體型晶胞結構如圖2所示:
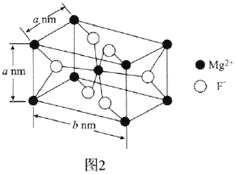
![]() 的配位數為________。
的配位數為________。
![]() 若阿伏加德羅常數的值為
若阿伏加德羅常數的值為![]() ,則
,則![]() 晶體的密度可表示為________
晶體的密度可表示為________![]() 用含a、b、
用含a、b、![]() 的代數式表示
的代數式表示![]() 。
。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com